ŔĚčŔެŠťÇň돊▓┐šÜäšžĹňşŽňĆĹšÄ░´╝îŔüÜšäŽňî╗ŔŹ»ňüąň║Ěń║žńŞÜňĆĹň▒ĽŠľ╣ňÉĹ´╝îŠÉşň╗║šžĹšáöňĺîňĽćńŞÜń╣őÚŚ┤šÜäŠíąŠóüŃÇé
š┐╗Ŕ»Ĺ |┬áNina
Ŕ┤úš╝ľ |┬áÚ╗ĹŠ░┤ń╗Ö ÚúÄňŐĘňşÉ
ŠťČŠťčCellňĆĹŔíĘ1š»çPerspectiveŃÇü1š»çReviewňĺî13š»çArticles´╝îňůÂńŞş4š»çńŞ║Šľ░ňćኝ║ňłÂŃÇüŠ▓╗šľŚšŤŞňů│ŠľçšźáŃÇ銾░ň×őňćášŐšŚůŠ»ĺšÜäňĆśň╝éńŻôŃÇüňĆŚńŻôš╗ôŠ×äŃÇüŔç┤šŚůŠť║ňłÂŃÇüŠťëŠĽłÚóäÚś▓ňĺîŠ▓╗šľŚń╗ŹŠś»ňşŽŠť»šĽîňů│Š│ĘšÜäńŞ╗ŔŽüšžĹňşŽÚŚ«Úóś´╝îńŞ║ň╝ÇňĆĹŠľ░ňćáŠ▓╗šľŚŠľ░ŔŹ»šëęŠëôńŞőňč║šíÇŃÇ銝ȊťčCellň»╣ňłęšöĘšöčšëęšöÁń┐íňĆĚň╣▓ÚóäŔâÜŔâÄňĆĹŔé▓ňĺîň揚öč´╝îň║öšöĘń║Äň揚öčňî╗ňşŽňĺîšÖçŠ▓╗šľŚŔ┐ŤŔíîń║ćň▒ĽŠťŤŃÇéń║║š▒╗ŔéáÚüôŔĆîšżĄšÜäŠ░┤ň╣│ňč║ňŤáŔŻČšž╗ŃÇüń║║ňëŹŔäĹŔ┐Ťňť║ňłÂŃÇüň╗║šźőń║║ňĆúňüąň║ĚšŤĹŠÁőńŻôš│╗šşëšáöšęŠĚ▒ňůąŠÄóš┤óÚÇéň║öŠÇžŔ┐ŤňîľŔžäňżő´╝îńŞ░ň»îń║抳Ĺń╗Čň»╣ń║║š▒╗Ŕ┐ŤňîľšÜäŔ«ĄščąŃÇéń║║-šî┤ňÁîňÉłŔâÜŔâÄšÜ䊳ÉňŐčŠ×äň╗║ŃÇüšöčšëęšöÁń┐íňĆĚň╣▓ÚóäŔâÜŔâÄňĆĹŔé▓ňĺîň揚öčšşëšáöšę´╝îńŞ║Ŕžúňć│ńżŤńŻôňÖĘň«śšÜäńŞąÚ珚躚╝║ÚŚ«Úóśňąáň«Üňč║šíÇŃÇéňĆŚńŻôňĺîÚůŹńŻôšÜäš╗ćŔâ×ňĄľń┐íňĆĚŠĽ┤ňÉłŃÇüŔŤőšÖŻš╗ôŠ×äŔžúŠ×ÉšşëňłćňşÉšöčšëęňşŽšÜäňč║šíÇšáöšę´╝îńŞ║ň╝ÇňĆĹÚçŹŔŽüšÜ䊳ÉŔŹ»ÚŁÂšé╣ŠĆÉńżŤňçćší«šÜäšÉćŔ«║Šö»ŠîüŃÇéňłęšöĘňč║ňŤáňĚąšĘőÚ珚╝ľšĘőÚźôš│╗š╗ćŔâ×´╝îňŐčŔ⯊ǞŔ░âŔŐéňůŹšľźŠŐĹňłÂšÜäŠáŞň┐âŔ┐çšĘő´╝îÚçŹňíĹŔé┐šśĄňůŹšľźňż«šÄ»ňóâ´╝îńŞ║ňůŹšľźšľŚŠ│Ľň╝ÇŔżčń║抍┤ňůĚń╝śňŐ┐šÜ䊾░ŠÇŁŔĚ»ŃÇé

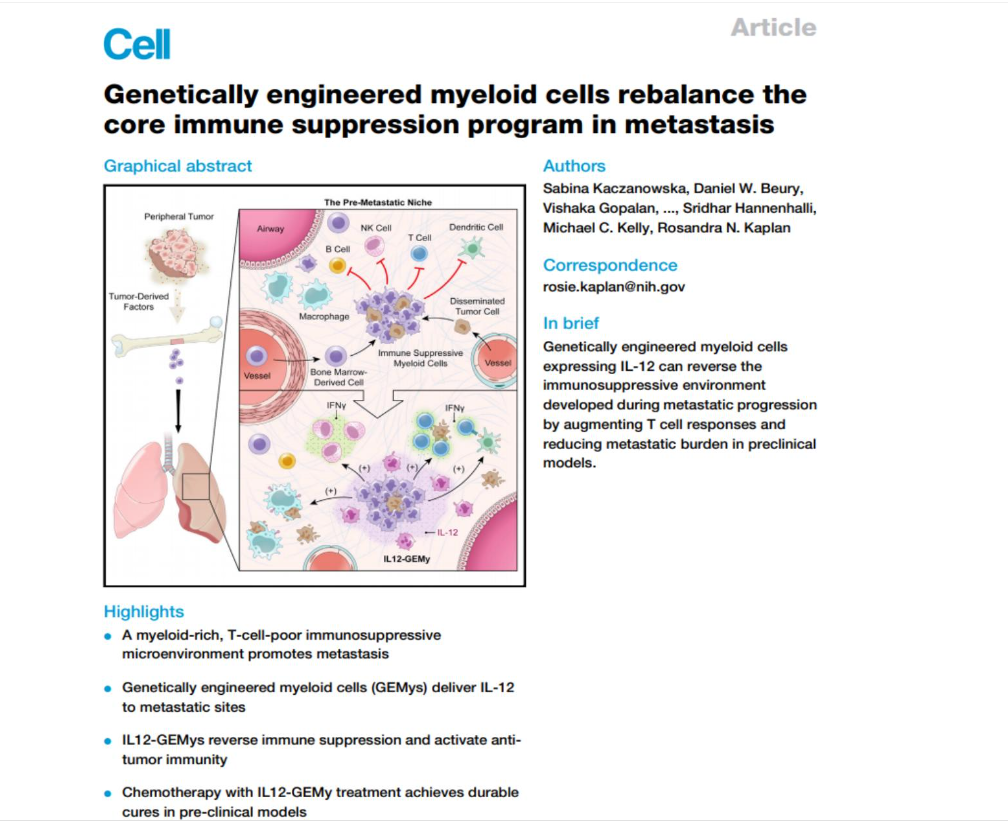
ŠťČš»çŠś»ŠŁąŔ笚żÄňŤŻňŤŻň«ÂšÖçšáöšęŠëÇšÜäRosandra N.KaplanŠĽÖŠÄłňĆĹŔíĘšÜäArticleŠľçšźáŃÇéŔŻČšž╗Šś»šÖçšÜäńŞ╗ŔŽüŠş╗ń║íňÄčňŤá´╝îňŤáŠşĄ´╝îň»╣ŔŻČšž╗ňż«šÄ»ňóâšÜäŠĚ▒ňůąń║ćŔžúŠś»ňŹüňłćň┐ůŔŽüšÜäŃÇéňż«šÄ»ňóâňĆśňîľšÜäňĆĹšö芌ęń║ÄńŞ┤ň║ŐňĆ»ŠúÇŠÁőňł░šÜäŔŻČšž╗ŠÇžšľżšŚů´╝ŤšäÂŔÇî´╝îŔŻČšž╗Ŕ┐çšĘőńŞşňů│Úö«šÜäňż«šÄ»ňóâŔ░âŔŐéń┐íňĆĚń╗ŹńŞŹŠśÄší«ŃÇéŔ┐Öš»çšáöšęÂńŞş´╝îšáöšęÂń║║ňĹśší«ň«Üń║ćÚźôš│╗š╗ćŔâ×ń╗őň»╝šÜäňůŹšľźŠŐĹňłÂŠś»Š×äň╗║Ŕé┐šśĄŔŻČšž╗ň돚öčŠÇüńŻŹšÜäŠáŞň┐âŔ┐çšĘőŃÇéňłęšöĘňč║ňŤáňĚąšĘőÚźôŠáĚš╗ćŔâ×´╝łGEMys´╝ëń╝áÚÇĺIL-12ŠŁąŔ░âŔŐéŔŻČšž╗ŠÇžňż«šÄ»ňóâ´╝îń╗ÄŔÇîÚŁÂňÉĹŔ┐ÖšžŹňůŹšľźŠŐĹňłÂŔ┐çšĘőŃÇéš╗ôŠ×ťŔíĘŠśÄ´╝îIL12-GEMysňĆ»ń╗ąňŐčŔ⯊Ǟňť░Ŕ░âŔŐéŔŻČšž╗ň돚öčŠÇüńŻŹńŞşňůŹšľźŠŐĹňłÂšÜäŠáŞň┐âŔ┐çšĘő´╝îń╗ÄŔÇÉňŐčňť░Ú珊ľ░ň╣│ŔííšÖçńŞşňĄ▒Ŕ░âšÜäŔŻČšž╗ňż«šÄ»ňóâŃÇéŔ┐ÖšžŹŠ┐ÇŠ┤╗ŠŐŚňÄčňĹłÚÇĺňĺîTš╗ćŔâ׊┤╗ňŁąÚÇćŔŻČŔŻČšž╗ň돚öčŠÇüńŻŹńŞşšÜäňůŹšľźŠŐĹňłÂŠť║ňłÂ´╝îÚÇÜŔ┐çňçĆň░ĹŔŻČšž╗ŠÇžňĺîňÄčňĆĹŠÇžŔé┐šśĄ´╝îŠĆÉÚźśŔŹĚšśĄň░ĆÚ╝ášÜäňşśŠ┤╗šÄçŃÇé´╝łŠĹśŔŽü´╝ë(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.02.048)
ŠŐĽŔÁäÚó䊝č´╝ÜŔé┐šśĄňůŹšľźšľŚŠ│ĽŠś»ňŻôň돚Üäňî╗šľŚňĆĹň▒ĽŔÂőňŐ┐ŠëÇňťĘ
šÖŻš╗ćŔâ×ń╗őš┤á´╝łIL-12´╝늜»Úźôš│╗š╗ćŔâ×ń║žšöčšÜäš╗ćŔâ×ňŤáňşÉń╣őńŞÇŃÇéńŞÇŔłČŠâůňćÁńŞő´╝îňťĘŠäčŠčôňĺîŔé┐šśĄňç║šÄ░ŠŚÂ´╝îÚźôš│╗š╗ćŔâ×ń╝Üń║žšöčIL-12´╝îŠ┐ÇŠ┤╗Tš╗ćŔâ×ňĺîŔ笚䊣Çń╝Ą´╝łNK´╝ëš╗ćŔâ×´╝îŔ┐śń╝Üňó×ň╝║ň╣▓Šë░š┤á╬│´╝łIFN-╬│´╝ëňĆŹň║ö´╝îňó×ňŐáŠŐŚňÄčňĹłÚÇĺ´╝îňçĆň░ĹŔíÇš«íšö芳ɚşëŔ┐çšĘőŃÇéňÄ芝Ȋś»ňŞ«ňŐꊝ║ńŻôŠŐŚšÖîšÜäÚźôš│╗š╗ćŔâ×´╝îňťĘŔé┐šśĄšÜäŔ»▒ň»╝ńŞő´╝îńŻ┐Úźôš│╗š╗ćŔâ×ňłćŠ│îIL-12šÜäŔâŻňŐŤňçĆň╝▒´╝îń╗ÄŔÇîňĄ▒ňÄ╗Ŕé┐šśĄŠŐĹňłÂŃÇéňŤáŠşĄ´╝îŔ┐Öš»çšáöšęšÜ䚍«šÜäňťĘń║Äň╝║Ŕíîňó×ň╝║Úźôš│╗š╗ćŔâ×ňłćŠ│îIL-12šÜäŔâŻňŐŤ´╝îŠüóňĄŹňůŠՌšÖîŔâŻňŐŤŃÇé90%šÜäšÖ犺╗ń║튜»ŔŻČšž╗ň»╝Ŕç┤šÜäŃÇéÚÇÜŔ┐çňč║ňŤáňĚąšĘőŠö╣ÚÇáÚźôš│╗š╗ćŔâ×´╝îňłęšöĘň«âń╗ČŠśôň»îÚŤćňťĘŔŻČšž╗ň돚öčŠÇüńŻŹšÜäšë╣šé╣´╝îňÉĹšÖîš╗ćŔâ×ŔŻČšž╗šŤ«šÜäňť░ÚçŐŠöżň╝║ňĄžšÜäŠŐŚšÖîń┐íňĆĚ´╝îń╗ÄŔÇîň«×šÄ░ÚĽ┐ń╣ůšÜäŠŐĹňłÂšÖçŔŻČšž╗ŠĽłŠ×ťŃÇéÚÖĄŠťČšáöšęÂńŞşKaplanŠĽÖŠÄłňŤóÚśčŠĆÉňç║šÜäŠö╣ÚÇáÚźôš│╗š╗ćŔâ×ňĄľ´╝îňůŹšľźšľŚŠ│ĽŔ┐śŠťëńŞÇńެŠÇŁŔĚ»Šś»ŔÇŚšźşňůŹšľźŠŐĹňłÂÚźôš│╗š╗ćŔâ×ŃÇéńŻćŔ┐çň║ŽšÜäŠÂłŔÇŚń╝ÜńŻ┐ŠéúŔÇůňůŹšľźňŐčŔâŻňĆŚŠŹč´╝îÚŁóńŞ┤ŠäčŠčôÚúÄÚÖę´╝îŔ┐śňĆ»ŔâŻńŻ┐ňůŹšľźŠŐĹňłÂÚźôš│╗š╗ćŔâ×ňĆŹň╝╣´╝îń╗ÄŔÇîňŐáÚÇčŔé┐šśĄšöčÚĽ┐ŃÇéšŤŞŠ»öń╣őńŞő´╝îšöĘÚźôš│╗š╗ćŔâ×ńŻťńŞ║ň╣│ňĆ░ŠŁąÚçŹňíĹňůŹšľźŠŐĹňłÂňż«šÄ»ňóâšÜäšşľšĽąŠŤ┤Šśżń╝śňŐ┐ŃÇéŔé┐šśĄňůŹšľźŠŐĹňłÂňż«šÄ»ňóâšÜäÚçŹňíĹ´╝îš▒╗ń╝╝PD-1/PDL-1šşëňůŹšľźŠúÇŠčąšé╣Šť║ňłÂ´╝늝ŤńŻťńŞ║Ŕé┐šśĄŠ▓╗šľŚšÜäňč║šíÇšöĘŔŹ»´╝îńŞÄšÄ░ŠťëŔé┐šśĄŠ▓╗šľŚŠľ╣Š│ĽŠ×䊳ɚ╗äňÉłšľŚŠ│Ľ´╝îňó×ň╝║Ŕé┐šśĄŠ▓╗šľŚŠĽłŠ×ťŃÇéŠáŞň┐âŠŐÇŠť»šŚŤšé╣´╝Üń║║Úźôš╗ćŔâךÜäÚ珚╝ľšĘőŠŐÇŠť»ÚÜżň║ŽŔżâÚźś´╝ÉňŐčšÄçŔżâńŻÄňłęšöĘÚźôš│╗š╗ćŔâ×ň«╣ŠśôňÉĹŔé┐šśĄňĺîŔŻČšž╗ÚâĘńŻŹŔüÜÚŤćšÜäšë╣šé╣´╝îň»╣ń║║Úźôš╗ćŔâ×Ŕ┐ŤŔíîňč║ňŤáŠö╣ÚÇá´╝îÚťÇńŻ┐Šö╣ÚÇáňÉÄšÜäń║║š▒╗Úźôš│╗š╗ćŔâ×´╝łGEMys´╝ëŔâŻňĄčŔ┐çŔíĘŔżżIL-12´╝îň╣ÂŔ⯊ťëŠĽłŠ┐ÇŠ┤╗ňůŹšľźš╗ćŔâ×ŃÇ銺ĄÚí╣IL-12-GEMysde Š×äň╗║ŠÁüšĘőŔżâňĄŹŠŁé´╝îŠŐÇŠť»ň╣│ňĆ░ÚŚĘŠžŤÚźś´╝ÉňŐčšÄçŔżâńŻÄŃÇ銺ĄňĄľ´╝îIL-12ňťĘń║║ńŻôńŞşŠö╣ňľäňůŹšľźňż«šÄ»ňóâšÜäńŻťšöĘň░ÜňżůÚ¬îŔ»üŃÇé
ňŤŻňćůŠŐĽŔÁäŠíłńżő´╝ÜńŞ░Š║ÉŔŹ»ńŞÜŔ┤şňůąńŞşšžĹňĄžÔÇťń║║Ú珚╗äšÖŻń╗őš┤á-12ŔŹ»šëęÔÇŁŠŐÇŠť»ŠłÉŠ×ť
2015ň╣┤10Šťł´╝îň«ëňżŻńŞ░ňÄčŔŹ»ńŞÜŔéíń╗ŻŠťëÚÖÉňůČňĆŞń╗ą5000ńŞçňůâŔ┤şňůąńŞşňŤŻšžĹňşŽŠŐÇŠť»ňĄžňşŽšÜäÔÇťń║║Ú珚╗äšÖŻń╗őš┤á-12ŔŹ»šëęÔÇŁ šÜ䚞ŊŐÇŠłÉŠ×ťŃÇéńŞşšžĹňĄžŔ┤čŔ┤úň«îŠłÉÔÇťń║║Ú珚╗äšÖŻń╗őš┤á-12ŔŹ»šëęÔÇŁńŞ┤ň║ŐŔ»ĽÚ¬îšö│Ŕ»ĚňĆŚšÉćŠëÇŔŽüŠ▒éšÜäňůĘÚâĘŠŐÇŠť»ŔÁ䊾ִ╝îň╣Âň░抺ĄŔŐéšé╣ńŻťńŞ║ŠŐÇŠť»ŠłÉŠ×ťŔŻČŔ«ęš╗ÖńŞ░Š║ÉŔŹ»ńŞÜŃÇ隍«ňëŹÔÇťń║║Ú珚╗äšÖŻń╗őš┤á-12ŔŹ»šëęÔÇŁňĚ▓šö│Ŕ»Ě1š▒╗Šľ░ŔŹ»ŃÇé
ňŤŻňĄľŠŐĽŔÁäŠíłńżő´╝ÜšÖżŠŚÂšżÄŠľŻŔ┤Áň«ŁŔÄĚDragonflyň╝ÇňĆĹšÜäIL-12ňťĘšáöń║žňôüňůĘšÉâšőČň«ÂŔ«ŞňĆ»
2020ň╣┤8Šťł´╝îšÖżŠŚÂšżÄŠľŻŔ┤Áň«Ł(BMS)ŔÄĚňżŚDragonflyňůČňĆŞň╝ÇňĆĹšÜäIL-12ňťĘšáöňůŹšľźšľŚŠ│ĽDF6002šÜäňůĘšÉâšőČň«ÂŔ«ŞňĆ»ŃÇéšÖżŠŚÂšżÄŠľŻŔ┤Áň«ŁŔ┤čŔ┤úDF6002ňĆŐňůšŤŞňů│ń║žňôüňťĘňůĘšÉâŔîâňŤ┤ňćůšÜäň╝ÇňĆĹňĺîňÉÄš╗şŠÄĘň╣┐´╝îDragonflyňůČňĆŞŔÄĚ4.75ń║┐šżÄňůâšÜäň돊ťčń╗śŠČż´╝îň╣ŠťëŔÁäŠá╝ŔÄĚňżŚňÉÄš╗şÚçîšĘőšóĹń╗śŠČż´╝îń╗ąňĆŐŠť¬ŠŁąń║žňôüÚöÇňö«ÚóŁšÜäňłćŠłÉŃÇé
DF6002Šś»ńŞÇšžŹňŹĽń╗ĚIL-12š╗ćŔâ×ňŤáňşÉńŞÄFcŔ׏ňÉłňŻóŠłÉšÜäŔ׏ňÉłŔŤőšÖŻ´╝îňůĚŠťëň╗ÂÚĽ┐šÜäňŹŐŔí░Šťč´╝îňĆ»ÚÇÜŔ┐çň╗║šźőń║žšöčŠŐŚŔé┐šśĄňĆŹň║öŠëÇň┐ůڝǚÜäšéÄŠÇžŔé┐šśĄňż«šÄ»ňó⊣ąŔżżňł░ň╝║ňŐŤšÜäŠŐŚŔé┐šśĄŠĽłŠ×ťŃÇéň«âšÜäINDšö│Ŕ»ĚňĚ▓š╗ĆňťĘ2020ň╣┤5ŠťłŔÄĚňżŚšżÄňŤŻFDAšÜäŠë╣ňçćŃÇéÚĺłň»╣ŠÖÜŠťčň«×ńŻôšśĄŠéúŔÇůšÜä1/2ŠťčńŞ┤ň║ŐŔ»ĽÚ¬îňĚ▓š╗ĆňÉ»ňŐĘŃÇéšÖżŠŚÂšżÄŠľŻŔ┤Áň«ŁšŤ«ňëŹŔ«íňłĺŔ┐ŤńŞÇŠşąŠÄĘŔ┐ŤDF6002ňťĘŔé┐šśĄňşŽňĺîŔíÇŠÂ▓ňşŽÚóćňččšÜäšáöňĆĹŃÇé

ń║îŃÇüŔé║Ŕí░ŔÇü
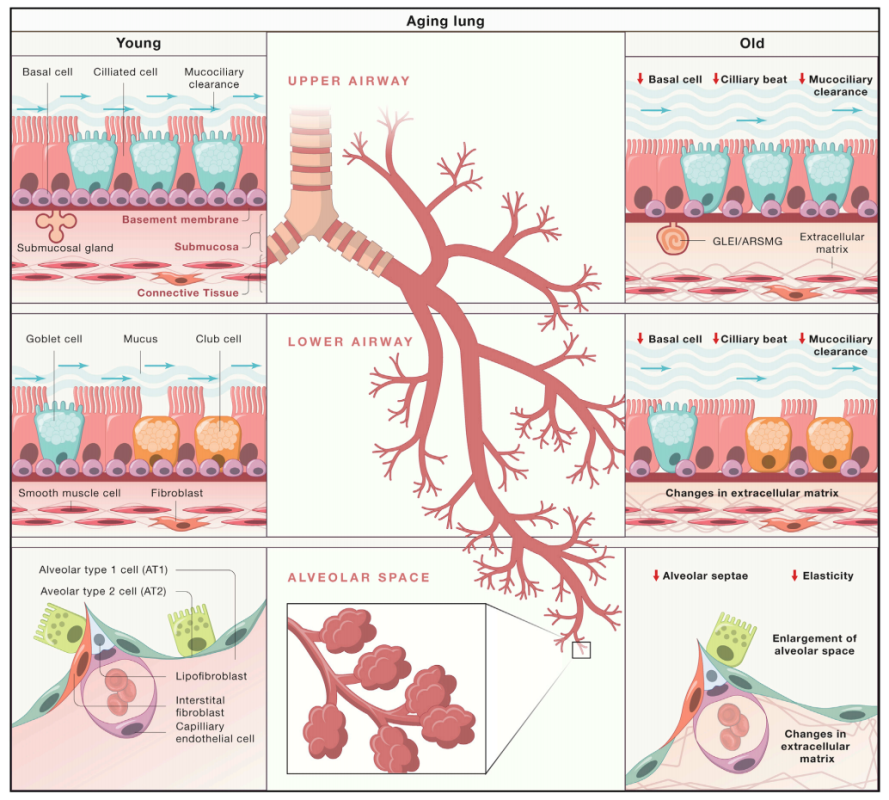 ŠťČš»çŠś»ŠŁąŔç¬ňôłńŻŤňĄžňşŽňî╗ňşŽÚÖóšÜäMarcia C. HaigisňŤóÚśčňĆĹŔíĘšÜäš╗╝Ŕ┐░´╝îŠÇ╗š╗ôń║ćňťĘŔé║Ŕí░ŔÇüŔ┐çšĘőńŞşňłćňşÉňĺîš╗ćŔâ×ň▒éÚŁóšÜäŠö╣ňĆśŃÇüň▒ÇÚâĘň║öŠ┐ÇňĆŹň║öÚÇÜŔĚ»šÜäňĆśňîľ´╝îń╗ąňĆŐŔí░ŔÇüŔ┐çšĘőŔé║ÚâĘšľżšŚůšÜäňĆĹšöčňĆĹň▒ĽŠť║ňłÂ´╝îň╣š╗ôňÉłCOVID-19ňĄžŠÁüŔíîšÜäŔâîŠÖ»´╝îŠÄóŔ«ĘŔé║ňćůňůłňĄęňůŹšľźňĺîÚÇéň║öŠÇžňůŹšľźÚÜĆšŁÇň╣┤ÚżäňĆśňîľšÜäšë╣šé╣ŃÇéŔ┐Öš»çš╗╝Ŕ┐░ÚśÉŔ┐░ň║öšöĘňŹĽš╗ćŔâ×ŔŻČňŻĽŔ░▒ňłćŠ×ÉňĺîÚüŚń╝áŔ░▒š│╗Ŕ┐ŻŔެŠŐÇŠť»´╝îŠĆşšĄ║šë╣ň«Üš╗ćŔâך▒╗ň×őňĺîňż«šÄ»ňóâňťĘŔí░ŔÇüŔ┐çšĘőńŞşňŽéńŻĽňĆĹšöčŠö╣ňĆśŃÇéÚźśÚÇÜÚçĆŃÇüňĄÜň▒éŠČíŃÇüňĄÜš╗äňşŽŠľ╣Š│Ľń╣芝ëňĆ»ŔâŻŔ┐ŤńŞÇŠşąŠö╣ňĆśŠłĹń╗Čň»╣ň╣┤ڿ䚍Şňů│Ŕé║ÚâĘšľżšŚůŠť║ňłÂšÜäšÉćŔžúŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.005)
ŠťČš»çŠś»ŠŁąŔç¬ňôłńŻŤňĄžňşŽňî╗ňşŽÚÖóšÜäMarcia C. HaigisňŤóÚśčňĆĹŔíĘšÜäš╗╝Ŕ┐░´╝îŠÇ╗š╗ôń║ćňťĘŔé║Ŕí░ŔÇüŔ┐çšĘőńŞşňłćňşÉňĺîš╗ćŔâ×ň▒éÚŁóšÜäŠö╣ňĆśŃÇüň▒ÇÚâĘň║öŠ┐ÇňĆŹň║öÚÇÜŔĚ»šÜäňĆśňîľ´╝îń╗ąňĆŐŔí░ŔÇüŔ┐çšĘőŔé║ÚâĘšľżšŚůšÜäňĆĹšöčňĆĹň▒ĽŠť║ňłÂ´╝îň╣š╗ôňÉłCOVID-19ňĄžŠÁüŔíîšÜäŔâîŠÖ»´╝îŠÄóŔ«ĘŔé║ňćůňůłňĄęňůŹšľźňĺîÚÇéň║öŠÇžňůŹšľźÚÜĆšŁÇň╣┤ÚżäňĆśňîľšÜäšë╣šé╣ŃÇéŔ┐Öš»çš╗╝Ŕ┐░ÚśÉŔ┐░ň║öšöĘňŹĽš╗ćŔâ×ŔŻČňŻĽŔ░▒ňłćŠ×ÉňĺîÚüŚń╝áŔ░▒š│╗Ŕ┐ŻŔެŠŐÇŠť»´╝îŠĆşšĄ║šë╣ň«Üš╗ćŔâך▒╗ň×őňĺîňż«šÄ»ňóâňťĘŔí░ŔÇüŔ┐çšĘőńŞşňŽéńŻĽňĆĹšöčŠö╣ňĆśŃÇéÚźśÚÇÜÚçĆŃÇüňĄÜň▒éŠČíŃÇüňĄÜš╗äňşŽŠľ╣Š│Ľń╣芝ëňĆ»ŔâŻŔ┐ŤńŞÇŠşąŠö╣ňĆśŠłĹń╗Čň»╣ň╣┤ڿ䚍Şňů│Ŕé║ÚâĘšľżšŚůŠť║ňłÂšÜäšÉćŔžúŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.005)
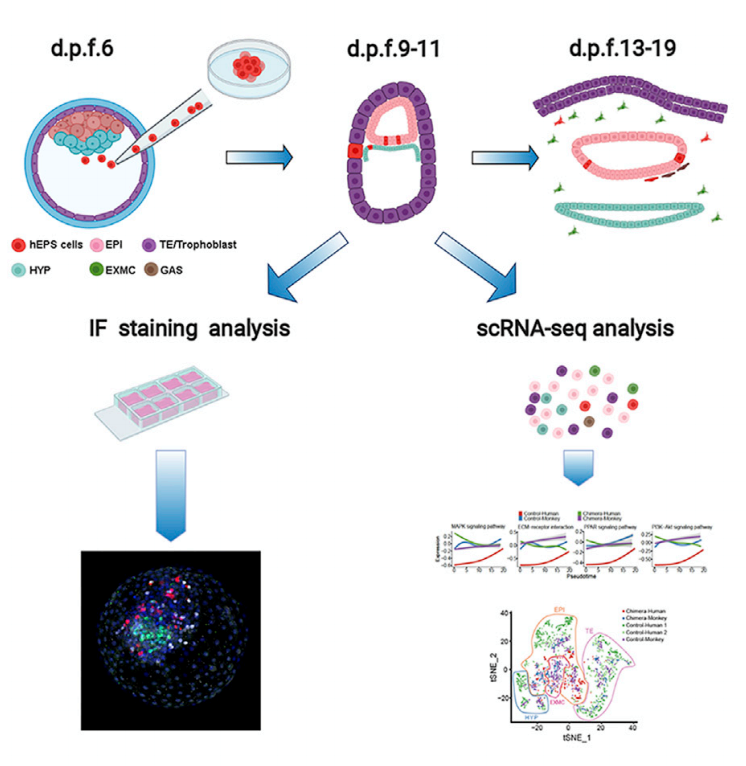
ńŞëŃÇüń║║-šî┤ňÁîňÉłŔâÜŔâÄšÜ䊳ÉňŐčŠ×äň╗║
ŠťČš»çŠś»ŠŁąŔç¬ńŞşňŤŻŠśćŠśÄšÉćňĚąňĄžňşŽšÜäňşúš╗┤ŠÖ║ÚÖóňúźŃÇüŔ░şÚčČŠĽÖŠÄłŃÇüšëŤŠś▒ň«çŠĽÖŠÄłňĺîšżÄňŤŻŠ▓ÖňůőšöčšëęňşŽšáöšęÂńŞşň┐âšÜäJuan Carlos Izpisua Belmonteňů▒ňÉîňĆĹŔíĘšÜäArticleŠľçšźáŃÇéňĄÜŔâŻň╣▓š╗ćŔâ×´╝łPSC´╝늜»ńŞÇš▒╗ŔâŻŔ笊łĹŠŤ┤Šľ░ň╣Âń║žšöčŠëÇŠťëŠłÉň╣┤š╗ćŔâך▒╗ň×őšÜäš╗ćŔâ×ŃÇéń║║ňĄÜŔâŻň╣▓š╗ćŔâ×´╝łhPSC´╝ëšÜäšžŹÚŚ┤ňÁîňÉłńŻôňŻóŠłÉŠś»Ŕ»äń╝░ńŻôňćůhPSCňĄÜŔ⯊ǞšÜ䊝늼łÚÇöňżä´╝îňůĚŠťëŠŻťňŐŤńŞ║ň揚öčňî╗ňşŽň║öšöĘŠĆÉńżŤňĄžÚçĆńŻôňćůšö芳ɚÜäń║║š▒╗š╗ćŔâ×ŃÇüš╗äš╗çňĺîňÖĘň«ś´╝îňîůŠőČňÖĘň«śšž╗ŠĄŹŃÇéń╗ąňżÇšáöšęÂňĄÜńŻ┐šöĘň░ĆÚ╝ášşëňĽ«ÚŻ┐š▒╗ňŐĘšëęšÜäŔâÜŔâÄŔ┐ŤŔíîňÁîňÉłńŻôšáöšę´╝îńŻćňşśňťĘńŞÄń║║š▒╗Ŕ┐ŤňîľŔĚŁšŽ╗ÚüąŔ┐ťŃÇüń╝ŽšÉćÚŚ«ÚóśšşëŃÇéńŞÄń╗ąňżÇšáöšęÂńŞŹňÉî´╝Ț»çšáöšęÂÚŽľŠČíňťĘńŻôňĄľňłÂňĄçňç║šö▒ń║║š▒╗ňĄÜŔâŻň╣▓š╗ćŔâ×´╝łhEPSCs´╝ëňĺîÚúčŔč╣šî┤´╝łMacaca fascicularis´╝ëŔâÜŔâÄš╗ćŔâך╗䊳ɚÜäÔÇťňÁîňÉłńŻôÔÇŁŔâÜŔâÄ´╝îŠĆÉňŹçń║ćhEPSCsńŻôňĄľšöčňşśŃÇüňó׊«ľŠ░┤ň╣│´╝îň╣ÂňťĘšî┤ŔâÜŔâÄňćůňłćňîľń║ćňçáńެš╗ćŔâ×Ŕ░▒š│╗´╝îň░抺ĄňÁîňÉłńŻôňťĘńŻôňĄľňşśŠ┤╗ŠŚÂÚŚ┤ŠĆÉňŹçŔç│20ňĄęŃÇéňĆŽňĄľňłęšöĘňŹĽš╗ćŔâ×ŔŻČňŻĽš╗äŠŐÇŠť»´╝łŔ»ąŠÁőň║ĆŠťŹňŐ튝ëň«ëŔ»║ń╝śŔżżŠĆÉńżŤ´╝ëň»╣ňÁîňÉłńŻôń║║šî┤š╗ćŔâ×ń╣őÚŚ┤šÜäń║Ąń║劾╣ň╝ĆŔ┐ŤŔíîń║ćŠÄóŔ«Ę´╝îň░抝ëňŐęń║ÄŠŤ┤ňąŻňť░šÉćŔžúń║║š▒╗šÜ䊌ꊝčňĆĹŔé▓ňĺîšüÁÚĽ┐š▒╗ňŐĘšëęšÜäŔ┐Ťňîľ´╝îń╗ąÚÇéň║öŔ┐ŤňîľŔĚŁšŽ╗ÚüąŔ┐ťšÜäšëęšžŹŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.020)
ňŤŤŃÇüš╗ćŔâ×ňĄľń┐íňĆĚšÜ䊼┤ňÉł
ŠťČš»çŠś»ŠŁąŔ笚덊┤ąňĄžňşŽŠâáň║Ěń║║š▒╗ÚüŚń╝áňşŽńŞşň┐âš╗ôŠ×äšöčšëęňşŽšžĹšÜäChristian SieboldŠĽÖŠÄłňŤóÚśčňĆĹŔíĘšÜäArticleŃÇéňťĘš╗ćŔâ×Ŕ┐üšž╗ŠłľňłćňîľŔ┐çšĘőńŞş´╝îš╗ćŔâ×ŔíĘÚŁóňĆŚńŻôňÉŠÜ┤Úť▓ń║ÄńŞŹňÉîšÜäÚůŹńŻô´╝îńŻćÚÇÜňŞŞńŞŹŠŞůŠąÜŔ┐Öń║Ťš╗ćŔâ×ňĄľń┐íňĆĚňŽéńŻĽŠĽ┤ňÉłŃÇéňŻôNetrin-1´╝łNET1´╝ëÚůŹńŻôš╗ôňÉłŠŚÂ´╝îNeogenin´╝łNEO1´╝ëňůůňŻôňÉŞň╝ĽŠÇžŠîçň»╝ňĆŚńŻô´╝îńŻćň«âÚÇÜŔ┐çŠÄ劾ąŠÇžŠîçň»╝ňłćňşÉ´╝łRGM´╝ëÚůŹńŻôń╗őň»╝ŠÄ劾ąŃÇéšáöšęÂŔíĘŠśÄń┐íňĆĚŠĽ┤ňÉłŠś»ÚÇÜŔ┐çńŞëňůâNEO1-NET1-RGMňĄŹňÉłšëęšÜäňŻóŠłÉŔÇîňĆĹšöčšÜä´╝îň«âń╝ÜŔžŽňĆĹńŞőŠŞŞń┐íňĆĚšÜ䚍Şń║ĺŠ▓ëÚ╗śŃÇéNEO1-NET1-RGMš╗ôŠ×äŠĆşšĄ║ń║ćňşśňťĘń║Äš╗ćŔâ×ŔćťńŞşšÜäÔÇťńŞëŔüÜńŻôÔÇŁŔÂůš╗äŔúůńŻôŃÇéŔÂůš║žŔúůÚůŹńŻôňŻóŠłÉÚÇÜŔ┐çŠŐĹňłÂń┐íňĆĚňů╝ň«╣šÜäRGM-NEO1ňĄŹňÉłńŻôňĺîNET1Ŕ»▒ň»╝šÜäNEO1Ŕâ×ňĄľňččš░çšÜäňŻóŠłÉ´╝îń╗ÄŔÇîŠŐĹňłÂń║ćRGMA-NEO1ń╗őň»╝šÜäšöčÚĽ┐ÚöąňíîÚÖĚňĺîRGMA-ŠłľNET1-NEO1ń╗őň»╝šÜ䚹ך╗ĆňůâŔ┐üšž╗ŃÇéŔ┐Öń║Ťš╗ôŠ×ťŔ»┤ŠśÄń║ćňůĚŠťëšŤŞňĆŹňŐčŔ⯚ÜäÚůŹńŻôňÉš╗ôňÉłňł░ňŹĽńެňĆŚńŻôŠś»ňŽéńŻĽÚü┐ňůŹš╗ôňÉłšź×ń║ëšÜä´╝»ÚÇÜŔ┐çňŻóŠłÉňëŐň╝▒ňůÂňŐčŔâŻŔżôňç║šÜäŔÂůňĄŹňÉłšëęšÜäňŻóň╝ĆŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.02.045)





 ŠťČš»çŠś»ŠŁąŔç¬ňôłńŻŤňĄžňşŽňî╗ňşŽÚÖóšÜäMarcia C. HaigisňŤóÚśčňĆĹŔíĘšÜäš╗╝Ŕ┐░´╝îŠÇ╗š╗ôń║ćňťĘŔé║Ŕí░ŔÇüŔ┐çšĘőńŞşňłćňşÉňĺîš╗ćŔâ×ň▒éÚŁóšÜäŠö╣ňĆśŃÇüň▒ÇÚâĘň║öŠ┐ÇňĆŹň║öÚÇÜŔĚ»šÜäňĆśňîľ´╝îń╗ąňĆŐŔí░ŔÇüŔ┐çšĘőŔé║ÚâĘšľżšŚůšÜäňĆĹšöčňĆĹň▒ĽŠť║ňłÂ´╝îň╣š╗ôňÉłCOVID-19ňĄžŠÁüŔíîšÜäŔâîŠÖ»´╝îŠÄóŔ«ĘŔé║ňćůňůłňĄęňůŹšľźňĺîÚÇéň║öŠÇžňůŹšľźÚÜĆšŁÇň╣┤ÚżäňĆśňîľšÜäšë╣šé╣ŃÇéŔ┐Öš»çš╗╝Ŕ┐░ÚśÉŔ┐░ň║öšöĘňŹĽš╗ćŔâ×ŔŻČňŻĽŔ░▒ňłćŠ×ÉňĺîÚüŚń╝áŔ░▒š│╗Ŕ┐ŻŔެŠŐÇŠť»´╝îŠĆşšĄ║šë╣ň«Üš╗ćŔâך▒╗ň×őňĺîňż«šÄ»ňóâňťĘŔí░ŔÇüŔ┐çšĘőńŞşňŽéńŻĽňĆĹšöčŠö╣ňĆśŃÇéÚźśÚÇÜÚçĆŃÇüňĄÜň▒éŠČíŃÇüňĄÜš╗äňşŽŠľ╣Š│Ľń╣芝ëňĆ»ŔâŻŔ┐ŤńŞÇŠşąŠö╣ňĆśŠłĹń╗Čň»╣ň╣┤ڿ䚍Şňů│Ŕé║ÚâĘšľżšŚůŠť║ňłÂšÜäšÉćŔžúŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.005)
ŠťČš»çŠś»ŠŁąŔç¬ňôłńŻŤňĄžňşŽňî╗ňşŽÚÖóšÜäMarcia C. HaigisňŤóÚśčňĆĹŔíĘšÜäš╗╝Ŕ┐░´╝îŠÇ╗š╗ôń║ćňťĘŔé║Ŕí░ŔÇüŔ┐çšĘőńŞşňłćňşÉňĺîš╗ćŔâ×ň▒éÚŁóšÜäŠö╣ňĆśŃÇüň▒ÇÚâĘň║öŠ┐ÇňĆŹň║öÚÇÜŔĚ»šÜäňĆśňîľ´╝îń╗ąňĆŐŔí░ŔÇüŔ┐çšĘőŔé║ÚâĘšľżšŚůšÜäňĆĹšöčňĆĹň▒ĽŠť║ňłÂ´╝îň╣š╗ôňÉłCOVID-19ňĄžŠÁüŔíîšÜäŔâîŠÖ»´╝îŠÄóŔ«ĘŔé║ňćůňůłňĄęňůŹšľźňĺîÚÇéň║öŠÇžňůŹšľźÚÜĆšŁÇň╣┤ÚżäňĆśňîľšÜäšë╣šé╣ŃÇéŔ┐Öš»çš╗╝Ŕ┐░ÚśÉŔ┐░ň║öšöĘňŹĽš╗ćŔâ×ŔŻČňŻĽŔ░▒ňłćŠ×ÉňĺîÚüŚń╝áŔ░▒š│╗Ŕ┐ŻŔެŠŐÇŠť»´╝îŠĆşšĄ║šë╣ň«Üš╗ćŔâך▒╗ň×őňĺîňż«šÄ»ňóâňťĘŔí░ŔÇüŔ┐çšĘőńŞşňŽéńŻĽňĆĹšöčŠö╣ňĆśŃÇéÚźśÚÇÜÚçĆŃÇüňĄÜň▒éŠČíŃÇüňĄÜš╗äňşŽŠľ╣Š│Ľń╣芝ëňĆ»ŔâŻŔ┐ŤńŞÇŠşąŠö╣ňĆśŠłĹń╗Čň»╣ň╣┤ڿ䚍Şňů│Ŕé║ÚâĘšľżšŚůŠť║ňłÂšÜäšÉćŔžúŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.005)