

š┐╗Ŕ»Ĺ | Howard
Ŕ┤úš╝ľ | YYY ÚúÄňŐĘňşÉ
ŠťČŠťčCellňů▒ňĆĹŔíĘ3š»çPreviewsŃÇü1š»çPrimerňĺî12š»çArticlesŃÇü2š»çResourcesŃÇéÚŽľŠČíňĆĹšÄ░ňĆ»ÚÇÜŔ┐çÚŁÂňÉĹÚĺÖ/ÚĺÖŔ░âš┤áŔŤőšÖŻńżŁŔÁľšÜäŔŤőšÖŻŠ┐ÇÚůÂII´╝łCaMKII´╝ëšÜäAAVňč║ňŤáŠ▓╗šľŚ´╝îń┐ŁŠŐĄŔžćšŻĹŔćťšą×š╗ĆŔŐéš╗ćŔâ× (RGC)ňůŹňĆŚŠŹčń╝Ą´╝îÚś╗Šşóšö▒ÚŁĺňůëšť╝ŃÇüš│ľň░┐šŚůŔžćšŻĹŔćťšŚůňĆśšşëň»╝Ŕç┤šÜäŔžćňŐŤŔí░ÚÇÇŃÇéÚŁÂňÉĹŔéáÚüôňż«šöčšëęšżĄšÜäÚą«ÚúčňĆ»Ŕ░âŔŐéń║║ńŻôňůŹšľźšŐŠÇüŃÇéÚŽľŠČíš╗śňłÂňç║ŠťÇňĄžŃÇüŠťÇňůĘÚŁóšÜäŔé║Ú│ךŐš╗ćŔâךÖîšÜäŔŤőšÖŻŔ┤Ęňč║ňŤáš╗äňŤżŔ░▒´╝îň»╣Ŕé║Ú│ךŐš╗ćŔâךÖîšÜäŠ▓╗šľŚňůĚŠťëŠîçň»╝ŠäĆń╣ëŃÇéňĄÜŔâ║ń╗úŔ░óňĆ»ŠÄžňłÂCD4+ŔżůňŐęTš╗ćŔâ×(TH)ňłćňîľńŞ║ńŞŹňÉîňŐčŔ⯚Üäš╗ćŔâ×´╝îńŞöŔ┐ÉšöĘcompassš«ŚŠ│Ľň░ćń╗úŔ░óšŐŠÇüńŞÄŔżůňŐęŠÇžTš╗ćŔâ×17´╝łTh17´╝ëňŐčŔâŻňĆśň╝éŠÇžšŤŞňů│Ŕüö´╝îň╣ÂÚÇÜŔ┐çń╗úŔ░óňłćŠ×ÉňżŚňł░Ú¬îŔ»üŃÇé


šŤ«ň돴╝îŔžćšŻĹŔćťšŚůňĆśšÜäŠ▓╗šľŚŠľ╣Š│ĽŠťëńŞëšžŹ´╝ÜŠ┐ÇňůëŠ▓╗šľŚŃÇüVEGFŠŐĹňłÂňëéŠ│Ęň░äŃÇüšÄ╗šĺâńŻôňłçÚÖĄŠť»ŃÇéŠ┐ÇňůëŠ▓╗šľŚŠŚóšöĘń║ÄňóךöčŠÇžŔžćšŻĹŔćťšŚůňĆśňĆłšöĘń║ÄÚ╗䊾ŚŚůňĆś´╝îńŻćń╝Üň»╝Ŕç┤10%šÜäŔžćňŐŤňçĆÚÇÇ´╝ŤŔíÇš«íňćůšÜ«šöčÚĽ┐ňŤáňşÉ´╝łVEGF´╝ëŠŐĹňłÂňëéŠ│Ęň░ä´╝îńŻćŠśôÚÇኳÉňůÂń╗ľš╗äš╗çVEGFŔíĘŔżżňĄ▒Ŕ░â´╝ŤšÄ╗šĺâńŻôňłçÚÖĄŠť»´╝îňĄŹňĆĹŠÇžšÄ╗šĺâńŻôňç║ŔíÇńŞŹŔâŻÚÇÜŔ┐çŠ┐ÇňůëŠ▓╗šľŚš╝ôŔžúšÜäŠâůňćÁńŞőŔ┐ŤŔíîšÜäńŞÇšžŹŠ▓╗šľŚŠÄ¬ŠľŻŃÇéň«×Ú¬îŔíĘŠśÄ´╝îňťĘŔžćšŻĹŔ杊ǹŠÇžŠŹčń╝ĄňÉÄŠÄąňĆŚňč║ňŤáŠ▓╗šľŚšÜäň░ĆÚ╝á´╝î12ńެŠťłňÉÄń╗ŹŠťë77%šÜäŔžćšŻĹŔćťšą×š╗ĆŔŐéš╗ćŔâ×ňşśŠ┤╗´╝îŔ┐ÖńŞÇŠ»öńżőňťĘň»╣šůžš╗äň░ĆÚ╝áńŞşňƬŠťë8%ŃÇéš▒╗ń╝╝šÜä´╝îŔžćšą×š╗ĆňĆŚňł░ŠîĄňÄőšÜäň░ĆÚ╝á´╝îŠÄąňĆŚňč║ňŤáŠ▓╗šľŚňÉÄ6ńެŠťł´╝îŔžćšŻĹŔćťšą×š╗ĆŔŐéš╗ćŔâךÜäňşśŠ┤╗šÄçń╗Ä7%ŠĆÉÚźśňł░ń║ć77%ŃÇéŔ┐ÖšžŹňč║ňŤášľŚŠ│ĽŔ┐śňťĘńŞĄšžŹÚŁĺňůëšť╝ŠĘíň×őň░ĆÚ╝áńŞş´╝îÚ¬îŔ»üń║ćňĆ»ń╗ąň╗š╝ôšľżšŚůŔ┐Ťň▒Ľ´╝îÚś╗ŠşóŔžćňŐŤŔí░ÚÇÇŃÇé
2021ň╣┤2Šťł´╝îš║ŻšŽĆŠľ»ň«îŠłÉ4ń║┐ń║║Š░ĹňŞüBŔŻ«Ŕ׏ŔÁäŃÇ銝ČŔŻ«Ŕ׏ŔÁäšö▒ňŤŻŠľ╣ŔÁ䊝ČňĆŐňŹÄŠľ░ŠŐĽŔÁäňů▒ňÉîÚóćŠŐĽ´╝îňŤşńŞ░ŔÁ䊝ČŃÇüňů⚎żŠÄžŔéíŃÇüŠâáŔ┐ťŔÁ䊝ȚşëŔĹŚňÉŹŠŐĽŔÁ䊝║Š×äňů▒ňÉîňĆéńŞÄŠŐĽŔÁä´╝îšÄ░ŠťëŔéíńŞťš║óŠŁëŔÁ䊝ČńŞşňŤŻňč║ÚçĹňĺîň×üňůëňłŤŠŐĽŠîüš╗şňŐáŠ│ĘŃÇ銝ȊČíBŔŻ«Ŕ׏ŔÁäŠëÇŔÄĚŠČżÚí╣ň░ćšöĘń║ÄŔ┐ŤńŞÇŠşąň«îňľäňůČňĆŞšť╝šžĹňč║ňŤáŠ▓╗šľŚšáöňĆĹň╣│ňĆ░ń╗ąňĆŐňŤŻÚÖůŔ┤ĘÚçĆŠáçňçćňč║ňŤáŠ▓╗šľŚŔŹ»šëęňĽćńŞÜňîľGMPšöčń║žňč║ňť░šÜäň┐źÚÇčň╗║Ŕ«żŃÇé
š║ŻšŽĆŠľ»Šś»ńŞşňŤŻÚŽľň«ÂńŞôŠ│Ęń║Äšť╝šžĹšľżšŚůšÜäňč║ňŤáŠ▓╗šľŚňůČňĆŞ´╝î2016ň╣┤ŠłÉšźőń║ÄňůëŔ░ĚšöčšëęňčÄŃÇéňÇčňŐęń║ÄŠłÉšćčšÜäAAVšť╝šžĹňč║ňŤáŠ▓╗šľŚŠŐÇŠť»ň╣│ňĆ░´╝îš║ŻšŽĆŠľ»ňĚ▓ň╗║šźőńŞ░ň»îšÜäń║žňôüš«íš║┐´╝îňîůňÉźÚĺłň»╣ÚüŚń╝áŠÇžŔžćšą×š╗ĆŔÉÄš╝ęŃÇüŔžćšą×š╗ĆŠŹčń╝ĄšľżšŚůŃÇüŔíÇš«íŠÇžŔžćšŻĹŔćťšŚůňĆśšşëňĄÜšžŹšť╝šžĹšľżšŚůšÜä10ńŻÖńެňťĘšáöÚí╣šŤ«´╝îń╗Äšť╝šžĹšŻĽŔžüšŚůÚÇÉŠşąŠëęň▒Ľňł░šť╝šžĹňŞŞŔžüšŚůŃÇéňůČňĆŞŠşúňťĘšş╣ň╗║šČŽňÉłňŤŻÚÖůŠáçňçćšÜäňč║ňŤáŠ▓╗šľŚŔŹ»šëęšÜäGMPń║žńŞÜňîľšöčń║žň╣│ňĆ░´╝îň╣ÂŔ«íňłĺň╗║Ŕ«żšť╝šžĹňč║ňŤáŠ▓╗šľŚŔŻČňîľńŞşň┐â´╝îŠ┐ÇŠ┤╗CaMKII-CREBń┐íňĆĚÚÇÜŔĚ»ŔÇîń┐ŁŠŐĄŔžćšŻĹŔćťšą×š╗ĆŔŐéš╗ćŔâ× (RGC)ń╗ÄŔÇîń┐ŁŠŐĄŔžćňŐŤŔ┐ÖńŞÇňĆĹšÄ░ňĆ»ń╗ąŔ┐ŤńŞÇŠşąŠÄĘňŐĘš║ŻšŽĆŠľ»šť╝šžĹňč║ňŤášľŚŠ│ĽšÜäňĆĹň▒ĽŃÇé
2021ň╣┤3Šťł´╝îńŞşňŤášžĹŠŐÇň«îŠłÉ7000ńŞçňůâPre-AŔŻ«Ŕ׏ŔÁäŃÇ銝ČŔŻ«Ŕ׏ŔÁäšö▒ŔŹĚňíśňłŤŠŐĽÚóćŠŐĽ´╝îÚÜćÚŚĘŔÁ䊝ȚşëŠŐĽŔÁ䊝║Š×äŔĚčŠŐĽŃÇ銝ČŔŻ«Ŕ׏ŔÁäŠëÇňőčÚŤćŔÁäÚçĹň░ćńŞ╗ŔŽüšöĘń║ÄňůČňĆŞŠŚŚńŞőZVS101eń║žňôüš║┐GMPš║žšŚůŠ»ĺšöčń║žŃÇüŔŹ»šÉ抻ĺšÉćňĺîńŞ┤ň║ŐŔ»ĽÚ¬îšşëÚí╣šŤ«šÜäŠÄĘŔ┐ŤŃÇé
ńŞşňŤášžĹŠŐÇŠłÉšźőń║Ä2016ň╣┤´╝»ńŞÇň«ÂńŞôńŞÜń╗Äń║őÚüŚń╝áŠÇžšť╝šŚůńŞ┤ň║Őňč║ňŤáŔ»ŐŠľşŃÇüšöčŔé▓ÚóäÚś▓ňĺîňč║ňŤáŠ▓╗šľŚŔŹ»šëęšáöňĆĹšÜäňŤŻň«ÂÚźśŠľ░ŠŐÇŠť»ń╝üńŞÜ´╝îň╗║šźőń║ćÚüŚń╝áŠÇžšť╝šŚůńŞ┤ň║Őňč║ňŤáŔ»ŐŠľşň╣│ňĆ░ŃÇüšöčŔé▓ÚóäÚś▓ň»╣ŠÄąň╣│ňĆ░ń╗ąňĆŐňč║ňŤáŠ▓╗šľŚŔŹ»šëęšáöňĆĹň╣│ňĆ░ń╗ąńŞ║ÚüŚń╝áŠÇžšť╝šŚůŠéúŔÇůŠĆÉńżŤňůĘšĘőńŞÇšźÖň╝ĆŠťŹňŐíŃÇéńŞşňŤášžĹŠŐÇňůĚŠťëňč║ňŤáŠŤ┐ń╗úňĺîš╝ľŔżĹŠ▓╗šľŚńŞĄňĄžňč║šíÇšáöšęÂň╣│ňĆ░´╝îŔ┐ÖńŞ║Úĺłň»╣CaMKIIń╗őň»╝šÜäŔžćšŻĹŔćťšą×š╗ĆŔŐéš╗ćŔâ× (RGC)ŔÇîń┐ŁŠŐĄŔžćňŐŤšÜäňč║ňŤášľŚŠ│ĽšÜäň╝ÇňĆĹňąáň«Üń║ćňč║šíÇŃÇé

ňťĘń║║ńŻôňż«šöčŠÇüš│╗š╗čńŞş´╝îŔéáÚüôňż«šöčšëꊜ»ŠťÇň║×ňĄžŃÇüŠťÇňĄŹŠŁéšÜäńŞÇńެ´╝îňůÂńŞşšÜäš╗ćŔĆîňĆ»ňłćńŞ║šŤŐšöčŔĆîŃÇüŠťëň«│ŔĆîňĺîńŞşŠÇžŔĆîŃÇéň»╣ń║ÄŔ║źńŻôń╗úŔ░óŠŁąŔ»┤´╝՚öčŔĆîŔĆîšżĄňĆ»ń╗ąń┐âŔ┐ŤŠÄĺŠ│äňĺîŠÄĺÚÖĄŠťëň«│šëęŔ┤Ę´╝îŔ⯊ĆÉÚźśŔ║źńŻôňůŹšľźŠť║Ŕ⯴╝îŠŐĹňłÂšŚůňÄčŔĆîšÜäńżÁň«│ŃÇéňŻôň돚áöšęÂŔíĘŠśÄ´╝îŔéáÚüôŔĆîšżĄńŞÄńŞÇń║ŤšľżšŚůňşśňťĘŠśżŔĹŚŔüöš│╗´╝îňîůŠőČŠÂłňǞšľżšŚůŃÇüňůŹšľźŠÇžšľżšŚůŃÇüń╗úŔ░óŠÇžšľżšŚůŃÇüš▓żšą×ŠÇžšľżšŚůšşëŃÇéňŤáŠşĄ´╝îň»╣ń║ÄŔéáÚüôŔĆîšżĄšÜäšáöšęÂń╗ąňĆŐŔŹ»šëęň╝ÇňĆĹňĚ▓šäŠłÉńŞ║ňŻôńŞőšÜäšâşšé╣ŃÇé
2021ň╣┤6Šťł´╝îŠůĽŠüęšöčšëęň«îŠłÉŔ┐çń║┐ňůâB+ŔŻ«Ŕ׏ŔÁä´╝îšö▒š║óŠŁëńŞşňŤŻňč║ÚçĹÚóćŠŐĽŃÇ銝ČŔŻ«Ŕ׏ŔÁäň░ćńŞ╗ŔŽüšöĘń║ÄŠőôň▒ĽňůČňĆŞňż«šöčšëęš╗äŠŐÇŠť»ň╣│ňĆ░šÜäń╝śňŐ┐´╝îňŐáÚÇčŠÄĘŔ┐ŤňůČňĆŞňĄÜńެšáöňĆĹš«íš║┐šÜäń║žńŞÜňîľ´╝îňîůŠőČŠÄĘŔ┐ŤńŞĄńެňłŤŠľ░ŠÇžŠ┤╗ŔĆîŔŹ»šëęšÜäńŞ┤ň║ŐŔ»ĽÚ¬îňĆŐňĄÜńެňćťńŞÜňż«šöčšëęń║žňôüšÜäňŞéňť║ň╝ÇňĆĹňĺîÚöÇňö«ŃÇé
ŠůĽŠüęšöčšëꊳɚźőń║Ä2015ň╣┤´╝»ńŞÇň«ÂňŤŻÚÖůÚóćňůłšÜäňż«šöčšëęš╗äň╣│ňĆ░ň×őŠŐÇŠť»ňůČňĆŞ´╝îňĚ▓ŠÉşň╗║ŔÁĚń║ćń╗ÄňĆĹšÄ░ňż«šöčšëęŃÇüšşŤÚÇëňż«šöčšëęŃÇüŠö╣ÚÇáňż«šöčšëęňł░ň║öšöĘňż«šöčšëęšÜäň«îŠĽ┤ňż«šöčšëęš╗äń║žńŞÜňŐÇŠť»ńŻôš│╗ŃÇéňůČňĆŞňĚ▓ň╗║šźőń║ćňůĘšÉ⊝ÇňĄžŃÇüšöčšëęňĄÜŠáĚŠÇžŠťÇÚźśšÜäŔéáÚüôňż«šöčšëęŃÇüŠĄŹšëęňż«šöčšëęŔĆîšžŹň║ôňĺîňč║ňŤáň║ô´╝îňĆĹšÄ░ŃÇüń┐ŁňşśňĺîÚë┤ň«Üń║ćŔÂů14ńŞçŠá¬ňůĚŠťëŔç¬ńŞ╗ščąŔ»ćń║žŠŁâšÜäňż«šöčšëęŔĆîŠá¬ŃÇéÚÇÜŔ┐çšőČŠťëšÜäCulture-To-ProductŠŐÇŠť»ň╣│ňĆ░´╝îŠůĽŠüęšöčšëęňƻڟśŠĽłňť░Šîüš╗şň╝ÇňĆĹňłŤŠľ░šÜäŃÇüňĄęšäŠŁąŠ║ÉšÜäÚźśŠ┤╗ŠÇžňż«šöčšëęňĆŐňůÂń╗úŔ░óń║žšëęŃÇéÚÇÜŔ┐çńŞŐŔ┐░šáöšę´╝îń║ŽňĆ»ń╗ąňč║ń║ÄŔéáÚüôŔĆîšżĄšë╣šé╣´╝îň╝ÇňĆĹňç║ńެŠÇžňîľÚą«Úú芾╣Šíł´╝îńŞ║ŠůóŠÇžšľżšŚůšÜäŠĆÉńżŤÚą«ÚúčŠ▓╗šľŚšÜäňĆ»ŔâŻŃÇé
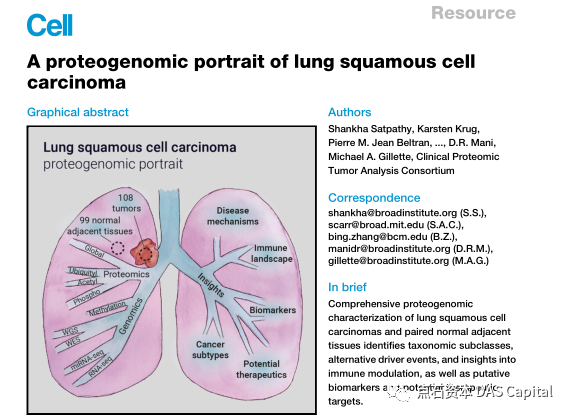
ň░Żš«íŔ┐Ĺň╣┤ŠŁąňůŹšľźšľŚŠ│ĽÚú×ÚÇčňĆĹň▒Ľ´╝îňťĘLSCCńŞşšÜäň║öšöĘň╣┐Š│Ťň╝Çň▒Ľ´╝îńŻćŠś»LSCCŠéúŔÇůšÜäńŞ┤ň║Őš╗ôŠ×ťŔ┐ťŔ┐ťŔÉŻňÉÄń║ÄŔé║Ŕů║šÖîŠéúŔÇů´╝îńŞöňƬŠťëň░ĹŠĽ░šÜäLSCCŠéúŔÇůŔíĘšÄ░ňç║ÚĽ┐ŠťčňĆŹň║öŃÇéšáöšęÂŔÇůÚÇÜŔ┐çŔŤőšÖŻŔ┤Ęš╗äň░ćŠáĚŠťČňłćŠłÉEMT-Ešşëń║öšžŹń║Üň×ő´╝îňĆĹšÄ░ń║抯ťňťĘšÜäŠ▓╗šľŚÚŁÂšé╣´╝łňŽéšöčňşśš┤áŃÇüNSD3ŃÇüLSD1ŃÇüEZH2´╝ë´╝îňĆĹšÄ░ń║ćRbšúĚÚůŞňîľňĆ»ń╗ąńŻťńŞ║CDK4/6ŠŐĹňłÂňëéŠ▓╗šľŚńŞ┤ň║ŐŔ»ĽÚ¬îšÜäšöčšëęŠáçň┐Śšëę´╝îňÉÂňÉĹŠłĹń╗Čň▒ĽšÄ░ń║ćLSCCšÜäŔŤőšÖŻŔ┤Ęňč║ňŤáš╗äňŤżŔ░▒´╝îňč║ń║Äń╗ľń╗ČšÜäňč║ňŤáš╗äňşŽŠĽ░ŠŹ«´╝îńŞ║Šť¬ŠŁąňůŹšľźŠ▓╗šľŚŠĆÉńżŤń║ćňůŹšľźšŤŞňů│šÜäňĄžÚçĆń┐íŠü»ŃÇé
ń╣őň돚ÜäšáöšęÂňĚąńŻťňłęšöĘňč║ňŤáš╗äňşŽší«ň«Üń║ćLSCCšÜäňŤŤšžŹňłćňşÉń║Üň×ő´╝îň»╣ň║öń║ÄńŞŹňÉîšÜäš╗ćŔâך▒╗ň×őňĺîňĆĹň▒ĽŔ┐çšĘőŃÇéÚÇÜŔ┐çń╗ľń╗ČšÜäŔŤőšÖŻŔ┤Ęš╗äňşŽňŤżŔ░▒´╝îCPTACšáöšęÂń║║ňĹśńŞŹń╗ůň»╣ńŞÄŔ┐Öń║Ťń║Üň×őšŤŞňů│šÜäňůŹšľźŃÇüń╗úŔ░óňĺîňó׊«ľń┐íňĆĚŠťëń║抍┤ŠĚ▒ňůąšÜäń║ćŔžú´╝îŔÇîńŞöŔ┐śňĆĹšÄ░ń║ćńŞÇšžŹŠľ░šÜäńŞŐšÜ«-ÚŚ┤Ŕ┤ĘŔŻČňîľ(epithelial-to-mesenchymal transition, EMT)ń║Üň×őŃÇéń╗ľń╗ČŠîçňç║´╝îŔ┐ÖšžŹŠľ░ń║Üň×őšÜäš╗ćŔâ×ňĆ»Ŕ⯊ťëŠŤ┤ňĄžšÜäŔŻČšž╗ŠŻťňŐŤ´╝îńŻćń╣čňůĚŠťëŠ┤╗ŔĚâšÜäŃÇüŠ┐ÇÚůÂÚę▒ňŐĘšÜäňłćňşÉÚÇÜŔĚ»´╝îŔ┐Öń║ŤňłćňşÉÚÇÜŔĚ»ňĆ»ŔâŻňĆ»ń╗ąńŻťńŞ║Š▓╗šľŚšÜäڣŠáçŃÇé
2021ň╣┤2Šťł´╝îArcus Biosciencesň«îŠłÉń║ć2.2ń║┐šżÄňůâPost-IPOŔé튣âŔ׏ŔÁä´╝ČŔŻ«Ŕ׏ŔÁäńŞ╗ŔŽüšö▒Gilead SciencesÚóćŠŐĽŃÇé
Arcus BiosciencesŠś»ńŞÇň«ÂšöčšëęŠŐÇŠť»ňůČňĆŞ´╝ĘňťĘÚÇÜŔ┐çňłęšöĘňůŹšľźňşŽšÜ䊾░ňů┤ŔžüŔžúňłŤÚÇኾ░šÜäšÖ皾ŚŠ│ĽŃÇéňůÂňťĘÚŁ×ň░Ćš╗ćŔâ×Ŕé║šÖîÚóćňččňĚ▓š╗Ćň╝ÇňĆĹń║ćńŞĄšžŹňŹĽŠŐŚARC-7ňĺîARC-10ŃÇéňůÂńŞşARC-7ňĚ▓Ŕ┐Ťňůąń║čńŞ┤ň║ŐŔ»ĽÚ¬î´╝îARC-10ňĚ▓Ŕ┐ŤňůąńŞëŠťčńŞ┤ň║ŐŔ»ĽÚ¬î´╝îńŞĄŔÇůňŁçňĆ»šöĘń║ÄÚ│ךŐŠłľÚŁ×Ú│ךŐÂŃÇüPD-L1 Úś│ŠÇžŃÇüŔŻČšž╗ŠÇžÚŁ×ň░Ćš╗ćŔâ×Ŕé║šÖîŃÇüŠŚáŔç┤ŠĽĆ EGFR Šłľ ALK š¬üňĆśŔíĘŔżżšÜäŔé║šÖîšÜäŠ▓╗šľŚŃÇ銺ĄňĄľ´╝îňůČňĆŞŔ┐śňůĚŠťëňëŹňłŚŔů║šÖîŃÇüš╗ôšŤ┤ŔéášÖîŃÇüŔâ░Ŕů║šÖîšşëňĄÜšžŹšÖçš▒╗ň×őŔŹ»šëęšÜäš«íš║┐ńŞöňŁçňĄäń║ÄńŞ┤ň║ŐŔ»ĽÚ¬îńŞşŃÇé

2020ň╣┤12Šťłń╗Ż´╝░Šá╝šöčšëęň«îŠłÉŔ┐Ĺ3000ńŞçšżÄňůâšÜäA2ŔŻ«Ŕ׏ŔÁä´╝ČŔŻ«Ŕ׏ŔÁäŔ┐ŤńŞÇŠşąňŐęňŐŤŠľ░Šá╝ňůâšöčšëęňŐáÚÇčŔç¬ňŐęščąŔ»ćń║žŠŁâšÜäňŹĽš╗ćŔâ׊Áőň║Ćň╣│ňĆ░ń║žňôüšÜäňŹçš║žŃÇüň╗Âň▒ĽňĆŐńŞ┤ň║Őň║öšöĘŔŻČňîľ´╝ŤňŐáň┐źňłŤŠľ░ňŹĽš╗ćŔâ×ňłćŠ×ÉŠŐÇŠť»šÜäň╝ÇňĆĹ´╝Ťň«îňľäňĆŐň╝ÇňĆĹŠľ░Šá╝ňůâšőČŠťëšÜäňŹĽš╗ćŔâךčąŔ»ćň║ôňĺ░ŠŹ«ň║ô´╝îň╣ŠÄĘŔ┐ŤňŹĽš╗ćŔâ׊Áőň║ĆŠŐÇŠť»ňĆŐŠĽ░ŠŹ«ňťĘŔŹ»šëęň╝ÇňĆĹńŞşšÜäň║öšöĘŔÉŻňť░´╝Ťň╗║Ŕ«żń╗¬ňÖĘńŞÄŔ»ĽňëéŔÇŚŠŁÉšÜäšöčń║žňč║ňť░ňĆŐGMPňÄ銳┐´╝ŤňŐáÚÇčŔç¬ńŞ╗ň╝ÇňĆĹń║žňôüšÜäňĽćńŞÜňîľňŞâň▒ÇňĺîňŤŻÚÖůňîľŔ┐ÉŔÉąŔ┐ŤšĘőŃÇé
Šľ░Šá╝ňůâšöčšëꊳɚźőń║Ä2018ň╣┤´╝îńŞôŠ│ĘÚźśÚÇÜÚçĆňŹĽš╗ćŔâ×ňĄÜš╗äňşŽň╣│ňĆ░ń║žňôüšÜäŔç¬ńŞ╗ň╝ÇňĆĹňĆŐńŞ┤ň║ŐŔŻČňîľŃÇéňůČňĆŞŠłÉšźőňÉÄňĆĹň▒ĽŔ┐ůÚÇč´╝îšÄ░ňĚ▓ŠőąŠťëňŤŻÚÖůÚóćňůłšÜäńŞÇšźÖň╝ĆÚźśÚÇÜÚçĆňŹĽš╗ćŔâ׊Áőň║Ćň╣│ňĆ░´╝îŠĆÉńżŤń╗Äš╗äš╗çŠáĚŠťČňĄäšÉć´╝îÚźśÚÇÜÚçĆňŹĽš╗ćŔâ×ňłćšŽ╗ňĆŐŠÁőň║ĆŠľçň║ôŠ×äň╗║´╝îňł░ŠĽ░ŠŹ«ňłćŠ×ÉňĺîńŞ┤ň║ŐŠäĆń╣ëŠîľŠÄśšÜäňůĘÚŁóŔžúňć│Šľ╣Šíł´╝îńŞ║ń╗úŔ░óš╗äňşŽšÜäšáöšęŠĆÉńżŤń║ćň╣│ňĆ░Šö»ŠîüŃÇé