š┐╗Ŕ»Ĺ | ňŐáńŞÇ
Ŕ┤úš╝ľ | YYY ÚúÄňŐĘňşÉ
ŠťČŠťčCellňĆĹŔíĘ3š»çPreviewsŃÇü1š»çReviewŃÇü1š»çTheoryŃÇü1š»çResourceňĺî13š»çArticles´╝îňůÂńŞş8š»çńŞ║Šľ░ňćᚍŞňů│Šľçšźá´╝îŠĆÉňĆŐSARS-CoV-2ňĆśň╝éńŻô501Y.V2ŃÇüB.1.351ňĺîP.1ňşśňťĘňůŹšľźÚÇâÚÇŞšÄ░Ŕ▒í´╝îňĆ»ŔžüšžĹňşŽšĽîńŞ║Šö╗ňůőŠľ░ňćáń╗ŹÚťÇńŻťňç║ńŞŹŠçłňŐ¬ňŐŤŃÇ銝ȊťčCellň░üÚŁóŠľçšźáń╗Äš▓żňçćňî╗šľŚšÜäŔžĺň║Ž´╝îňŤ┤š╗Ľń║║ńŻôŔéáÚüôŔĆîšżĄň▒Ľň╝ÇňĄÜš╗äňşŽšáöšę´╝îŠĆÉňç║ŔéáÚüôňż«šöčšëęňşśňťĘńެńŻôšë╣ň╝éŠÇžŃÇéňĆŽňĄľ´╝îŔ┐ÉšöĘŔé┐šśĄŔŻČňŻĽš╗äÚóäŠÁőŔé┐šśĄŠ▓╗šľŚšÜäňĆŹň║ö´╝îńŞ║Šľ░ŔŹ»ńŞ┤ň║ŐŔ»ĽÚ¬îŠĆÉńżŤńż┐ňłę´╝îńŞ║š▓żňçćŔé┐šśĄňşŽšÜäňĆĹň▒ĽŠĆÉńżŤšÉćŔ«║Šö»ŠîüŃÇéŔé┐šśĄňůŹšľźÚÇâÚÇŞńŞÄŔé┐šśĄŔŻČšž╗šÜ䊝║ňłÂŠÄóš┤ó´╝îńŞ║š╗ćŔâ׊▓╗šľŚŔŹ»šëęšÜäň╝ÇňĆĹŠĆÉńżŤŠťëňŐŤńżŁŠŹ«ŃÇ銝ȊťčCellŔ┐śń╗őš╗Źń║ćňč║ňŤáš╝ľŔżĹŠŐÇŠť»ň║öšöĘń║ÄŔŻČňŻĽŔ░âŠÄžšÜ䊾░Šľ╣Š│ĽňĆŐŔŻČň║žňşÉňŻĺňĚóšÜ䊝║ňłÂ´╝îňŐęňŐŤCRISPRšŤŞňů│Ŕ폚öčŠŐÇŠť»šÜäň╝ÇňĆĹňłęšöĘŃÇé

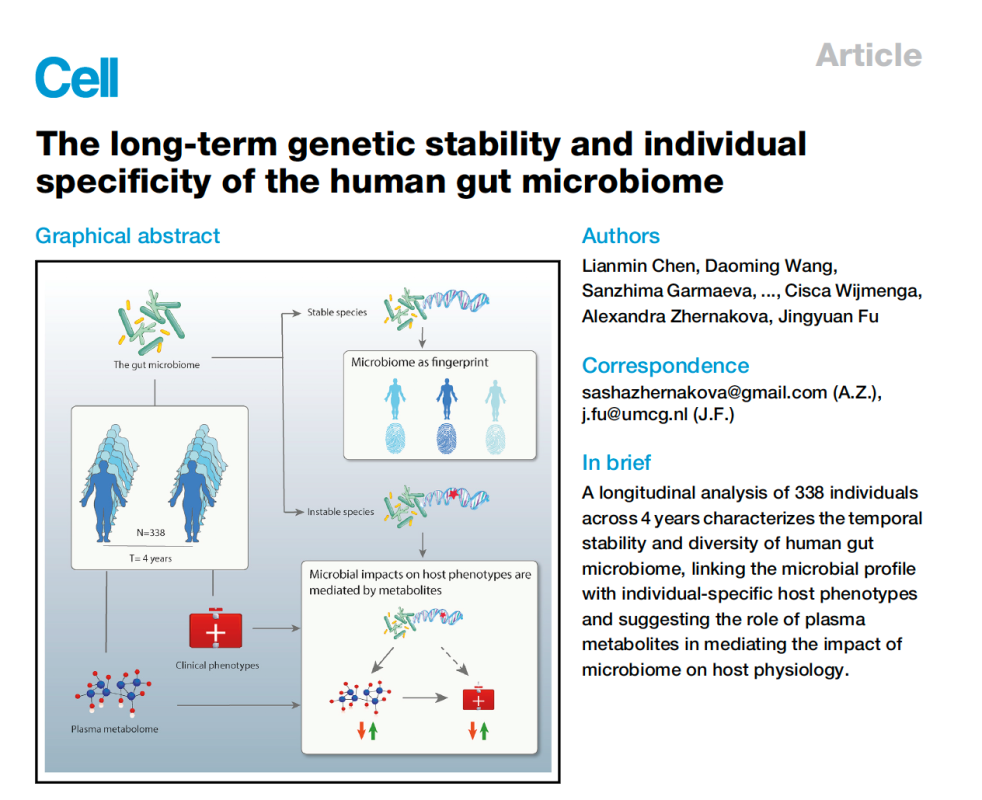
ŠťČš»çńŞ║ŔŹĚňů░Šá╝šŻŚň«üŠá╣ňĄžňşŽňî╗ňşŽńŞşň┐âňéůÚŁÖŔ┐ť´╝łJingyuan Fu´╝ëňŤóÚśčňĆĹŔíĘšÜäArticleŠľçšźá´╝ȊťčcellšÜäň░üÚŁóŠľçšźáŃÇéňč║ń║ÄLifeLines-DEEPÚśčňłŚ´╝îšáöšęÂŔÇůňŤŤň╣┤ňëŹňÉÄňłćňłźŔÄĚňżŚ338ňÉŹňĆŚŔ»ĽŔÇůšÜäŔíĘň×őš╗äŃÇüŔíÇŠÂ▓ń╗úŔ░óš╗äŃÇüŔéáÚüôŔĆîšżĄň«Ćňč║ňŤáš╗äšşëňĄÜš╗äňşŽŠĽ░ŠŹ«Ŕ┐ŤŔíîňłćŠ×ÉŃÇéń╗ľń╗ČňĆĹšÄ░ŔéáÚüôŔĆîšżĄňşśňťĘň«┐ńŞ╗šë╣ň╝éŠÇž´╝îń╗ąŠşĄň╝ÇňĆĹń║ćÚźśš▓żň║ŽÔÇťňż«šöčšëęŠîçš║╣ÔÇŁš«ŚŠ│Ľ´╝îń╗ąŔéáÚüôŔĆîšżĄšÜäÚüŚń╝áŠ×䊳ɊŁąňçćší«ňî║ňłćň«┐ńŞ╗´╝îš▓żší«šĘőň║ŽÚźśŔżż85-95%ŃÇéń╗ľń╗ČňłćŠ×Éš╗ćŔĆîšëęšžŹńŞ░ň║ŽŃÇüń╗úŔ░óÚÇöňżäŃÇüš╗ôŠ×äňĆśň╝éňĺîŔĆîŠá¬ŠŤ┐ŠŹóšÜäňĆśňîľ´╝îňĆĹšÄ░ňůÂńŞş190ńެňĆśňîľńŞÄň«┐ńŞ╗ŔíĘň×őšŤŞňů│Ŕüö´╝î519ńެňĆśňîľńŞÄŔíÇŠÁćń╗úŔ░óšëęŠÁôň║ŽšŤŞňů│ŔüöŃÇéŔ┐Öń║ŤŔüöš│╗ńŞ╗ŔŽüÚŤćńŞşń║Äň┐âŔäĆń╗úŔ░óšë╣ňżüŃÇüŔíÇŠÁćš╗┤šöčš┤áBňĺîň░┐Š»ĺšŚçŃÇéŔ┐Öń║ŤšÄ░Ŕ▒íŔíĘŠśÄ´╝îŔéáÚüôňż«šöčšëęšżĄňĆ»ŔâŻÚÇÜŔ┐çń╗úŔ░óń║žšëęňŻ▒ňôŹň┐âŔäĆňüąň║ĚŃÇé´╝łŠĹśŔŽü´╝ë(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.024)
ŠŐĽŔÁäÚó䊝č´╝Üň«Ćňč║ňŤáš╗䊯ťňŐŤňĚĘňĄž´╝îňĄÜš╗äňşŽŠłÉńŞ║ňĆĹň▒ĽŔÂőňŐ┐ň«Ćňč║ňŤáš╗ä´╝îń╣čšž░ňż«šöčšëęšÄ»ňóâňč║ňŤáš╗äŃÇéň«Ćňč║ňŤáš╗äňĆŐňĄÜš╗äňşŽŠĽ┤ňÉłňłćŠ×ÉÚÜÂň▒×ń║Äš▓żňçćňî╗šľŚÚóćňččŃÇéÚÜĆšŁÇš╗äňşŽŠľ░ŠŐÇŠť»šÜäŠÂîšÄ░ňĺîÚźśÚÇÜÚçĆŠ░┤ň╣│šÜäňĆĹň▒Ľ´╝îň»╣ňĄÜš╗äňşŽŠĽ░ŠŹ«šÜ䊼┤ňÉłňłćŠ×ÉŠłÉńŞ║šžĹňşŽň«ÂŠÄóš┤óšöčňĹŻňąąšžśšÜ䊾░Šľ╣ňÉĹŃÇéšľźŠâůŠŚÂń╗úń╣őńŞő´╝ůňÄčňż«šöčšëęšÜäň«Ćňč║ňŤáš╗äŠúÇŠÁőÚí║ň║öń║ćńŞ┤ň║Őň»╣Ú珚ŚçŠäčŠčôšÜäŔ┐źňłçڝNJ▒éŃÇéń║║ńŻôŔéáÚüôňż«šöčšëęňč║ňŤáš╗äŔóźšž░ńŞ║ÔÇťń║║š▒╗šÜäšČČń║îňč║ňŤáš╗äÔÇŁ´╝îň»╣ń║║ńŻôňüąň║ĚŠťëÚçŹŔŽüňŻ▒ňôŹŃÇéň«Ćňč║ňŤáš╗äšáöšęÂŔ┐ŤňůąňĄÜš╗äňşŽŠŚÂń╗ú´╝îŔéáÚüôňż«šöčšëęš╗äňĺîń╗úŔ░óš╗äŔüöňÉłňłćŠ×ÉňŤ┤š╗Ľń╗úŔ░óŠÇžšľżšŚůŃÇüšą×š╗ĆÚÇÇŔíîŠÇžšľżšŚůŃÇüŠüŠǞŔé┐šśĄšşëšľżšŚůň▒Ľň╝Ç´╝îňůőŠťŹňŹĽńŞÇš╗äňşŽšáöšęšÜäň▒ÇÚÖÉŠÇž´╝îńŞ║ŠÄóš┤óšľżšŚůšÜ䊳ÉňŤáňĺîŠ▓╗šľŚŠĆÉńżŤŠľ░šÜäŠÇŁŔĚ»´╝îńŞ║ň«×šÄ░šľżšŚůŠŚęšşŤŠĆÉńżŤŠľ░šÜ䊾╣Š│ĽŃÇ銝ȊťčCellŠĆÉňç║Šľ░ÚóľšÜäÔÇťňż«šöčšëęŠîçš║╣ÔÇŁš«ŚŠ│Ľ´╝îňĆ»ŔâŻňťĘš▓żňçćŔ»ŐšľŚŃÇüŠ│Ľňî╗Úë┤ň«ÜŃÇüŠáĚŠťČŠ║»Š║ÉšşëÚóćňččňůĚŠťëÚçŹŔŽüň║öšöĘń╗ĚňÇ╝ŃÇé
ŠáŞň┐âŠŐÇŠť»šŚŤšé╣´╝ÜňĄÜš╗äňşŽŠĽ░ŠŹ«ň║öň╗║šźőŠťëŠĚ▒ň║Žń╗ĚňÇ╝šÜäŔĚĘš╗äňşŽŠĽ░ŠŹ«Ŕüöš│╗
ňťĘš╗äňşŽŠŐÇŠť»ńŞŹŠľşňĆĹň▒ĽŃÇüŠÁőň║ĆŠłÉŠťČńŞŹŠľşÚÖŹńŻÄšÜäňŻôńŞő´╝îňůĘňč║ňŤáš╗äŃÇüň«Ćňč║ňŤáš╗äŃÇüń╗úŔ░óš╗äŃÇüŔíĘŔžéÚüŚń╝áš╗äšşëňĄÜš╗äňşŽŠĽ░ŠŹ«ń╗ąšłćňĆĹň╝Ćňó×ÚĽ┐ŃÇéňĄÜš╗äňşŽŠĽ┤ňÉłňłćŠ×ÉšÜäÚÜżšé╣ňĚ▓ńŞŹňťĘń║ÄňÉäš▒╗ŠĽ░ŠŹ«šÜäŔÄĚňżŚ´╝îŔÇîňťĘń║Äň╗║šźőŠťëŠĚ▒ň║Žń╗ĚňÇ╝šÜäŔĚĘš╗äňşŽŠĽ░ŠŹ«Ŕüöš│╗´╝îňîůŠőČň»╣ŠĽ░ŠŹ«Ŕ┐ŤŔíîŠĚ▒ň║ŽŠĽ┤ňÉłňłćŠ×ÉŃÇüň╝ÇňĆĹň╣Âń╝śňĚ▒ň║ŽŠîľŠÄśń┐íŠü»šÜäš«ŚŠ│ĽŃÇüŠĆÉÚźśňłćŠ×Éš╗ôŠ×ťšÜ䊼ƊäčŠÇžńŞÄňçćší«ŠÇžšşëňůĚńŻôŠëőŠ«ÁŃÇé
ňŤŻňćůŠŐĽŔÁäŠíłńżő´╝Üňż«Ŕ┐ťňč║ňŤáŔÄĚŔůżŔ«»ÚóćŠŐĽ2ń║┐ňůâCŔŻ«Ŕ׏ŔÁä
2021ň╣┤2Šťł4ŠŚą´╝îŠäčŠčôÚóćňččš▓żňçćňî╗ňşŽń╝üńŞÜň╣┐ňĚ×ňż«Ŕ┐ťňč║ňŤášžĹŠŐÇŠťëÚÖÉňůČňĆŞ´╝łń╗ąńŞőš«Çšž░ÔÇťňż«Ŕ┐ťňč║ňŤáÔÇŁ´╝ëň«úňŞâň«îŠłÉ2ń║┐ňůâCŔŻ«Ŕ׏ŔÁäŃÇ銝ČŔŻ«Ŕ׏ŔÁäšö▒ŔůżŔ«»ÚóćŠŐĽ´╝îńŞşÚçĹŔÁ䊝ČŃÇüÚ╝ÄŠÖľŠŐĽŔÁäŃÇüňŤŻšžĹňśëňĺîšşëšÄ░ŠťëŔéíńŞťňů▒ňÉîňĆéńŞÄŃÇéňůČň╝ÇŔÁ䊾֊śżšĄ║´╝îňż«Ŕ┐ťňč║ňŤáńŞ╗ŔŽüńŞôŠ│Ęń║Äňč║ňŤáŠŐÇŠť»ňłŤŠľ░ńŞÄŠäčŠčôš▓żňçćňî╗šľŚ´╝«ň돊őąŠťëńŞĄňĄžŠáŞň┐âŠŐÇŠť»ň╣│ňĆ░´╝îňîůŠőČň«Ćňč║ňŤáš╗äŠÁőň║Ć´╝łmNGS´╝ëŠŐÇŠť»ńŞÄňč║ňŤáš╝ľŔżĹňĚąňůĚ´╝łCRISPR-Cas12/13´╝ëň┐źÚÇčŔ»ŐŠľşŠŐÇŠť»ŃÇéÚçĹňîÖňč║ňŤáCŔŻ«Ŕ׏ŔÁä2.3ń║┐ňůâń║║Š░ĹňŞü2020ň╣┤11Šťł2ŠŚą´╝îÚçĹňîÖňč║ňŤáň«îŠłÉ2.3ń║┐ňůâń║║Š░ĹňŞüšÜäCŔŻ«Ŕ׏ŔÁä´╝îŔ»ąŔŻ«ŠŐĽŔÁ䊾╣ńŞ║ňŹÄšŤľŔÁ䊝ČŃÇüŠŁĆŠ│ŻŔÁ䊝ČňĺîňůâšöčňłŤŠŐĽ´╝îAŔŻ«ŠŐĽŔÁäń║║ňÉŤŔüöŔÁ䊝ȚČČńŞëŠČíŔ┐ŻňŐáŠŐĽŔÁäŃÇéÚçĹňîÖňč║ňŤáŠĚ▒ŔÇĽŠäčŠčôŠÇžšľżšŚůňč║ňŤáŠúÇŠÁő´╝îÚŁóňÉĹňĹ╝ňÉŞŃÇüŔíÇŠÂ▓ŃÇüŠÂłňîľŃÇüŠäčŠčôšşëňşŽšžĹ´╝îň«ÜňłÂňĚ«ň╝éňîľšÜäň«Ćňč║ňŤáš╗äŠúÇŠÁőŠÁüšĘőňĺîš«ŚŠ│Ľ´╝îňč║ń║ÄńŞëń╗úš║│š▒│ňşöŠÁőň║ĆŠÄĘňç║ňłćňşÉŠúÇŠÁőń║žňôü´╝îŠĆÉňŹçšŚůňÄčňż«šöčšëęň┐źÚÇčŠúÇňç║Š░┤ň╣│´╝îšČŽňÉłš▓żňçćňî╗šľŚňťĘŠäčŠčôŠÇžšľżšŚůńŞşšÜäňĆĹň▒ĽŔÂőňŐ┐ŃÇé
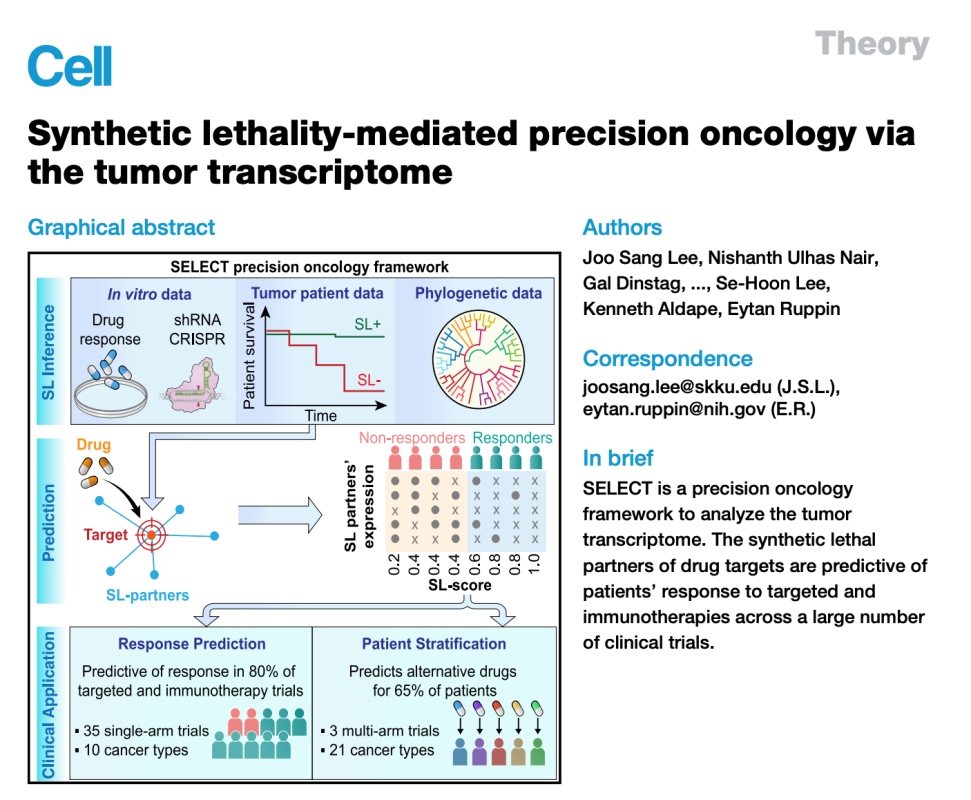
ŠťČš»çńŞ║šżÄňŤŻÚęČÚçîňů░ňĚ×Ŕ┤Łňí׊ľ»ŔżżňŞéňŤŻň«ÂšÖçšáöšęŠëÇšÜäEytan RuppinňŤóÚśčňĆĹŔíĘšÜäTheoryŠľçšźáŃÇéš▓żší«Ŕé┐šśĄňşŽňĚ▓ňĆľňżŚń║ćÚçŹňĄžŔ┐Ťň▒Ľ´╝îńŞ╗ŔŽüŠś»ÚŁÂňÉĹšÖçÚę▒ňŐĘňč║ňŤášÜäňĆ»ŠôŹńŻťš¬üňĆśŃÇéńŞ║ń║ćŔÄĚňżŚŠŤ┤ňĄÜšÜäŠ▓╗šľŚŠť║ń╝Ü´╝ÇŔ┐ĹšÜäšáöšęÂň╝ÇňžőŠÄóš┤óŔé┐šśĄŔŻČňŻĽš╗äňťĘŠîçň»╝ŠéúŔÇůŠ▓╗šľŚńŞşšÜäńŻťšöĘŃÇ銝Ț»çŠľçšî«ń╗őš╗Źń║ćńŞÇšžŹš▓żší«Ŕé┐šśĄňşŽŠíćŠ×ÂSELECT´╝łsynthetic lethality and rescue-mediated precision oncology via the transcriptome´╝ë´╝îÚÇÜŔ┐çŔé┐šśĄŔŻČňŻĽš╗äňĆŐňč║ňŤášŤŞń║ĺńŻťšöĘŠŁąÚóäŠÁőŠéúŔÇůň»╣Ŕé┐šśĄŠ▓╗šľŚšÜäňĆŹň║öŃÇéSELECTňťĘ35Úí╣ňĚ▓ňĆĹŔíĘšÜäŠÂÁšŤľ10šžŹńŞŹňÉîšÖçš▒╗ň×őšÜäÚŁÂňÉĹňĺîňůŹšľźŠ▓╗šľŚńŞ┤ň║ŐŔ»ĽÚ¬îšÜäňč║šíÇńŞŐŔ┐ŤŔíîŠÁőŔ»Ľ´╝îŔâŻňĄčÚóäŠÁő80%ńŞ┤ň║ŐŔ»ĽÚ¬îšÜäš╗ôŠ×ťŃÇéŔ»ąÚóäŠÁőŠľ╣Š│Ľňĺîń╗úšáüňůČň╝ÇšöĘń║ÄňşŽŠť»šöĘÚÇö´╝îńŞ║Šť¬ŠŁąšÜäň돚×╗ŠÇžńŞ┤ň║ŐšáöšęÂňąáň«Üń║ćňč║šíÇŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.030)
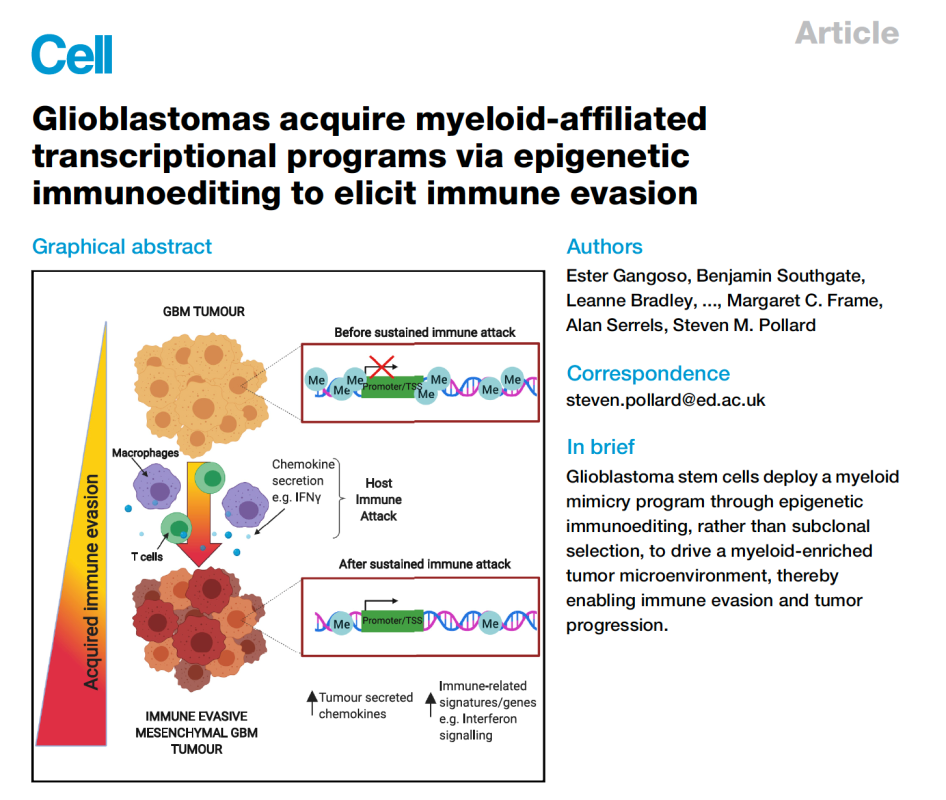
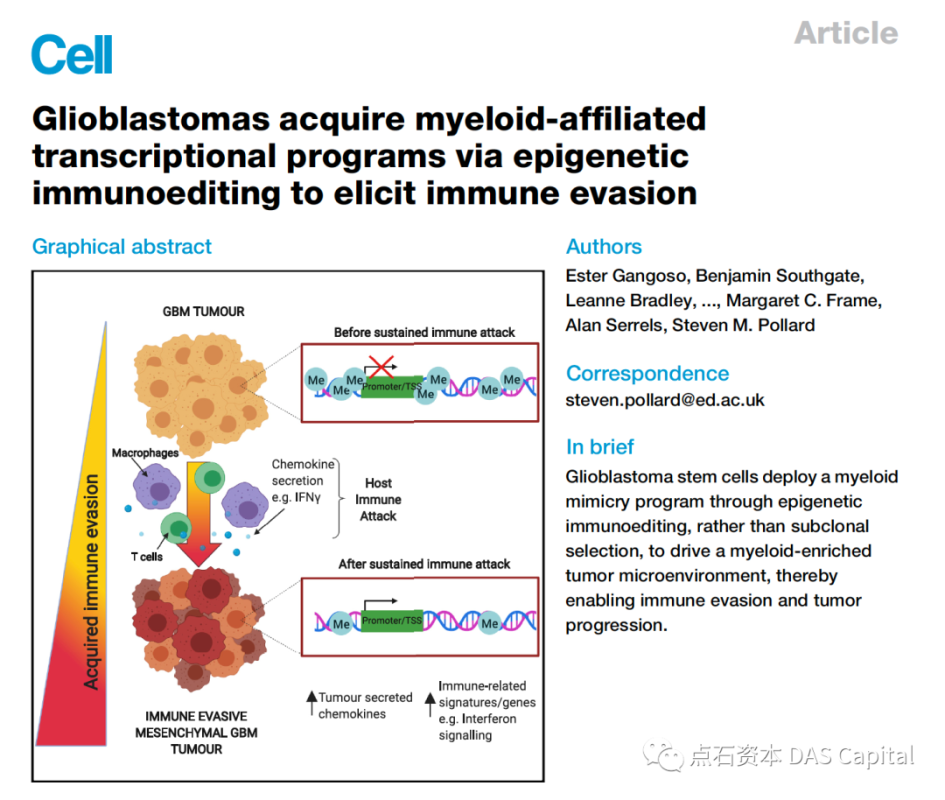
ŠťČš»çńŞ║Ŕő▒ňŤŻšł▒ńŞüňáíňĄžňşŽSteven M. PollardňŤóÚśčňĆĹŔíĘšÜäArticleŠľçšźáŃÇéňĄÜňŻóŠÇžŔâÂŔ┤ĘŠ»Źš╗ćŔâךśĄ´╝łGlioblastoma multiforme´╝îGBM´╝늜»ńŞÇšžŹńżÁŔóşŠÇžŔäĹŔé┐šśĄ´╝«ňëŹňĚ▓ŠťëňůŹšľźŠ▓╗šľŚŠľ╣Š│ĽňťĘŔ┐ÖńެÚóćňččšÜäň║öšöĘŔ┐śŠ▓íŔÄĚňżŚŠłÉňŐčŃÇéšáöšęÂŔÇůň░ćGBMň╣▓š╗ćŔâ×´╝łGSCs´╝ëšž╗ŠĄŹňł░ňůĚŠťëňůŹšľźŠ┤╗ŠÇžšÜäň«┐ńŞ╗ńŻôňćů´╝îňĆĹšÄ░ń║ćńŞÇšžŹŔÄĚňżŚŠÇžšÜäňůŹšľźÚÇâÚü┐Šť║ňłÂÔÇöÔÇöGSCsÚÇÜŔ┐çňó×ň╝║ňůŹšľźŠŐĹňłÂŔé┐šśĄňż«šÄ»ňó⊣ąÚÇâÚü┐ňůŹšľźŠŞůÚÖĄŃÇéń╗ÄŠť║ňłÂńŞŐŔ«▓´╝îŔ┐ÖńŞŹŠś»šö▒Ŕé┐šśĄń║ÜňůőÚÜćšÜäÚüŚń╝áÚÇëŠőęň╝ĽŔÁĚšÜä´╝îŔÇ»šö▒ŔíĘŔžéÚüŚń╝ášÜäňůŹšľźš╝ľŔżĹň╝ĽŔÁĚšÜäŃÇéňťĘňůŹšľźŠö╗ňç╗ňÉÄ´╝îGSCsńŞşšÜäšĘ│ň«ÜŔŻČňŻĽňĺîŔíĘŔžéÚüŚń╝áňĆśňîľňżŚňł░ňŐáň╝║ŃÇéŔ┐Öń║ŤňĆśňîľňÉ»ňŐĘń║ćńŞÇńެńŞÄÚ¬ĘÚźôšŤŞňů│šÜäŔŻČňŻĽšĘőň║Ć´╝îň»╝Ŕç┤Ŕé┐šśĄšŤŞňů│ňĚĘňÖČš╗ćŔâךÜäňó×ňŐáŃÇ銺ĄňĄľ´╝îń╗ľń╗ČňťĘń║║ÚŚ┤ňůůŔ┤Ęń║Üň×őGSCsńŞşňĆĹšÄ░ń║暍Şń╝╝šÜäŔíĘŔžéÚüŚń╝áňĺîŔŻČňŻĽšë╣ňżüŃÇéš╗ôŔ«║Šś»´╝îŔíĘŔžéÚüŚń╝áňůŹšľźš╝ľŔżĹňĆ»ŔâŻÚÇÜŔ┐çÚçŹňíĹŔé┐šśĄňůŹšľźňż«šÄ»ňóâ´╝îňťĘŠťÇňůĚńżÁŔóşŠÇžšÜäÚŚ┤ňůůŔ┤ĘGBMń║Üň×őńŞşÚę▒ňŐĘŔÄĚňżŚŠÇžňůŹšľźÚÇâÚü┐šĘőň║ĆŃÇé´╝łŠĹśŔŽü´╝ë(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.023)
ŠŐĽŔÁäÚó䊝č´╝ÜŔé┐šśĄňůŹšľźňëŹÚÇöňů늜Ĵ╝îŠö╗ňůőGBMÚüôÚś╗ńŞöÚĽ┐
Ŕé┐šśĄňůŹšľźŠ▓╗šľŚšÜäŔ┐ůÚÇčňĆĹň▒Ľš╗ÖŠŚáŠĽ░šÖ皌ůń║║ňŞŽŠŁąń║ćšöčňĹŻšÜäňŞîŠťŤ´╝îňťĘŔ┐çňÄ╗30ńŻÖň╣┤šÜäňĆĹň▒ĽňÄćšĘőńŞş´╝îš╗ćŔâ׊▓╗šľŚń║žňôüšÖżŔŐ▒ÚŻÉŠöżŃÇéńŻćňĄÜňŻóŠÇžŔâÂŔ┤ĘŠ»Źš╗ćŔâךśĄ´╝łGBM´╝ëńŻťńŞ║ŠťÇňŞŞŔžüšÜäŔäĹŔé┐šśĄ´╝îńżÁŔóşŠÇžň╝║´╝îŔç│ń╗ŐŠ▓튝늝늼łšÜäŔé┐šśĄňůŹšľźŠ▓╗šľŚŠľ╣Š│Ľ´╝îÚóäňÉÄŠ×üňĚ«´╝îń║öň╣┤šöčňşśšÄçńŻÄń║Ä5%ŃÇéňťĘňůŹšľźŠ▓╗šľŚšë╣ň╝éŠÇžŔ»ćňłźňĺÇń╝ĄšÜäŔ┐çšĘőńŞş´╝îGBMŔâŻŔíĘŔżżńŞÇš│╗ňłŚňůŹšľźń┐íňĆĚŔ┤čŔ░âŠÄžňłćňşÉ´╝îňŞ«ňŐęŔé┐šśĄň«îŠłÉňůŹšľźÚÇâÚÇŞ´╝îń╗Őň╣┤2Šťł´╝îÚ║╗šťüŠÇ╗ňî╗ÚÖóńŞ╣š║│Š│Ľń╝»šÖçšáöšęŠëÇŃÇüÚ║╗šťüšÉćňĚąňşŽÚÖóňĺîňôłńŻŤňĄžňşŽňŹÜňĄžšáöšęŠëÇšÜäšžĹňşŽň«ÂňťĘCellŠŐąÚüôń║ćńŞÇńެňĆ»Ŕ⯚öĘń║ÄŠÁŞŠÂŽŠÇžŔâÂŔ┤ĘšśĄšÜäňůŹšľźŠ▓╗šľŚŠľ░ڣšé╣´╝îń╗ľń╗ČňĆĹšÄ░CD161ňĆŚńŻôšÜäŠ┐ÇŠ┤╗ń╝ÜŠŐĹňłÂTš╗ćŔâ×ň»╣Ŕé┐šśĄš╗ćŔâךÜäňĆŹň║öŃÇ銝ȊťčCellŠĆÉňç║ŔíĘŔžéÚüŚń╝áňůŹšľźš╝ľŔżĹń╣čňĆéńŞÄŔé┐šśĄňż«šÄ»ňóâÚçŹňíĹňĺîňůŹšľźÚÇâÚÇŞŔ┐çšĘő´╝îš╗ÖňůŹšľźŠ▓╗šľŚŠ▓╗ŠäłGBMňó×ňŐáń║抾░šÜäÚÜżň║ŽňĺîŠîĹŠłśŃÇé
ŠáŞň┐âŠŐÇŠť»šŚŤšé╣´╝ÜGBMňůŹšľźÚÇâÚÇŞŠť║ňłÂńŞ░ň»î´╝îń║čÚťÇňłŤŠľ░ŠÇžšľŚŠ│ĽGBM
ň»╣š╗ćŔâ׊▓╗šľŚŔŹ»šëęňůĚŠťëň╝║ňĄžšÜäŔÇÉŔŹ»ŠÇž´╝îňůŹšľźňÄčŠÇžňĆŹň║öň╝▒´╝îÚÇÜŔ┐çÚçŹňíĹŔé┐šśĄňż«šÄ»ňóâŔ┐ŤŔíîňůŹšľźÚÇâÚÇŞ´╝îń╝áš╗čšÜäŠúÇŠčąšé╣ŠŐĹňłÂňëéň»╣ňůÂńŞŹŔâŻń║žšöčŔë»ňąŻšÜäšľŚŠĽłŃÇéšÖçňůŹšľźŠ▓╗šľŚňůČňĆŞInovio Pharmań║Ä2020ň╣┤šą×š╗ĆŔé┐šśĄň╣┤ń╝ÜńŞŐňůČňŞâńŞëŔüöňůŹšľźšľŚŠ│ĽIIŠťčńŞ┤ň║ŐšáöšęÂÚś│ŠÇžš╗ôŠ×ť´╝îňîůŠőČTš╗ćŔâ׊┐ÇŠ┤╗ňůŹšľźšľŚŠ│ĽINO-5401ŃÇüš╝ľšáüIL-12šÜäňůŹšľźŠ┐ÇŠ┤╗ňëéINO-9012ŔüöňÉłPD-1Úś╗ŠľşŠÇžŠŐŚńŻôLibtayoŃÇéŠö╗ňůőÚÜżŠ▓╗ŠÇžŔé┐šśĄÚťÇŔŽüń╗ąňč║šíÇšáöšęÂńŞ║ňč║šč│´╝îń╗ąňłŤŠľ░ŠÇžŔŹ»šëęŔ»ĽÚ¬îńŞ║ŔÉŻŔäÜšé╣´╝îń╗ąŔüöňÉłšľŚŠ│ĽńŞ║ŠëőŠ«Á´╝îń╗ÄŔÇîš╗ÖŔé┐šśĄŠéúŔÇůňŞŽŠŁąšŽĆÚč│ŃÇé
ňŤŻňćůŠŐĽŔÁäŠíłńżő´╝Üń╝śňŹíŔ┐¬ň«îŠłÉŠĽ░ňŹâńŞçB+ŔŻ«Ŕ׏ŔÁä
2021ň╣┤3Šťł30ŠŚą´╝îńŞôŠ│Ęń║ÄŔç¬ńŞ╗ňłŤŠľ░ň×őCAR-T 2.0ń║žňôüšáöňĆĹšÜäńŞŐŠÁĚń╝śňŹíŔ┐¬šöčšëęňî╗ŔŹ»šžĹŠŐÇŠťëÚÖÉňůČňĆŞň«úňŞâň«îŠłÉŠĽ░ňŹâńŞçB+ŔŻ«Ŕ׏ŔÁäŃÇ銺ĄŔŻ«Ŕ׏ŔÁäšö▒ňżĚŔžéŔÁ䊝ČÚóćŠŐĽ´╝̊şúŠŐĽŔÁäŔĚčŠŐĽŃÇéňőčÚŤćŔÁäÚçĹň░ćň║öšöĘń║ÄňůČňĆŞÚŽľńެCAR-T 2.0ń║žňôüssCART-19Š│Ęň░äŠÂ▓ńŞ┤ň║ŐŔ»ĽÚ¬îšÜäŠÄĘŔ┐Ť´╝îňĄÜńެŠľ░ń║žňôüšÜäINDšö│ŠŐąňĆŐńŞ┤ň║ŐŔ»ĽÚ¬îšÜäň┐źÚÇčňÉ»ňŐĘ´╝îń╗ąňĆŐň«×ńŻôŔé┐šśĄň║öšöĘšÜ䊾░ň×őňÇÖÚÇëń║žňôüšÜäň╝ÇňĆĹňĺîÚ¬îŔ»üŃÇ銝¬ŠŁąń╝śňŹíŔ┐¬ň░ćňžőš╗łŔç┤ňŐŤń║ÄŠľ░ńŞÇń╗úCAR-TŠŐÇŠť»šÜäšáöňĆĹ´╝îńŞôŠ│Ęń║Äň╝ÇňĆĹŠŤ┤ň«ëňůĘŃÇüŠŤ┤ŠťëŠĽłšÜäŔé┐šśĄšľŚŠ│ĽŃÇéňŹíŠŤ┐ňî╗šľŚň«îŠłÉŠĽ░ń║┐ń║║Š░ĹňŞüPre-BŔŻ«Ŕ׏ŔÁä2021ň╣┤2Šťł10ŠŚą´╝îńŞôŠ│ĘšáöšęÂŔé┐šśĄŠÁŞŠÂŽŠĚőňĚ┤š╗ćŔâךľŚŠ│Ľ(TIL)šÜäšöčšëęŠŐÇŠť»ń╝üńŞÜňŹíŠŤ┐ňî╗šľŚň«îŠłÉń║┐ňůâš║žń║║Š░ĹňŞüPre-BŔŻ«Ŕ׏ŔÁä´╝îńŞ░ň╗¬ŔÁ䊝ČÚóćŠŐĽŃÇéňîŚń║ČňŹíŠŤ┐ňî╗šľŚňůČňĆŞŠś»ňŤŻňćůňö»ńŞÇŠőąŠťëňłŤŠľ░TILšľŚŠ│ĽšÜäń║║ńŻôńŞ┤ň║ŐšáöšęŠĽ░ŠŹ«šÜäń╝üńŞÜŃÇéňůČňĆŞň돊ťčšÜäÔÇťŔÂůň╝║ň×őTILÔÇŁŠ▓╗šľŚŠÖÜŠťčń╝áš╗čŠ▓╗šľŚŠŚáŠĽłň«×ńŻôšśĄšÜ䊎éň┐ÁÚ¬îŔ»ü(POC)ńŞ┤ň║ŐšáöšęŠĽ░ŠŹ«ňĚ▓š╗Ćň▒ĽšÄ░ń║ćń╗Ąń║║Šî»ňąőšÜ䊳ɊםŃÇéňůšáöňĆĹšÜäšČČňŤŤń╗úń║žňôüÔÇťŔÂůň╝║ň×őcTILÔÇŁń╗ůÚťÇÚççÚŤćňĄľňĹĘŔíÇńŞşšÜäTILš╗ćŔâ×´╝üšá┤Ŕé┐šśĄš╗äš╗çňĆľŠŁÉšÜäň▒ÇÚÖÉŠÇž´╝îŠőôň▒Ľń║ćŔ»ąšľŚŠ│ĽšÜäÚÇéšöĘń║║šżĄŃÇé
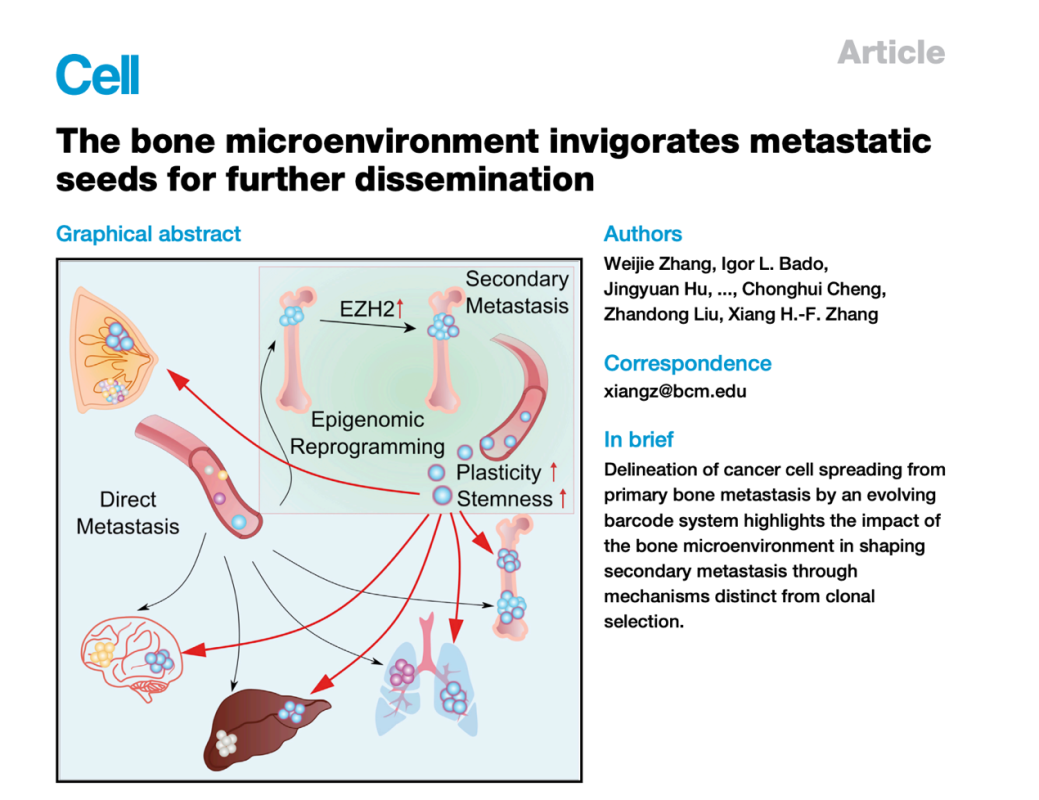
ŠťČš»çńŞ║šżÄňŤŻŔ┤Łňőĺňî╗ňşŽÚÖóXiang H.-F. ZhangňŤóÚśčňĆĹŔíĘšÜäArticleŠľçšźáŃÇéŔŻČšž╗ŔóźŔ«ĄńŞ║Šś»Ŕé┐šśĄňĆĹň▒ĽšÜ䊝ÇňÉÄńŞÇŠşąŃÇéšäÂŔÇî´╝ÇŔ┐ĹšÜäňč║ňŤáš╗äšáöšęÂŔíĘŠśÄ´╝îŔ«ŞňĄÜŔŻČšž╗Šś»šö▒ňůÂń╗ľŔŻČšž╗šÜäŔ┐ŤńŞÇŠşąŠëꊼúň╝ĽŔÁĚšÜäŃÇéšäÂŔÇî´╝«ňëŹň░Üš╝║ń╣ĆšŤŞň║öšÜäńŞ┤ň║Őň돊Ęíň×ő´╝îňůŠť║ňłÂň░ÜńŞŹŠŞůŠąÜŃÇéňťĘŔ┐Öš»çŔ«║ŠľçńŞş´╝îšáöšęÂŔÇůńŻ┐šöĘň╝éšžŹňů▒šöčňĺîŔ┐ŤňŁíňŻóšáüš│╗š╗蚺늾╣Š│Ľ´╝îŔ»üŠśÄń║ćÚ¬Ęňż«šÄ»ňóâń┐âŔ┐Ťń╣│Ŕů║šÖîňĺîňëŹňłŚŔů║šÖîš╗ćŔâךÜäŔ┐ŤńŞÇŠşąŔŻČšž╗ň╣Âň╗║šźőňĄÜňÖĘň«śš╗žňĆĹŔŻČšž╗ŃÇéń╗ľń╗ČňĆĹšÄ░Ŕ┐ÖšžŹń┐âŔ┐ŤŔŻČšž╗šÜäńŻťšöĘŠś»šö▒ŔíĘŔžéÚüŚń╝áÚ珚╝ľšĘőÚę▒ňŐĘšÜä´╝îŔíĘŔžéÚüŚń╝áÚ珚╝ľšĘőŔÁőń║łÚ¬ĘŠëꊼúšÜäšÖîš╗ćŔâ×ň╣▓š╗ćŔâ׊áĚšë╣ŠÇžŃÇ銺ĄňĄľ´╝îń╗ľń╗ČňĆĹšÄ░EZH2Š┤╗ŠÇžňó×ňŐáňĆ»ń╗őň»╝Ŕé┐šśĄň╣▓š╗ćŔâ×ňĺîŔŻČšž╗ŔâŻňŐŤšÜäňó×ňŐáŃÇéňÉîŠáĚšÜäňĆĹšÄ░ń╣čÚÇéšöĘń║ÄňŹĽš╗ćŔâ׊ŁąŠ║ÉšÜäšżĄńŻô´╝îŔíĘŠśÄňůŠť║ňłÂńŞŹňÉîń║ÄňůőÚÜćÚÇëŠőęŃÇéš╗╝ńŞŐŠëÇŔ┐░´╝îń╗ľń╗ČšÜäňĚąńŻťŠĆşšĄ║ń║ćÚ¬Ęňż«šÄ»ňóâňťĘŔŻČšž╗ňĆĹň▒ĽńŞşšÜäńŻťšöĘ´╝îň╣ÂڜɊśÄń║ćÚę▒ňŐĘš╗łŠťźŠťčňĄÜňÖĘň«śŔŻČšž╗šÜäŔíĘŔžéňč║ňŤáÚ珚╝ľšĘőŔ┐çšĘő´╝îŔ┐śŠîçňç║ň╣▓ÚóäŔé┐šśĄš╗ćŔâךÜäŔíĘŔžéÚüŚń╝áŔ░âŠÄžňĆ»ŠťëŠĽłŠŐĹňłÂÚ¬Ęňż«šÄ»ňóâń╗őň»╝šÜäš╗žňĆĹŠÇžŔŻČšž╗ŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.011)
ŠťČš»çńŞ║ňŐáňłęšŽĆň░╝ń║ÜňĄžňşŽJonathan S. WeissmanňŤóÚśčňĆĹŔíĘšÜäResourceŠľçšźáŃÇéňťĘCRISPRšÜäňč║šíÇń╣őńŞŐ´╝îń╗ľń╗ČŠĆÉňç║ń║ćńŞÇšžŹňĆ»š╝ľšĘőšÜäŔŻČňŻĽŔ░âŠÄžš╝ľŔżĹňÖĘCRISPRoff´╝îšö▒ńŞžňĄ▒Š┤╗ŠÇžšÜäCas9ŔŤőšÖŻ´╝łdCas9´╝ëňĺîDNAšö▓ňč║ŔŻČšž╗ÚůÂŔ׏ňÉłŔÇɴ╝îÚÇÜŔ┐çňťĘňč║ňŤáńŞşňŐáňůąŠłľšž╗ÚÖĄšö▓ňč║ňîľń┐«Úą░ŠŁąŠÄžňłÂňč║ňŤášÜäŔíĘŔżżŃÇéCRISPRoffš×ČŠŚÂŔíĘŔżżňĆ»ňÉ»ňŐĘÚźśň║Žšë╣ň╝éšÜäDNAšö▓ňč║ňîľňĺîňč║ňŤáŠŐĹňłÂ,ň╣ÂňĆ»ÚÇÜŔ┐çŔŻČňŻĽŔ░âŠÄžŔ»▒ň»╝ňĄÜŔâŻň╣▓š╗ćŔâ×ňłćŔúéňłćňîľńŞ║šą×š╗ĆňůâŃÇéšáöšęÂŔÇůŔ┐śň╝ÇňĆĹń║ćńŞÇšžŹńŞÄCRISPRoffňŐčŔ⯚ŤŞňĆŹšÜäš╝ľŔżĹňÖĘ´╝îň«âÚÇÜŔ┐çŔ׏ňÉłDNAňÄ╗šö▓ňč║ňîľÚůÂňĺîŔŻČňŻĽŠ┐ÇŠ┤╗ňŤáňşÉŠŁąÚÇćŔŻČňč║ňŤáŔŻČňŻĽŠŐĹňłÂšŐŠÇü´╝îń┐âŔ┐Ťňč║ňŤáŔíĘŔżżŃÇéšáöšęÂŔÇůš╗ôňÉłňůĘňč║ňŤáš╗äšşŤÚÇëňĺîŠčôŔë▓Ŕ┤ĘŠáçŔ«░ňłćŠ×É´╝îňĆĹšÄ░CRISPRoffŔâŻňĄčŠ▓ëÚ╗śš╗ŁňĄžňĄÜŠĽ░ňč║ňŤášÜäsgRNAs´╝îň»╣ń║Äš╝║ń╣ĆňůŞň×őCpGň▓ŤšÜäňč║ňŤáń╣čňÉîŠáĚŠťëŠĽłŃÇéšáöšęÂŔÇůÚÇÜŔ┐çCRISPRoffň«×šÄ░šą×š╗ĆňůâńŞşTauŔŤőšÖŻŔíĘŔżżÚÖŹńŻÄ´╝îňĆ»ŔâŻńŞ║Úś┐ň░öňů╣ŠÁĚÚ╗śšŚçšÜäÚóäÚś▓Š▓╗šľŚŠĆÉńżŤńŞÇšžŹňĆ»ŔíîšşľšĽąŃÇé´╝łŠĹśŔŽü´╝ë(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.025)
ŠŐĽŔÁäÚó䊝č´╝ÜCRISPRŔ폚öčŠŐÇŠť»ň║öšöĘň╣┐Š│Ť´╝îŔíĘŔžéÚüŚń╝áń┐«Úą░ňĄžŠťëňĆ»ńŞ║
CRISPRňč║ňŤáš╝ľŔżĹŠŐÇŠť»ŠťÇňłŁšöĘń║ÄńŻŹšé╣šë╣ň╝éŠÇžšÜäňč║ňŤáš╗äš╝ľŔżĹ´╝îŔÇîňÉÄšžĹňşŽň«Âń╗Čň»╣ňůÂŔ┐ŤńŞÇŠşąŠÄóš┤ó´╝îň╝ÇňĆĹňç║šöĘń║ÄŔŻČňŻĽŔ░âŠÄžšÜäŔ폚öčŠŐÇŠť»ŃÇéŠö╣ÚÇáňżŚňł░ńŞŹňůĚŠťëňłçňë▓Š┤╗ŠÇžšÜädCas9´╝îňťĘsgRNAšÜäń╗őň»╝ńŞőń╗ŹňĆ»ń╗ąÚŁÂňÉĹňč║ňŤáš╗äň║ĆňłŚ´╝îňĆ»ŠťëŠĽłšÜäŠ┐ÇŠ┤╗ŠłľŠŐĹňłÂš╝ľšáüňč║ňŤáňĺîڣך╝ľšáüňč║ňŤášÜäŔíĘŔżżŃÇéÚóçňůĚń╗úŔíĘŠÇžšÜäCRISPRiňĺîCRISPRaňŁçňč║ń║ÄdCas9Ŕ┤Ęš▓ĺň╝ÇňĆĹ´╝îňůÂńŞşCRISPRińŻťńŞ║Šľ░ňů┤ŠŐÇŠť»šÜäń╗úŔíĘ´╝îňçşňÇčňůŠŤ┤ńŻÄšÜäŔä▒ڣŠĽłň║ö´╝úňťĘŠîĹŠłśRNAiňťĘňč║ňŤáŔíĘŔżżŔ░âŠÄžńŞşšÜäň╣┐Š│Ťň║öšöĘŃÇé2015ň╣┤´╝îSigma AldrichŠÄĘňç║ńŞÇŠČżCRISPRŔíĘŔžéÚüŚń╝áňéČňîľňëé´╝îň░ćCRISPRŠŐÇŠť»šÜäŔ┐ÉšöĘŠőôň▒Ľňł░ŔíĘŔžéÚüŚń╝áňşŽŠ░┤ň╣│ŃÇéŔ»ąŠŐÇŠť»ÚÇÜŔ┐çń╣ÖÚů░ňîľšë╣ň«ÜšÜäš╗äŔŤőšÖŻ´╝îŠ┐ÇŠ┤╗šŤ«Šáçňč║ňŤá´╝îň«×šÄ░ńŞŹŠö╣ňĆśDNAň║ĆňłŚšÜäň돊ĆÉńŞőň»╣ňč║ňŤáš╗äŔ┐ŤŔíîń┐«Úą░ŃÇ銝Ț»çŠľçšźáň░ćŔíĘŔžéÚüŚń╝ášö▓ňč║ňîľń┐«Úą░ńŞÄňč║ňŤáŔŻČňŻĽŔ░âŠÄžŔüöš│╗ŔÁĚŠŁą´╝늝ŤňťĘCRISPRi/CRISPRań╣őňÉÄ´╝ÉńŞ║ńŞőńŞÇńެňĽćńŞÜňîľńŻ┐šöĘšÜäňč║ń║ÄCRISPRŠŐÇŠť»šÜäŔŻČňŻĽŔ░âŠÄžňĚąňůĚŃÇé
ŠáŞň┐âŠŐÇŠť»šŚŤšé╣´╝Üň«ëňůĘŠÇžŠłÉńŞ║CRISPRŔíĘŔžéÚüŚń╝áŔ폚öčŠŐÇŠť»ň║öšöĘšÜäňů│Úö«šé╣
CRISPR-Cas9ŠŐÇŠť»ň║öšöĘń║ÄŔíĘŔžéÚüŚń╝áń┐«Úą░Úóćňčč´╝îńŞ║šžĹňşŽň«ÂŠôŹš║ÁŔíĘŔžéÚüŚń╝áňůâń╗ÂňŞŽŠŁąń║ćň돊ëÇŠť¬ŠťëšÜ䊝║ń╝ÜŃÇéńŻćň«ëňůĘŠÇžń╗ŹŠś»CRISPRŔ폚öčŠŐÇŠť»ň║öšöĘšÜäńŞ╗ŔŽüÚŚ«Úóś´╝îňůší«ňłçŠ░┤ň╣│šÜäŔä▒ڣŠ░┤ň╣│Ŕ┐śŠť¬ňżŚňł░ŔíĘňżüŃÇé
ňŤŻňćůŠŐĽŔÁäŠíłńżő´╝ÜňŹÜÚŤůŔżĹňŤáň«îŠłÉ4ń║┐ňůâB+ŔŻ«Ŕ׏ŔÁä
2021ň╣┤4Šťł21ŠŚą´╝îń╗ąňč║ňŤáš╗äš╝ľŔżĹŠŐÇŠť»ńŞ║ňč║šíÇšÜäšöčšëęňî╗ŔŹ»ń╝üńŞÜňŹÜÚŤůŔżĹňŤáň«úňŞâň«îŠłÉ4ń║┐ňůâšÜäB+ŔŻ«Ŕ׏ŔÁä´╝îŔ┐ÖŔŻ«Ŕ׏ŔÁäšö▒Šşúň┐âŔ░ĚŔÁ䊝ČÚóćŠŐĽ´╝îňŹÜŔ┐ťŔÁ䊝ČŃÇüňĄĆň░öňĚ┤ŠŐĽŔÁäšşëŔĚčŠŐĽ´╝îňŹÜÚŤůŔżĹňŤášÄ░ŠťëŠŐĽŔÁäŔÇůIDGŔÁ䊝ČŃÇüšĄ╝ŠŁąń║ÜŠ┤▓ňč║ÚçĹŃÇüš║óŠŁëŔÁ䊝ČńŞşňŤŻňč║ÚçĹšşëŔĚčŠŐĽŃÇéŔ┐ÖŠś»ňŹÜÚŤůŔżĹňŤáňťĘňÄ╗ň╣┤10ŠťłBŔŻ«Ŕ׏ŔÁä4.5ń║┐ňůâń╣őňÉÄŔ┐ŻňŐášÜäB+ŔŻ«Ŕ׏ŔÁä´╝îňůÂňůČňĆŞšž░Ŕ┐ŻňŐášÜäŔ┐ÖŔŻ«Ŕ׏ŔÁäň░ćŔóźšöĘń║ÄŠÄĘŔ┐ŤňůÂń╗ąňč║ňŤáš╝ľŔżĹŠŐÇŠť»ńŞ║ňč║šíÇšÜäń║žňôüš«íš║┐šÜäńŞ┤ň║ŐŔŻČňîľ´╝îŠÄĘňŐĘń║žńŞÜňîľňĆĹň▒ĽŃÇéŔżëňĄžňč║ňŤáň«îŠłÉ4ń║┐ňůâBŔŻ«Ŕ׏ŔÁä2021ň╣┤5Šťł17ŠŚą´╝îšö▒ňĄÜň«ÂňůĘšÉâščąňÉŹňč║ÚçĹňů▒ňÉîŠŐĽŔÁä´╝îŔÇüŔéíńŞťŠîüš╗şňŐáŠîüŃÇ銏«ń║ćŔžú´╝ČŔŻ«Ŕ׏ŔÁäň░ćšöĘń║ÄŠö»ŠîüňůČňĆŞŠŐÇŠť»ňłŤŠľ░´╝îń║žňôüńŞ┤ň║Őň돚áöňĆĹńŞÄńŞ┤ň║ŐŠ│Ęňćî´╝îŔŹ»šëęŔŻČňîľńŞşŔ»Ľň╣│ňĆ░ň╗║Ŕ«żń╗ąňĆŐň«îňľäšöčń║žńŞÄńŞ┤ň║Őň╝ÇňĆĹňŤóÚśčŃÇéŔżëňĄžňč║ňŤáňłŤňžőń║║ŃÇüŔĹúń║őÚĽ┐ňů╝ÚŽľňŞşšžĹňşŽÚíżÚŚ«ńŞ║ŠŁĘŔżëňŹÜňúźňťĘňč║ňŤáš╝ľŔżĹÚóćňččŠĚ▒ŔÇĽňĄÜň╣┤´╝îň╗║šźőń║ćńŞÇšžŹŔóźňĹŻňÉŹńŞ║GOTIšÜ䊾░ň×őŔä▒ڣŠúÇŠÁőŠŐÇŠť»´╝îň╣ÂńŞöňĆĹŠśÄń║ćńŞŹń╝Üń║žšöčŔ»»ń╝ĄšÜ䊾░ńŞÇń╗úňč║ňŤáš╝ľŔżĹŠŐÇŠť»´╝îń╗ÄŔÇîńŻ┐ňč║ňŤáš╝ľŔżĹŠŤ┤ňŐáň«ëňůĘŃÇüÚźśŠĽł´╝îńŞ║ňůÂŔ┐ŤňůąńŞ┤ň║ŐŠĆÉńżŤń║ćÚçŹŔŽüšÜäň«ëňůĘń┐ŁÚÜťŃÇé
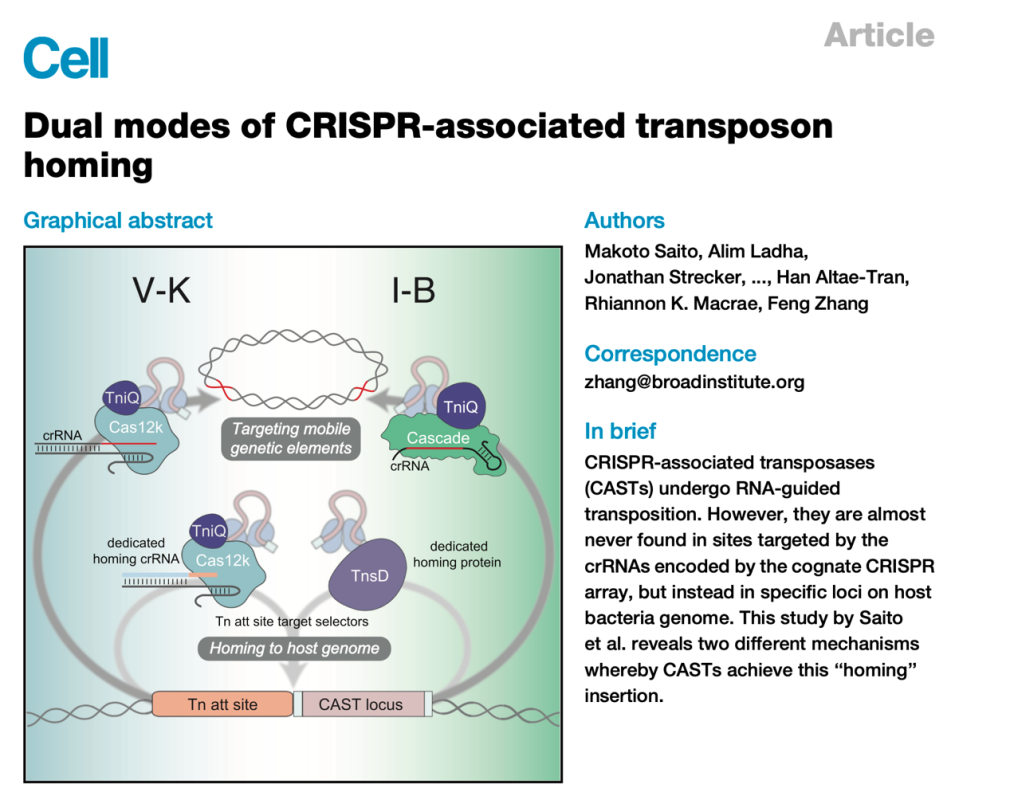
┬ኝȚ»çńŞ║šżÄňŤŻBroadšáöšęŠëÇšÜäň╝áÚöőňŤóÚśčňĆĹŔíĘšÜäArticleŠľçšźáŃÇ銾çńŞşň»╣ńŞŹňÉîš▒╗ň×őCASTš│╗š╗čšÜäňŻĺňĚóŠť║ňłÂŔ┐ŤŔíîń║ćš│╗š╗čšáöšę´╝îš╗ôŠ×ťňĆĹšÄ░ń║ćńŞĄšžŹŠł¬šäÂńŞŹňÉîšÜäňŻĺňĚóŠť║ňłÂ´╝ÜňůÂńŞşV-Kň×őCASTš│╗š╗čńżŁŔÁľń║ÄCRISPRÚśÁňłŚń╣őňĄľšÜäň╝éńŻŹščşÚôżcrRNAň«×šÄ░ňŻĺňĚó´╝îŔÇîI-Bň×őCASTš│╗š╗čňłÖńżŁŔÁľń║ÄTnsDŔŤőšÖŻň«×šÄ░ňŻĺňĚóŃÇéŔ┐ÖńŞÇšáöšęÂŔ«ęŠłĹń╗Čň»╣CASTš│╗š╗čšÜäňĄÜŠáĚŠÇžŠťëń║抍┤ŠĚ▒ňůąšÜäŔ«ĄŔ»ć´╝îń╣čńŞ║Šť¬ŠŁąšÜäŠö╣ÚÇáňĺîň║öšöĘňąáň«Üń║ćňč║šíÇŃÇé´╝łŠĹśŔŽü´╝ë(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.006)
ňŤŤŃÇüňůÂń╗ľŠľçšźáŠĹśŔŽüŔÁĆŠ×É
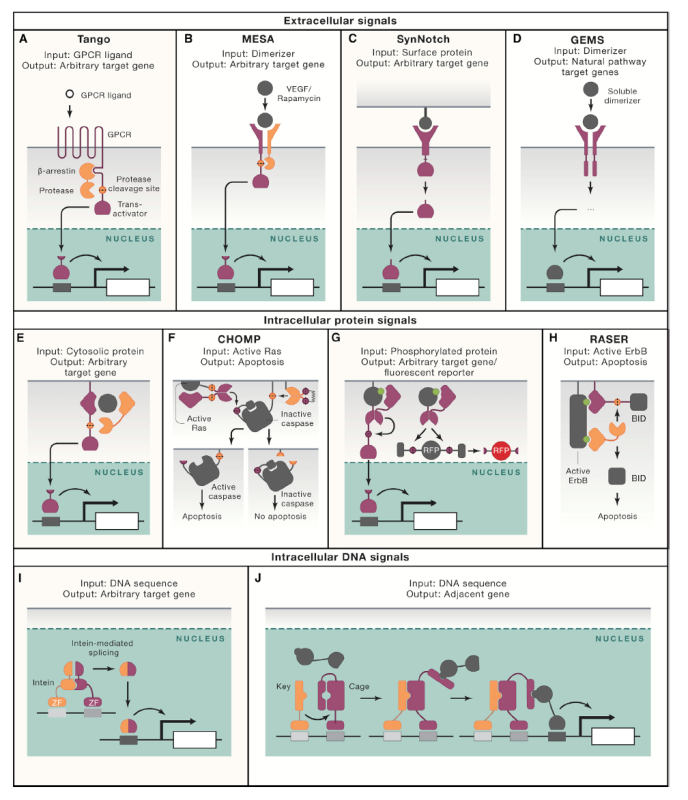
┬ኝȚ»çńŞ║ňŐáňĚךÉćňĚąňşŽÚÖóšÜäMichael ElowitzňŤóÚśčňĆĹŔíĘšÜäReviewŠľçšźáŃÇéňÉłŠłÉšöčšëęňşŽšÜäńŞÇńެňč║ŠťČŠîĹŠłśŠś»ňłŤÚÇáňç║ŔâŻňĄčň»╣ňĄŹŠŁéš╗ćŔâ×ňŐčŔâŻŔ┐ŤŔíîš╝ľšĘőšÜäňłćňşÉšÄ»ŔĚ»ŃÇéŔŤőšÖŻŔ┤ĘňĆ»ń╗ąšŤŞń║ĺš╗ôňÉłŃÇüňłćŔúéŃÇüŔ┐ŤŔíîňîľňşŽń┐«Úą░´╝îň╣ÂńŞÄňćůŠ║ÉŠÇžÚÇöňżäšŤ┤ŠÄąńŞöň┐źÚÇčňť░ňüÂŔüö´╝îŠëÇń╗ąňč║ń║ÄŔŤőšÖŻŔ┤ĘšÜäŔ░âŠÄžŔ«żŔ«íňĆ»ń╗ąŔ┐ŤńŞÇŠşąŠőôň▒ĽňÉłŠłÉšöčšëęňşŽšÜäňĚąšĘőŔâŻňŐŤŃÇ銝ÇŔ┐ĹšÜäňĚąńŻťňĚ▓š╗Ćň╝ÇňžőŔžúňć│Ŕ┐ÖńŞÇŠîĹŠłś´╝îÚŤćńŞşňťĘŔ»ŞňŽéŠşúń║ĄŠÇžňĺîňĆ»š╗äňÉłŠÇžšşëňÄčňłÖńŞŐ´╝îŔ┐Öń║ŤňÄčňłÖňůüŔ«Şń╗ÄńŞÇš╗䊝ëÚÖÉšÜäňĚąšĘőŔŤőšÖŻŔ┤Ęš╗äňłćŠ×äň╗║ńŞŹňÉîšÜäšÄ»ŔĚ»ňŐčŔâŻŃÇéŔ┐Öń║ŤŠľ╣Š│ĽŠşúňťĘńŻ┐ŔâŻňĄčŠäčščąŃÇüń╝áŔżôňĺîňĄäšÉćń┐íŠü»šÜäňłćňşÉšÄ»ŔĚ»ňĚąšĘőňîľ´╝îŔâŻňĄčňŐĘŠÇüŠÄžňłÂš╗ćŔâ×ŔíîńŞ║´╝îň╣ÂňÉ»šöĘŠľ░šÜäŠ▓╗šľŚšşľšĽą´╝îň╗║šźőńŞÇńެň╝║ňĄžšÜäš╝ľšĘőšöčšëęňşŽŔîâň╝ĆŃÇé´╝łŠĹśŔŽü´╝ë(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.007)
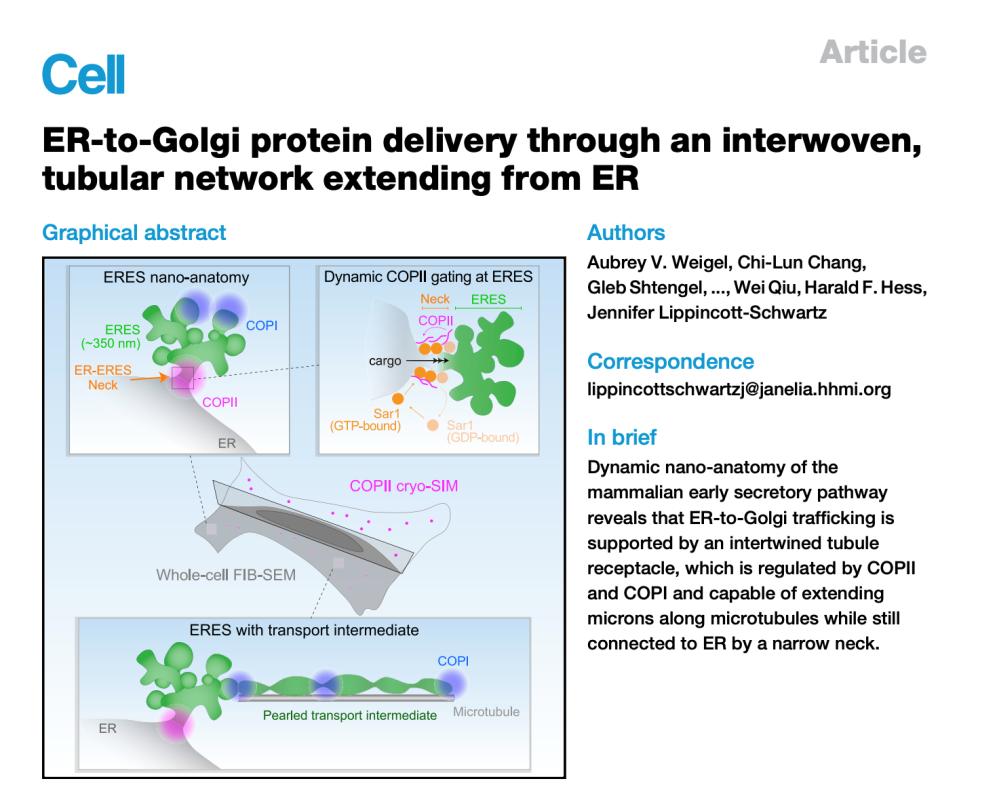
┬ኝȚ»çńŞ║šżÄňŤŻÚťŹňŹÄňżĚ┬Ěń╝ĹŠľ»ňî╗ňşŽšáöšęŠëÇšÜäJennifer Lippincott-SchwartzňŤóÚśčňĆĹŔíĘšÜäArticleŠľçšźáŃÇéňô║ń╣│ňŐĘšëꊌꊝčňłćŠ│îÚÇöňżäšÜäňŐĘŠÇüš║│š▒│ŔžúňëľňşŽŠĆşšĄ║ňćůŔ┤ĘšŻĹňł░Úźśň░öňč║ńŻôšÜäŔ┐ÉŔżôŠś»šö▒ńŞÇńެšŤŞń║ĺń║Ąš╗çšÜäňż«š«íš│╗š╗čŠö»ŠîüšÜä´╝îŔ»ąš│╗š╗čšö▒COPIIňĺîCOPIŔ░âŔŐé´╝îŔâŻňĄčŠ▓┐šŁÇňż«š«íň╗Âń╝Şňż«š▒│´╝îňÉÂń╗ŹšäÂÚÇÜŔ┐çšőşš¬äšÜäÚółÚâĘńŞÄňćůŔ┤ĘšŻĹšŤŞŔ┐×ŃÇéš╗ćŔâ×ňćůšÜäňĄÜšžŹňŐčŔâŻńżŁŔÁľń║ÄňÉäšžŹŔŤőšÖŻŔ┤Ęš▓żší«Ŕ┐ÉŔżôňł░ňůšŤ«šÜäš╗ćŔâ×ňÖĘŃÇéň»╣ń║ÄňłćŠ│îÚÇöňżä´╝łš║ŽňŹáŠëÇŠťëŔŤőšÖŻŔ┤ĘšÜä30%´╝ë´╝îŔ┐ŤŔíîšČČńŞÇŠČíŔ┐ÉŔżô´╝łń╗ÄňćůŔ┤ĘšŻĹňł░Úźśň░öňč║ńŻô´╝ëšÜäšëęšÉćŠÇžŔ┤Ęň░ÜńŞŹŠŞůŠąÜŃÇéšáöšęÂŔÇůňłęšöĘňůĘš╗ćŔâ×ŃÇüŔüܚ䎚Ž╗ňşÉŠŁčŠëźŠĆĆšöÁňşÉŠśżňż«ÚĽťŃÇüňćĚňć╗š╗ôŠ×äšůžŠśÄŠśżňż«ÚĽťňĺîŠ┤╗š╗ćŔâ×ňÉąŔ┤žšëęÚçŐŠöżŠľ╣Š│Ľ´╝îŠĆÉńżŤń║ćňô║ń╣│ňŐĘšëęš╗ćŔâ׊ŚęŠťčňłćŠ│îň«ĄšÜäńŞëš╗┤ňŐĘŠÇüŔžćňŤż´╝îňůĚŠťëňÉäňÉĹňÉîŠÇžňłćŔżĘšÄçňĺîš▓żší«šÜäŔŤőšÖŻŔ┤Ęň«ÜńŻŹŃÇéňćůŔ┤ĘšŻĹńŞŹŠś»ňŹĽšőČšÜäňŤŐŠ│í´╝îŔÇ»ń║žšöčńŞÇńެšö▒šŤŞÚé╗šÜäŔäéŔ┤ĘňĆîň▒é´╝łňćůŔ┤ĘšŻĹňç║ňĆúÚâĘńŻŹ´╝ëš╗䊳ɚÜäňĄŹŠŁéŃÇüń║Ąš╗çšÜäš«íšŐšŻĹš╗ť´╝îšöĘń║ÄŔŤőšÖŻŔ┤ĘŔżôňç║ŃÇéCOPIIň«ÜńŻŹń║ÄŔ┐ÖńެÚółÚâĘňî║ňččň╣ÂňŐĘŠÇüŔ░âŔŐ銣ąŔç¬ňćůŔ┤ĘšŻĹšÜäŔŤőšÖŻŔ┤Ę´╝îŔÇîCOPIšÜäńŻťšöĘŠŤ┤ńŞ║Ŕ┐ťšź»´╝îŠŐĄÚÇüňŐáÚÇčňłćšŽ╗šÜäš«íšŐÂň«×ńŻôÚÇÜŔ┐çňż«š«íň«ÜňÉĹŔ┐ÉňŐĘň╣ÂŔ┐׊ĹŔç│Úźśň░öňč║ńŻôŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.035)
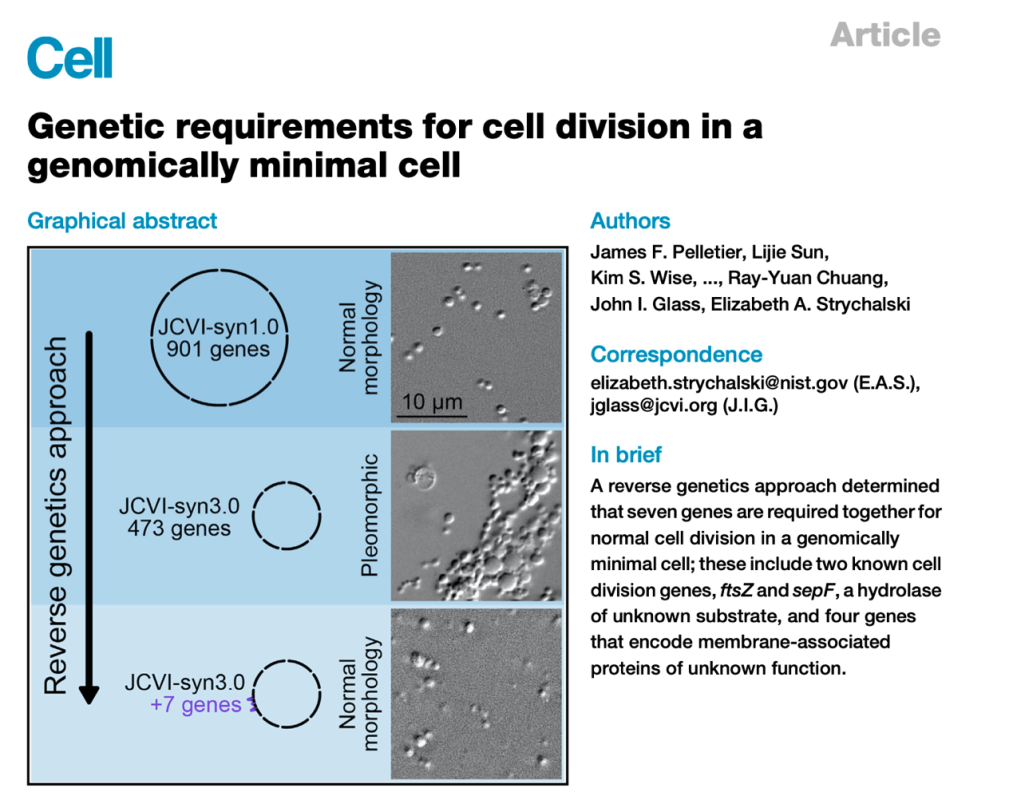
ŠťČš»çńŞ║šżÄňŤŻňŤŻň«ÂŠáçňçćńŞÄŠŐÇŠť»šáöšęÂÚÖóElizabeth A. StrychalskiňŤóÚśčňĆĹŔíĘšÜäArticleŠľçšźáŃÇéńŞ║ń║ćšáöšęÂJCVI-syn3.0š╗ćŔâ×ńŞşŠâŐń║║šÜäňŻóŠÇüňĆśň╝é´╝îšáöšęÂŔÇůň╝ÇňĆĹń║ćŔíĘňżüš╗ćŔâ×ňó׊«ľň╣ÂÚë┤ň«ÜňŻ▒ňôŹš╗ćŔâ×ňŻóŠÇüňč║ňŤášÜ䊾╣Š│ĽŃÇéňż«ŠÁüŠÄžňîľňşŽŠü努ęňÖĘňĆ»ń╗ąŔžéň»čň»╝Ŕç┤ńŞŹŔžäňłÖňŻóŠÇüšÜäňćůňťĘš╗ćŔâ×ňŐĘňŐŤňşŽŃÇéJCVI-syn3.0ńŞşńŞŹňůĚŠťë19ńެňč║ňŤášÜäňč║ňŤáš╗äń║žšöčń║ćJCVI-syn3A´╝îňůÂňŻóŠÇüńŞÄJCVI-syn1.0šŤŞń╝╝ŃÇéšáöšęÂŔÇůŔ┐ŤńŞÇŠşąÚë┤ň«Üń║ćŔ┐Ö19ńެňč║ňŤáńŞşšÜä7ńެ´╝îňîůŠőČńŞĄńެňĚ▓ščąšÜäš╗ćŔâ×ňłćŔúéňč║ňŤáftsZňĺîsepFŃÇüńŞÇńެŠť¬ščąň║ĽšëęšÜäŠ░┤ŔžúÚů´╝îń╗ąňĆŐňŤŤńެš╝ľšáüŠť¬ščąňŐčŔ⯚ÜäŔćťšŤŞňů│ŔŤőšÖŻšÜäňč║ňŤá´╝îŔÇîŠüóňĄŹńŞÄ JCVI-syn1.0ŔíĘň×őšŤŞń╝╝šÜäŔíĘň×őÚťÇŔŽüŔ┐Öń║Ťňč║ňŤášÜäňů▒ňÉîňşśňťĘŃÇéŔ┐Öń║Ťš╗ôŠ×ťň╝║Ŕ░âń║ćňč║ňŤáš╗䊝Çň░Ćš╗ćŔâ×ńŞşš╗ćŔâ×ňłćŔúéňĺîňŻóŠÇüšÜäňĄÜňč║ňŤáŠÇžŔ┤ĘŃÇ銏«ń╗őš╗Ź´╝îňč║ňŤáš╗䊝Çň░ĹšÜäš╗ćŔâ×´╝îńżőňŽéJCVI-syn3.0´╝îŠĆÉńżŤń║ćڜɊśÄŠáŞň┐âšöčšÉćŔ┐çšĘőšÜäňč║šíÇňč║ňŤášÜäň╣│ňĆ░ŃÇéň░Żš«íŔ┐ÖšžŹŠťÇň░ĆšÜäš╗ćŔâ×ňîůňÉźń║ćšžŹšżĄňó×ÚĽ┐ŠëÇň┐ůڝǚÜäňč║ňŤá´╝îńŻćňůÂňŹĽńެš╗ćŔâךÜäšöčšÉćňşŽń╗ŹńŞŹŠśÄŠÖ░ŃÇé(ňÄ芾çÚôżŠÄą´╝Ühttps://doi.org/10.1016/j.cell.2021.03.008)