

Šť¬ŠŁąňŹüň╣┤´╝îňÉłŠłÉšöčšëęňşŽň░ćń╝ÜňŻ╗ň║ĽňĆśÚŁęňćťńŞÜŃÇüÚą«Úúčňĺîňî╗šľŚšşëÚóćňččŃÇé2021ň╣┤´╝îňĄÜň«ÂňÉłŠłÉšöčšëęňşŽňůČňĆŞń╗ąŔÂůŔ┐ç10ń║┐šżÄňůâšÜäń╝░ňÇ╝ńŞŐňŞé´╝îňč║ňŤáš╗äňĚąšĘőňĚ▓ŠŞŚÚÇĆňł░šöčšëęšžĹňşŽšáöšęšÜäňÉäńެÚóćňčč´╝îDNAňÉłŠłÉŃÇüš╝ľŔżĹňĺîÚ珊ľ░š╝ľšáüŠşúňťĘňŞ«ňŐęŔžúňć│šľĹÚÜżŠŁéšŚçŃÇé
ňÉłŠłÉšöčšëęňşŽšÜ䊝ČŔ┤ĘŠś»Programming life´╝îŔ«ęš╗ćŔâ×ńŞ║ń║║š▒╗ňĚąńŻťń║žšöčŠâ│ŔŽüšÜäšëęŔ┤Ę´╝îšŤŞŠ»öń║Äń╝áš╗čňîľňşŽňÉłŠłÉ´╝îšöčšëęňÉłŠłÉňůĚŠťëňż«ň×őňîľŃÇüňĆ»ňż¬šÄ»ŃÇüŠŤ┤ň«ëňůĘšÜäšë╣šé╣ŃÇéňŤáŠşĄ´╝îňÉłŠłÉšöčšëęňşŽŠś»ńŞÇńެÔÇťňŁíÚĽ┐ÚŤ¬ňÄÜÔÇŁšÜäŔÁŤÚüôŃÇ銏«McKinseyš╗čŔ«í´╝îňůĘšÉâ60%ń╗ąńŞŐšÜäňîľňşŽŠľ╣Š│ĽňłÂÚÇášÜäń║žňôüÚâŻňĆ»ń╗ąÚÇÜŔ┐çšöčšëęŠŐÇŠť»ňłÂÚÇá´╝îÚóäŔ«íŠť¬ŠŁą10ňł░20ň╣┤´╝îňťĘňůÂňĚ▓š╗čŔ«íšÜä400ńŻÖńެň║öšöĘňť║ŠÖ»ÚçîÚŁó´╝îšöčšëęŠŐÇŠť»ň║öšöĘŠ»Ćň╣┤ň░暍┤ŠÄąňŞŽňŐĘ4ńŞçń║┐šżÄňůâšÜäš╗ĆŠÁÄńŻôÚçĆŃÇé
ňżłňĄÜń║║ŠŐŐňÉłŠłÉšöčšëęňşŽŠ»öńŻť21ńŞľš║¬šÜäÔÇťňĄęňĚąň╝ÇšëęÔÇŁ´╝îÚéúń╣łń╗Çń╣łŠś»ňÉłŠłÉšöčšëęňşŽšÜ䊝ČŔ┤Ę´╝čÚę▒ňŐĘń║žńŞÜŔ┐ŤňůąŔôČňőâňĆĹň▒ĽšÜäň║Ľň▒éÚÇ╗ŔżĹŠś»ń╗Çń╣ł´╝čń║žńŞÜÚôżńŞŐŠťëňô¬ń║ŤŠť║ń╝Ü´╝芝ȊľçÚ珚é╣Ŕžúňć│Ŕ┐ÖńŞëńŞ¬ÚŚ«ÚóśŃÇé
ňÉłŠłÉšöčšëęňşŽšÜ䊝ČŔ┤ĘŠś»ÔÇťš╝ľšáüšöčňĹŻÔÇŁ´╝îŔÇîšöčňĹŻšÜ䊝ČŔ┤Ęň░▒Šś»ńŞÇńެń┐íŠü»š│╗š╗čŃÇéňŽéŠ×ťŠŐŐšöčšëęńŻôšťőńŻťšö▒AGCTš╝ľšáüšÜäń┐íŠü»š│╗š╗č´╝îÚéúń╣łňÉłŠłÉšöčšëęň░▒Šś»ÚÇÜŔ┐çš╝ľšĘőń╗úšáü´╝îŔ«żŔ«íň╣ÂňłÂÚÇኾ░šëęšžŹ´╝îńŻ┐ňůÂŔâŻňĄčŔíîńŻ┐ŠŚóň«ÜňŐčŔâŻŃÇé
ň▒éň▒éŠőćŔžúŠŁąšťő´╝îňťĘšöčšëęń┐íŠü»š│╗š╗čńŞş´╝îš╗ćŔâ×ň░▒ňąŻŠ»öÔÇťŔ«íš«ŚŠť║ÔÇŁ´╝»ń┐ŁÚÜťš│╗š╗čŔ┐ÉŔíîšÜäšëęšÉćŔúůšŻ«´╝ŤATCGšó▒ňč║ň░▒ňąŻŠ»öÔÇť0101ń║îŔ┐ŤňłÂŔ┐Éš«ŚšČŽÔÇŁ´╝îŠŐŐń┐íŠü»ŔŻČňîľńŞ║ń║║š▒╗ňĆ»Ŕ»╗šÜäŔ»şŔĘÇŠîçń╗Ą´╝ŤDNAňłÖš▒╗Š»öńŞ║šíČšŤśŔÁĚňł░ňşśňéĘń╗úšáüšÜäńŻťšöĘ´╝ŤmRNAňąŻŠ»öWindowsš│╗š╗č´╝ŤŔŤőšÖŻŔ┤ĘňłÖńŞ║ň║öšöĘŔŻ»ń╗´╝ǚ╗łň«×šÄ░ńŞŹňÉîšÜäňŐčŔâŻŃÇéňťĘŠĽ┤ńެšöčšëęń┐íŠü»š│╗š╗čńŞş´╝îÚÇÜŔ┐çš╝ľšáüšöčňĹŻň«×šÄ░ňÉłŠłÉšöčšëę´╝îńŞőŠŞŞňłÖňĆ»ń╗ąň║öšöĘňł░šöčšëęňłÂÚÇáŃÇüňî╗šľŚňłÂŔŹ»ŃÇüšó│ńŞşňĺîŃÇüDNAňşśňéĘšşëňłŤŠľ░ň║öšöĘńŞşŃÇé

ňŤż šöčšëęňşŽš▒╗Š»öŔ«íš«ŚŠť║ňŽéńŻĽň«×šÄ░š╝ľšáüšöčňĹŻ
ňůÂň«×ňťĘń║║š▒╗ŠľçŠśÄšÜäÚĽ┐Š▓│ńŞş´╝îňťĘňů│š│╗ňł░Ŕç¬Ŕ║źňĹŻŔ┐ÉšÜäÚŚ«ÚóśńŞŐ´╝îń║║ń╗ČńŞÇšŤ┤ňťĘŔ┐ŻŠ▒éŔ┐ŁŔâîŔ笚äŠ│ĽňłÖŃÇéňĚąńŞÜÚŁęňĹŻń╣őňÉÄ´╝îň»╣ňîľšč│Ŕ⯊║ÉšÜäšľ»šőéŠÂłŔÇŚÚçŐŠöżń║ćňĄžÚçĆń║îŠ░žňîľšó│ŃÇüňłÂÚÇኌáň░ŻšÜäň×âňťżňĺîŠ▒íŠčô´╝îŔ┐Ťňůą21ńŞľš║¬ń╗ąŠŁą´╝îń║║ń╗ČńŞÇšŤ┤ňťĘŔ┐ŻŠ▒éŠëżňł░ńŞÇšžŹŠľ╣Š│ĽŔ«ęń║║š▒╗ŠľçŠśÄńŞÄŔ笚äš│╗š╗čÚ珊ľ░Ŕ׏ňÉł´╝îňÉłŠłÉšöčšëęňşŽŠü░ňąŻŔâŻňĄčňťĘŔ┐ÖńŞĄńެŠľ╣ňÉĹńŞŐňÉŠ╗íŔÂ│ń║║š▒╗šÜäڝNJ▒éŃÇé
2000ň╣┤-2003ň╣┤Šś»ňÉłŠłÉšöčšëęňşŽšÜäšÉćŔ«║ňłŤň╗║ŠŚÂŠťč´╝îňč║ňŤáš║┐ŔĚ»ňťĘń╗úŔ░óňĚąšĘőÚóćňččšÜäň║öšöĘŠś»Ŕ┐ÖńŞÇŠŚÂŠťčšÜäń╗úŔíĘ´╝î2002ň╣┤ń║║š▒╗ÚŽľŠČíňÉłŠłÉń║暌ůŠ»ĺ´╝î2003ň╣┤ňťĘňĄžŔéኣćŔĆîńŞşň«×šÄ░ń║ćÚŁĺŔĺ┐š┤áňëŹńŻôÚÇöňżäšÜäňĚąšĘőňîľŃÇé
2004ň╣┤-2007ň╣┤Šś»ňÉłŠłÉšöčšëęňşŽšÜäŠëęň╝ኝčňĺîňĆĹň▒ĽŠťč´╝îŔ┐ÖńŞÇڜŠ«Áňč║šíÇšáöšęÂň┐źÚÇčňĆĹň▒Ľ´╝îňĚąšĘőňîľšÉćň┐ÁŠŚąšŤŐŠĚ▒ňůą´╝î2004ň╣┤MITńŞżŔíîń║ćšČČńŞÇň▒ŐIGEM´╝łňŤŻÚÖůňč║ňŤáňĚąšĘőŠť║ňÖĘňĄžŔÁŤ´╝ë´╝îŔÖŻšäÂňÉłŠłÉšöčšëęňşŽšÜäň║öšöĘÚóćňččŠëęňĄž´╝îńŻćŠÇ╗ńŻôňĚąšĘőŠŐÇŠť»Ŕ┐Ťň▒Ľš╝ôŠůóŃÇé
2008ň╣┤-2013ň╣┤´╝îňč║ňŤáš╝ľŔżĹŠĽłšÄçňĄžň╣ůŠĆÉňŹç´╝░ŠŐÇŠť»ňĺîňĚąšĘőŠëőŠ«ÁŠÂîšÄ░´╝îň║öšöĘń╗Äšöčšëęňč║ňîľňşŽňôüŃÇüšöčšëęŔ⯊║ÉŠőôň▒ĽŔç│šľżšŚůŔ»ŐŠľşŃÇüŔŹ»šëęňĺîšľźŔőŚň╝ÇňĆĹŃÇüńŻťšëęŔé▓šžŹŃÇüšÄ»ňó⚍ŊÁőŃÇüšöčšëꊾ░ŠŁÉŠľÖšşëÚóćňččŃÇé2010ň╣┤5Šťł´╝îšżÄňŤŻšöčšëęňşŽň«ÂňůőŔÄ▒Šá╝┬ĚŠľçšë╣ň░ö(Craig Venter)ŠĽÖŠÄłňĺîń╗ľšÜäňŤóÚśčň░▒ňÉłŠłÉń║ćńŞÇšžŹňÄčŠáŞšöčšëęÔÇöÔÇöńŞŁšŐŠö»ňÄčńŻôŃÇé
2014ň╣┤ń╣őňÉÄ´╝îšöčšëęŠŐÇŠť»ńŞÄń┐íŠü»ŠĽ░ŠŹ«Ŕ׏ňÉłšÜäňĆĹň▒Ľšë╣šé╣ŠŤ┤ňŐኜĊśż´╝îňŹŐň»╝ńŻôňÉłŠłÉšöčšëęňşŽŃÇüňĚąšĘőšöčšëęňşŽšşëšÉćň┐ÁšŤŞš╗žŠĆÉňç║ŃÇé

ňŤż ňÉłŠłÉšöčšëęňşŽšÜäňĆĹň▒ĽňÄćňĆ▓
ń╗Äń║žńŞÜŔžćŔžĺŠŁąšťő´╝îňÉłŠłÉšöčšëęňşŽšÜäšČČńŞÇńެňŹüň╣┤´╝ł2000-2010´╝ëńŞ╗ŔŽüňĆĹň▒Ľń║ćňşŽšžĹšÉćŔ«║ňč║šíÇ´╝îń╗ÄšČČń║îńެňŹüň╣┤´╝ł2011-2020´╝ëň╝Çňžő´╝îÚÜĆšŁÇňĚąšĘőňîľšÉćň┐ÁŠŚąŠŞÉŠĚ▒ňůą´╝îŠŐÇŠť»ň╣│ňĆ░ňżŚňł░ÚçŹŔžć´╝îňĚąšĘőŠľ╣Š│ĽňĺîňĚąňůĚńŞŹŠľşšž»ŠĚÇ´╝îňÉłŠłÉšöčšëęňşŽń║žńŞÜňîľňŐáÚÇčŃÇé2015ň╣┤ń╗ąŠŁąňůĘšÉâňÉłŠłÉšöčšëęňşŽšŤŞňů│šÜäŔ«║ŠľçňĆĹŔíĘÚçĆňĹłšÄ░ÔÇťń║ĽňľĚň╝ĆÔÇŁňó×ÚĽ┐´╝î2020ň╣┤ńŞÇň╣┤ňůĘšÉ⚍Şňů│Ŕ«║ŠľçňĆĹŔíĘÚçĆŔÂůŔ┐ç2000š»ç´╝îŔÇîňůĘšÉâňÉłŠłÉšöčšëęňşŽń╝üńŞÜŔ׏ŔÁäń║őń╗ŠĽ░ÚçĆňĺîÚçĹÚóŁňŁçňłŤńŞőňÄćňĆ▓Ŕ«░ňŻĽ´╝îňłćňłźńŞ║189ŔÁĚňĺî56.6ń║┐šżÄňůâ

ňŤż Ŕ┐ĹňŹüň╣┤ňÉłŠłÉšöčšëęňşŽń║žňşŽšáöń║ĽňľĚň╝Ćňó×ÚĽ┐
ŠŚÂŔç│ń╗ŐŠŚą´╝îňÉłŠłÉšöčšëęňşŽňĚ▓š╗ĆŔÁ░ňç║ň«×Ú¬îň«Ą´╝îňťĘňÉäńެŠľ╣ňÉĹň«×šÄ░ń║žńŞÜňîľŃÇ銺úňŤáňŽéŠşĄ´╝îňşŽŠť»ňŞŽňĄ┤ń║║Šłľň░ćňć│ň«ÜňÉłŠłÉšöčšëęňşŽšÜäňĆĹň▒ĽŠľ╣ňÉĹŃÇéňŤŻňćůšÜäňÉłŠłÉšöčšëęňşŽń║žňşŽšáöňťłń╣čňĹłšÄ░ňç║ňşŽŠť»ŔâîŠÖ»ŔüÜÚŤćšÜäšë╣šé╣´╝öňŽéńŞşňŤŻšžĹňşŽÚÖóŠĚ▒ňť│ňůłŔ┐ŤŠŐÇŠť»šáöšęÂÚÖóŃÇüŠŞůňŹÄňĄžňşŽŃÇüńŞŐŠÁĚń║ĄÚÇÜňĄžňşŽŃÇüňîŚń║ČňĄžňşŽŃÇüńŞşňŤŻšžĹňşŽÚÖóŃÇüňŹŚń║ČňćťńŞÜňĄžňşŽŃÇüŔą┐ňîŚňĄžňşŽŃÇüńŞşňŤŻňćťńŞÜňĄžňşŽšşëňťĘňÉłŠłÉšöčšëęňşŽÚóćňč芻öŔżâš¬üňç║ŃÇé

ňŤż ňůĘšÉâňÉłŠłÉšöčšëęňşŽÚóćňćŤń║║šëęňů│š│╗Ŕ░▒
ňÉłŠłÉšöčšëęňşŽňŽéńŻĽň«×šÄ░š╝ľšáüšöčňĹŻňĹó´╝čń╗ąń║║ÚÇáŔéëÚżÖňĄ┤ňůČňĆŞImpossible FoodsńŞ║ńżő´╝îŔŽüš╗ĆňÄćňłŤŠäĆń║žšöčÔÇöÔÇöń║žňôüŔ«żŔ«íÔÇöÔÇöš╗ćŔâך╝ľšáüÔÇöÔÇöń║žňôüňĽćńŞÜňîľňçáńŞ¬ÚśÂŠ«ÁŃÇé
ÚŽľňůłšČČńŞÇńެšÄ»ŔŐ銜»ňłŤŠäĆń║žšöč´╝îń║║ń╗ČńŞ║ń╗Çń╣łÚťÇŔŽüń║║ÚÇáŔéë´╝čň╣ÂńŞŹŠś»ńŞ║ń║ćňŹĽš║»Š╗íŔÂ│š┤áÚúčńŞ╗ń╣ëŔÇůšÜäڝNJ▒é´╝îŔÇ»ń╝áš╗čŔéëš▒╗šöčń║žŠľ╣ň╝ĆňşśňťĘňżłňĄÜÚŚ«Úóś´╝îÚŁóńŞ┤ňĆ»Šîüš╗şŠÇžšÜäŠîĹŠłś´╝öňŽéšżÄňŤŻń║║ň»╣šëŤŔéëšÜäڝNJ▒éÚçĆŠ×üňĄž´╝łšżÄňŤŻŠ»Ćň╣┤ŠÂłŔ┤╣šÜäŠëÇŠťëŔéëš▒╗Úçî´╝îšóÄšëŤŔéëňŹáń║ć60%´╝ë´╝îÚą▓ňů╗šëŤň»╣ňťčňť░ŃÇüÚą▓ŠľÖŃÇüŠ░┤šÜäŠÂłŔÇŚÚçĆŠ×üňĄž´╝łšöčń║ž1ňůČŠľĄšëŤŔéë´╝îÚťÇŔŽüŠÂłŔÇŚ16ňůČŠľĄŔ░Ěšëęňĺî1.5ńŞçňŹçŠ░┤´╝ë´╝îšëŤŔéëšöčń║žň»╣šÄ»ňóâňŻ▒ňôŹń╣čňżłňĄž´╝łšÄ░ňťĘňůĘšÉ⊪ęň«ĄŠ░öńŻôŠÄĺŠöżńŞş´╝ë15%Šś»ňŤáńŞ║ňů╗šëŤÚÇኳɚÜä´╝ëŃÇé
šČČń║îńެšÄ»ŔŐéň░▒Šś»ń║žňôüŔ«żŔ«í´╝îń║║ÚÇášëŤŔéëŠÇÄń╣łňüÜ´╝čšëŤŔéëšÜ䊳ÉňłćńŞşÚÖĄń║ćŔŤőšÖŻŔ┤ĘŃÇüŔäéŔé¬ŃÇüŠ░┤ń╗ąňĄľ´╝îŔ┐śŠťëńŞÇńެÚçŹŔŽüŠłÉňłćÔÇťŔíÇš║óš┤áÔÇŁ´╝îŔ┐ÖŠś»ńŞÇšžŹňťĘŠëÇŠťëňŐĘŠĄŹšëęńŞşňĆĹšÄ░šÜäŔŤőšÖŻŔ┤Ę´╝»ŔÁőń║łŔéëń╗ąŠáçň┐ŚŠÇžňĹ│ÚüôšÜ䊳ÉňłćŃÇé
šČČńŞëńެšÄ»ŔŐéň░▒Šś»š╗ćŔâך╝ľšáü´╝îń╣芜»ňÉłŠłÉšöčšëęňşŽšÜäŠáŞň┐⊺ąÚ¬ĄŃÇéImpossible FoodsÚÇÜŔ┐çŠÁőŔ»ĽňÉäšžŹŔíÇš║óš┤áŔŤőšÖŻ´╝ǚ╗łňć│ň«ÜńŻ┐šöĘńŞÇšžŹňĄžŔ▒ćšöčń║žšÜäŔŤőšÖŻŔ┤ĘŔíÇš║óŔŤőšÖŻ´╝îŠŐŐŔíÇš║óš┤ášÜäňč║ňŤáňůâń╗ŠöżŔ┐ŤÚůÁŠ»ŹÚçî´╝îšöĘÚůÁŠ»ŹňÉłŠłÉ´╝îňćŹňŐáňůąŔéëÚą╝ń╣őńŞşŃÇéňťĘŠĽ┤ńެš╗ćŔâך╝ľšáüšÜäŔ┐çšĘőńŞş´╝îÚťÇŔŽüš╗ĆňÄćŔ«żŔ«í-Š×äň╗║-ŠÁőŔ»Ľ-ňşŽń╣ášÜäňż¬šÄ»´╝îń╗ąší«ň«ÜŠťÇńŻ│šÜäšöčšëęňÉłŠłÉÚÇöňżäŃÇé
šČČňŤŤńެšÄ»ŔŐéň░▒Šś»ń║žňôüňĽćńŞÜňîľ´╝îňŞŞńŻ┐šöĘšöčšëęňĆĹÚůÁŔ┐ŤŔíîšöčń║žŃÇ銻öňŽéImpossible FoodsňťĘňąąňůőňů░ň╗║šźőšöčń║žňč║ňť░´╝îÚâĘňłćšöčń║žňĄľňîůš╗ÖOSIÚŤćňŤóŃÇé

ňŤż ń╗ąImpossible FoodsńŞ║ńżő´╝îňÉłŠłÉšöčšëęňşŽňŽéńŻĽň«×šÄ░š╝ľšáüšöčňĹŻ
ń╗ÄńŞŐŔ┐░ń║║ÚÇáŔéëšÜäńżőňşÉńŞşňĆ»ń╗ąšťőňł░´╝îňÉłŠłÉšöčšëęňşŽŠÂëňĆŐńŞĄňĄžŔŽüš┤á´╝ÜńŞÇŠś»šöčšëęŠŐÇŠť»ŠťČŔ║ź´╝îń║»Ŕç¬ňŐĘňîľňĺ░ŠŹ«šžĹŠŐÇŃÇéšÄ░ňťĘňĄžňĄÜŠĽ░ňŞŞŠŞęňŞŞňÄőńŞőšÜ䊝늝║šëęŔ┤Ę´╝îňč║ŠťČÚâŻňĆ»ń╗ąŠő┐šöčšëꊣąňÉłŠłÉ´╝îňůÂńŞşšÜäňî║ňłźňťĘń║ÄŠś»ňÉŽŔâŻň«×šÄ░š╗ĆŠÁÄŠÇžŃÇé
Úę▒ňŐĘňÉłŠłÉšöčšëęňşŽňĄžňĆĹň▒ĽšÜäňÄčšÉ抝ëńŞëňĄžň║Ľň▒éÚÇ╗ŔżĹ´╝îňłćňłźŠś»ňĚąšĘőŠÇŁš╗┤ŃÇüŠĽ░ŠŹ«Úę▒ňŐĘŃÇüňŐáÚÇčŔ┐ŤňîľŃÇéŔÇîŔĚĘňşŽšžĹš╗ôňÉłňłÖŠś»ňÉłŠłÉšöčšëęňşŽšÜäÔÇťšüÁÚşéÔÇŁŃÇé
ňĚąšĘőŠÇŁš╗┤šÜäŠáŞň┐âň░▒Šś»ÔÇťŠĘíňŁŚňîľÔÇŁňĺîÔÇťŠáçňçćňîľÔÇŁŃÇ銳Ĺń╗ČňťĘň╝ÇňĄ┤ŠĆÉňł░Ŕ┐ç´╝îšöčňĹŻšÜ䊝ČŔ┤Ęň░▒Šś»ńŞÇńެšöčšëęń┐íŠü»š│╗š╗č´╝îÚéúń╣łŔ┐ÖňąŚš│╗š╗čńŞşšÜäšöčšëęňůâń╗Âň░▒Šś»ňůĚŠťëňŹĽńŞÇńŞöŠśÄší«ňŐčŔ⯚ÜäDNAšë犫Á´╝îňîůŠőČňÉ»ňŐĘňşÉŃÇüńŞşŠşóňşÉń╗ąňĆŐňůÂń╗ľňč║šíÇňŐčŔâŻň║ĆňłŚŃÇéŔ┐Öń║Ťšöčšëęňůâń╗š╗äňÉłŔúůÚůŹňŻóŠłÉšöčňîľňĆŹň║ö´╝îňćŹÚÇÜŔ┐çšöčšëęŔúůšŻ«Ŕ┐׊Ĺš╗䊳ɚÜäš║┐ŔĚ»ňĺîŔ░âŠÄžšŻĹš╗ťň░▒ňŻóŠłÉšöčšëęš│╗š╗čŃÇé
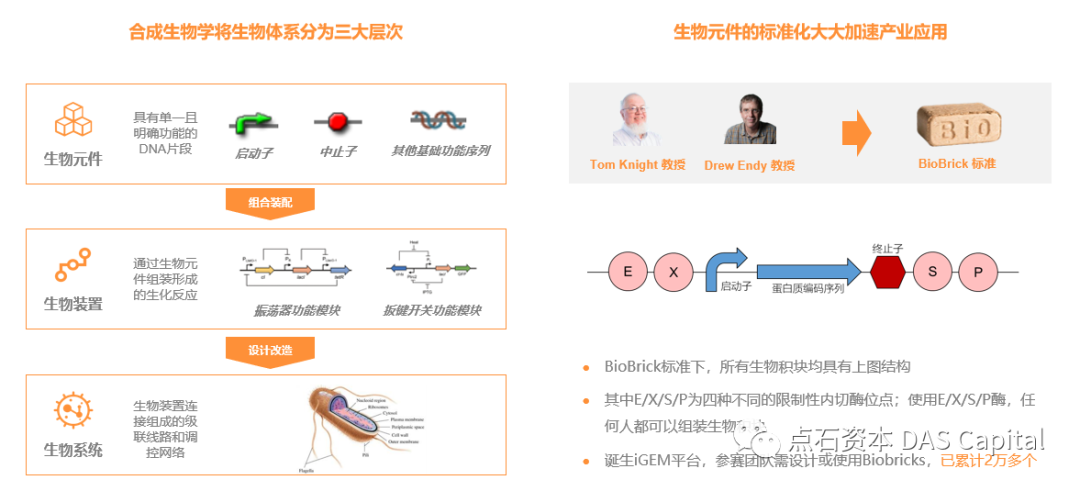
šöčšëęňůâń╗šÜäŠáçňçćňîľňĄžňĄžŠÄĘňŐĘń║ćňÉłŠłÉšöčšëęňşŽšÜäń║žńŞÜň║öšöĘŃÇéŔÇîŔžúňć│ŠáçňçćňîľÚŚ«ÚóśšÜ䊜»ňçáńŻŹňôłńŻŤňĺîMITšÜäňĚąšĘőňŞł´╝îń╗ąTom-KnightňĺîDrew EndyŠĽÖŠÄłńŞ║ń╗úŔíĘ´╝îń╗ľń╗Čň╗║šźőń║ćńŞÇńެŠĽ░ŠŹ«ň║ô´╝îňĆźÔÇťŠáçňçćšöčšëęňşŽš╗äń╗šÖ╗Ŕ«░ň║ô´╝łRegistry of Standard Biological Parts´╝ëÔÇŁŃÇéŔ┐ÖńެŠĽ░ŠŹ«ň║ôÚçëňÉäšžŹňÉäŠáĚšÜäňč║ňŤáňůâń╗´╝¬Ŕç│šŤ«ňëŹňĚ▓š╗Ćš┤»šž»ń║ć2ńŞçňĄÜńެŃÇéŔÇîńŞöŔ┐śŔ«żŔ«íń║ćńŞÇňąŚŠáçňçćšÜäš╗äŔúůŠÁüšĘő´╝îŔ┐ÖŠáĚň░▒ŔâŻňâĆŠő╝ń╣ÉÚźśńŞÇŠáĚŠő╝Ŕ┐Öń║Ťňč║ňŤáňůâń╗ÂŃÇé
ŠĘíňŁŚňîľňĺîŠáçňçćňîľňąáň«Üń║ćňÉłŠłÉšöčšëęňşŽšÜäňč║šíÇ´╝îń╣čŠÄĘňŐĘń║ćŔ┐ÖńެŔíîńŞÜšÜäŠĘ¬ňÉĹňłćňĚą´╝îńŞÇÚâĘňłćń║║ńŞôÚŚĘňÄ╗ŔžúŠ×Éňč║ňŤáňůâń╗šÜäňŐčŔ⯚╗žš╗şňüÜšžĹšáö´╝îňĆŽńŞÇÚâĘňłćń║║šöĘŔ┐Öń║Ťňč║ňŤáňůâń╗ÂňÄ╗š╗äŔúůŠľ░šÜäšöčňĹŻš│╗š╗čŃÇé
ňŤż ňÉłŠłÉšöčšëęňşŽň║Ľň▒éÚÇ╗ŔżĹń╣őÔÇťňĚąšĘőŠÇŁš╗┤ÔÇŁ
ňŤáńŞ║ňĚąšĘőŠÇŁš╗┤šÜäň╝Ľňůą´╝Ĺń╗ČňĆ»ń╗ąňâĆŠő╝ń╣ÉÚźśńŞÇŠáĚš╗äŔúůšöčňĹŻ´╝îńŻćŠś»ňŤáńŞ║ňÉłŠłÉšöčňĹŻň»╣š▓żňçćň║ŽšÜäŔŽüŠ▒éŠ×üÚźś´╝îň»╝Ŕç┤ŠťÇš╗łŠłÉňŐčšÄçňżłńŻÄŃÇéŔžúňć│Ŕ┐ÖńŞÇÚŚ«Ú󜊝ǚ«ÇňŹĽšÜäňŐ׊│Ľň░▒Šś»ňĄÜň«×Ú¬îŃÇüňĄÜŠÁőŔ»Ľ´╝îńŻćŔ┐ÖŠŚášľĹňŐáňĄžń║ćňĚąńŻťÚçĆŔÇîńŞöń╣čńŞŹňĄčš▓żňçćŃÇéŠâ│ŔŽüŠĆÉÚźśňÉłŠłÉšöčňĹŻšÜ䊳ÉňŐčšÄç´╝îň░▒ÚťÇŔŽüš╗ôňÉłŔ«íš«ŚŠť║šžĹňşŽ´╝îÚÇÜŔ┐犼░ŠŹ«Úę▒ňŐĘ´╝îšöĘŔ«íš«ŚŠť║ŠŁąŠĘíŠőčšöčňĹŻ´╝îŔ┐Öń╣芜»ňÉłŠłÉšöčšëęňşŽšÜäšČČń║îńެň║Ľň▒éÚÇ╗ŔżĹŃÇé
ňŽéŠ×ťŠłĹń╗ČŔŽüňÉłŠłÉšÜäšöčňĹŻňŐčŔâŻŔ笚䚼îŠá╣ŠťČŠ▓튝ë´╝îÚéúń╣łň░▒ÚťÇŔŽüňÉłŠłÉšöčšëęňşŽšÜäšČČńŞëńެň║Ľň▒éÚÇ╗ŔżĹ´╝îňŹ│ÔÇťňŐáÚÇčŔ┐ŤňîľÔÇŁŃÇéšöčšëęšÜäŔ┐ŤňîľÚťÇŔŽüńŞĄńެŠŁíń╗´╝îńŞÇŠś»ÔÇťňč║ňŤáš¬üňĆśÔÇŁ´╝îń║»ÔÇťŔ笚äÂÚÇëŠőęÔÇŁ´╝îŔÇîňŐáÚÇčŔ┐Ťňîľň░▒Šś»ń║║ńŞ║Šö╣ňĆśŔ┐ÖńŞĄńެŠŁíń╗ÂŃÇé
ň»╣ń║ÄňÉłŠłÉšöčšëęňşŽŔÇîŔĘÇ´╝îňŐáÚÇčŔ┐ŤňîľšÜ䊾╣Š│Ľń╗ÄÚÜĆŠť║ÚÇÉŠŞÉŔÁ░ňÉĹšÉćŠÇžŔ«żŔ«íŃÇéŔ┐çňÄ╗ŔÄĚňżŚŠľ░ŔĆîšžŹńŞ╗ŔŽüńżŁÚŁáŔ»▒ňĆśŔé▓šžŹ´╝îŔ┐ÖÚí╣ŠŐÇŠť»ŠťČŔ┤ĘńŞŐŠś»ňłÂÚÇáňĄžÚçĆÚÜĆŠť║š¬üňĆśňÉÄŔ┐ŤŔíîšşŤÚÇëŃÇéňąŻňĄäŠś»ŠôŹńŻťš«ÇňŹĽŃÇüÚÇéšöĘŔîâňŤ┤ň╣┐´╝îńŻćš╝║šé╣ňťĘń║Äš¬üňĆśÚÜĆŠť║ŠÇžÚźśŃÇüŔÇîńŞöš¬üňĆśÚóĹšÄçÚÜżń╗ąŠÄžňłÂŃÇé
ňÉÄŠŁąÚÇÉŠşąňĆĹň▒Ľňç║ń║ćš╗ĆňůŞń╗úŔ░óňĚąšĘőňĺîš│╗š╗čń╗úŔ░óňĚąšĘő´╝îŔ┐ÖńŞĄšžŹšşľšĽąň»╣ňĚ▓ščąňŐčŔ⯚Üäňč║ňŤášë犫ÁŔ┐ŤŔíîšÉćŠÇž/ňŹŐšÉćŠÇžšÜäŠö╣ÚÇáŃÇéšŤŞŠ»öÚÜĆŠť║š¬üňĆś´╝îšÉćŠÇž/ňŹŐšÉćŠÇžŔ«żŔ«íňĄžňĄžŠĆÉÚźśń║ćň╝ÇňĆĹŔĆîšžŹšÜ䊼łšÄç´╝îńŻćňĆŚÚÖÉń║ÄŠ×äň╗║ŃÇüŠÁőŔ»ĽÚÇÜÚçĆń╗ąňĆŐň»╣šöčšëęňč║ňŤáš╗äňŐčŔ⯚ÜäŔ«ĄŔ»ćŃÇé
ÚÜĆšŁÇŠĽ░ŠŹ«šžĹňşŽšÜäňĆĹň▒Ľ´╝îňč║ňŤáŠÁőň║ĆŠŐÇŠť»ŠĆÉńżŤń║ćŠÁĚÚçĆšÜäňč║ňŤáš╗äń┐íŠü»´╝îňłęšöĘňĄžÚçĆšÜäšöčšëęňşŽŠĽ░ŠŹ«´╝늝Ťň╗║šźőŔÁĚÔÇťň║ĆňłŚ-ňŐčŔâŻÔÇŁšÜäÚ╗Ĺš«▒ŠĘíň×ő´╝îń╗ÄŔÇîš╗Ľň╝ÇšÄ░ŠťëšÉćŔ«║šÜäščąŔ»ćšôÂÚół´╝îň«×šÄ░ňůĘňč║ňŤáš╗äň▒éÚŁóšÜäš╗ćŔâ×ňĚąšĘőŔ«żŔ«í´╝îň░抝¬ščąňŐčŔâŻňč║ňŤášÜäňĆĹšÄ░ňĺîŠö╣ÚÇášŤŞš╗ôňÉłŃÇé

ňŤż ňÉłŠłÉšöčšëęňşŽň║Ľň▒éÚÇ╗ŔżĹń╣őÔÇťňŐáÚÇčŔ┐ŤňîľÔÇŁ
Šľ░ŠŐÇŠť»šÜäŔ»×šöčŠÂîšÄ░ňç║ń║ćńŞÇŠë╣ńŞ║ňÉłŠłÉšöčšëęňşŽšŤŞňů│ňůČňĆŞŠĆÉńżŤňč║šíÇń║žňôüňĺŹňŐíšÜäňůČňĆŞ´╝îňŽéDNA/RNAŔ«żŔ«íňĺîňÉłŠłÉŃÇüšŤŞňů│ŔŻ»ń╗ÂňĺîšöčšëęńŻôŔ«żŔ«íńŞÄŔç¬ňŐĘňîľň╣│ňĆ░šşëÚóćňččšÜäňůČňĆŞŃÇéňůŞň×őń╗úŔíĘňŽéTwist´╝îňĚ▓š╗Ćň╗║šźőń║ćÚźśÚÇÜÚçĆŃÇüńŻÄŠłÉŠťČšÜ䊾░ńŞÇń╗úšíůňč║DNAňÉłŠłÉň╣│ňĆ░´╝îňĆ»ń╗ąňĄžÚçĆňÉłŠłÉÚźśŔ┤ĘÚçĆšÜäDNAšë犫ÁňĆŐňč║ňŤá´╝îšöĘń║ÄŔŹ»šëęň╝ÇňĆĹň«×Ú¬îňĺîńŞ┤ň║ŐŔ»ŐŠľşšşëňť║ŠÖ»ŃÇé
ŔÇîňťĘń║žńŞÜÚôżńŞşŠŞŞ´╝îń╣čŠÂîšÄ░ňç║ńŞÇń║ŤňťĘšöčšëęńŻôŔ«żŔ«íńŞÄŔç¬ňŐĘňîľň╣│ňĆ░ÚóćňččšÜäňůČňĆŞŃÇéń╗ľń╗ČňÇčňŐęŔŻ»ń╗ÂňĺîšíČń╗ÂŔžúňć│Šľ╣ŠíłšÜäš╗ôňÉł´╝îńŻ┐ňżŚń║║ń╗ČňĆ»ń╗ąň┐źÚÇčÚźśÚÇÜÚçĆňť░Ŕ«żŔ«íŃÇüŠ×äň╗║ŃÇüŠÁőŔ»Ľňĺîń╝śňîľšöčňĹŻńŻôŃÇéňůŞň×őń╗úŔíĘňŽéGinkgo Bioworks´╝îňůÂň«ÜńŻŹń║Äň╣│ňĆ░´╝┤ńŞôŠ│Ęń║ÄňÉłŠłÉšöčšëęňşŽń╗ĚňÇ╝ÚôżšÜäŔ«żŔ«íšÄ»ŔŐéŃÇéňůÂÚÇÜŔ┐çň╗║šźőŔžäŠĘíň║×ňĄžšÜäň«Ćňč║ňŤáš╗䊼░ŠŹ«ň║ô´╝îš╗śňłÂňč║ňŤáŃÇüŔŤőšÖŻŔ┤Ęňĺîń╗úŔ░óÚÇöňżä´╝îň╣ÂňÇčňŐęšöčšëęÚôŞÚÇáňÄéňĺ║ňÖĘňşŽń╣ኣąńŞŹŠľşňť░Ŕ┐ÉŔíîDBTLňĹĘŠťč´╝îń╗ąŔ«żŔ«íÚÇéňÉłšöčń║žšŤ«Šáçń║žšëęšÜäňż«šöčšëę´╝îńŞ║ńŞőŠŞŞňÉłńŻťń╝Öń╝┤ŠĆÉńżŤŠĘíňŁŚňîľšÜäŔžúňć│Šľ╣ŠíłŃÇé

ňŤż ňÉłŠłÉšöčšëęňşŽń║žńŞÜÚôż
ŔÇîňťĘńŞőŠŞŞ´╝îňÉłŠłÉšöčšëęňşŽňłÖňĆ»ń╗ąňťĘń║║š▒╗ŔíúÚúčńŻĆŔí╣Šľ╣ÚŁóÚŁóŔ┐ŤŔíîň║öšöĘň╝ÇňĆĹňĺîń║žňôüŔÉŻňť░ŃÇéňÉłŠłÉšöčšëęňşŽňťĘňî╗šľŚňüąň║ĚÚóćňččšÜäň║öšöĘň╣┐Š│Ť´╝îŠÂëňĆŐš╗ćŔâ×ňůŹšľźšľŚŠ│ĽŃÇüRNAŔŹ»šëęŃÇüňż«šöčŠÇüšľŚŠ│ĽŃÇüňč║ňŤáš╝ľŔżĹšŤŞňů│ň║öšöĘŃÇüńŻôňĄľŠúÇŠÁőŃÇüňî╗šľŚŔÇŚŠŁÉŃÇüŔŹ»šëꊳÉňłćšöčń║žňĺîňłÂŔŹ»šöĘÚůšşëňĄÜŠľ╣ÚŁóŃÇé
ń╗ÄńŞőŠŞŞň║öšöĘšÜäŔíîńŞÜšę║ÚŚ┤ŠŁąšťő´╝îňÉłŠłÉšöčšëęňşŽńŞőŠŞŞń║žňôüňŞéňť║2024ň╣┤ň░ćŔÂůŔ┐ç180ń║┐šżÄňůâ´╝îňůÂńŞşňî╗šľŚňüąň║ĚŠŁ┐ňŁŚňŹáŠŹ«ńŞ╗ň»╝ňť░ńŻŹ´╝îňŞéňť║šę║ÚŚ┤ŔÂůŔ┐ç50ń║┐šżÄÚçĹ´╝îCAGRŔżż19%ŃÇé

ňŤż ňÉłŠłÉšöčšëęňşŽňŞéňť║šę║ÚŚ┤
ňÉłŠłÉšöčšëęňşŽšÜäňĆĹň▒ĽŔŽüňŻĺňŐčń║ÄňĄÜšžŹŠŐÇŠť»šÜäŔ׏ňÉł´╝îňîůŠőČDNA/RNAŔ«żŔ«íňĺîňÉłŠłÉŃÇüňč║ňŤáŠÁőň║Ćňĺîňč║ňŤáš╝ľŔżĹšşëňč║šíÇŠŐÇŠť»´╝îń╗ąňĆŐńŞÇš│╗ňłŚńŞŹŠľşŠëęň▒ĽšÜäŠŐÇŠť»´╝îňŽéŔ«íš«ŚŃÇüšöčšëęń┐íŠü»ňşŽŃÇüňĄÜš╗äňşŽŃÇüń║║ňĚąŠÖ║ŔâŻŃÇüŔç¬ňŐĘňîľŃÇü3D šöčšëęŠëôňŹ░ňĺîš▓żň»ćňĆĹÚůÁšşëŃÇé
ňč║ňŤáš╝ľŔżĹŃÇüňč║ňŤáňÉłŠłÉŃÇüňč║ňŤáŠÁőň║Ć´╝îŔ┐Öń║ŤÚ⯊ś»ň║Ľň▒éšöčšëęŠŐÇŠť»ŃÇéŔ┐çňÄ╗ňŹüň╣┤ÚŚ┤´╝îń║║ń╗Čň»╣DNAŔ┐ŤŔíîŔ»╗ŃÇüŠö╣ŃÇüňćÖšÜäŠŐÇŠť»ňĆĹň▒ĽÚÇčň║ŽŔÂůŔ┐çń║ćŠĹęň░öň«Üňżő´╝îŠŐÇŠť»ŠłÉŠťČÚÖŹńŻÄń║ć1000ňÇŹń╗ąńŞŐŃÇéšÄ░ňťĘŔÇâÚ¬îšöčšëęŠŐÇŠť»ń╝üńŞÜšÜäŠáŞň┐âšź×ń║ëňŐŤńŞŹŠś»ŔâŻňÉŽň«×šÄ░šÜäÚŚ«Úóś´╝îŔÇ»Šś»ňÉŽŔâŻňüÜŠŤ┤ÚźśšÜäÚÇÜÚçĆ´╝îŔÄĚňżŚŠŤ┤ÚźśŔ┤ĘÚçĆšÜ䊼░ŠŹ«´╝îŔ┐Öň░▒ÚťÇŔŽüňÇčňŐęŔç¬ňŐĘňîľňĺ░ŠŹ«šžĹňşŽŃÇé

ňŤż ŠŐÇŠť»Š×äň╗║ŠłÉŠťČÚÖŹńŻÄ´╝łšÄçŠĆÉňŹç
ňĆŽňĄľ´╝îň»╣š╗ĆŠÁÄŠĽłšöĘšÜäŔ┐ŻŠ▒éń╣芜»Úę▒ňŐĘňÉłŠłÉšöčšëęňşŽňĄžňĆĹň▒ĽšÜäńŞ╗ŔŽüňÄčňŤáŃÇéń╗ąÚŁĺŔĺ┐š┤áńŞ║ńżő´╝îÚŁĺŔĺ┐š┤ኜ»Š▓╗šľŚšľčšľżšÜäÚçŹŔŽüŔŹ»šëę´╝îň▒áňĹŽňĹŽňŤáňĆĹšÄ░ÚŁĺŔĺ┐š┤áňťĘ2015ň╣┤ŔÄĚňżŚŔ»║Ŕ┤Łň░öšöčšÉ抳ľňî╗ňşŽňąľŃÇéŔÇîń╝áš╗čšÜäÚŁĺŔĺ┐š┤áŔÄĚňżŚŠľ╣Š│ĽÚťÇŔŽüń╗ÄšžŹŠĄŹšÜäÚŁĺŔĺ┐ńŞşŠĆÉňĆľ´╝îňŹášöĘňĄžÚçĆšÜäňťčňť░´╝îń║žÚçĆňĆŚŠ░öňÇÖšşëňĄľÚâĘňŤáš┤ášÜäňŻ▒ňôŹńŞŹšĘ│ň«Ü´╝ɊťČÚźśŠśé´╝łšżÄňůâš║ž´╝ëŃÇéŔÇîAmyrisšÜäňłŤňžőń║║Jay D KeaslingŠĽÖŠÄłňłęšöĘňÉłŠłÉšöčšëęňşŽŠľ╣Š│Ľš╝ľšĘőÚůÁŠ»ŹňÉłŠłÉÚŁĺŔĺ┐š┤á´╝îň╣Âň«×šÄ░ňĚąńŞÜňîľšöčń║ž´╝îńŞŹňĆŚŠ░öňÇÖšşëňĄľÚâĘňŤáš┤áňŻ▒ňôŹ´╝îń║žÚçĆňĄž´╝ɊťČńŻÄ´╝łšżÄňłćš║ž´╝ë´╝îŔŐéš║ŽňĄžÚçĆňťčňť░ŃÇé
ňÉłŠłÉšöčšëęňşŽŠśżšÄ░ňç║šÜäňĚĘňĄžšÜäESGń╗ĚňÇ╝ňĚ▓š╗Ćň╝ĽŔÁĚňůĘšÉâňÉäňŤŻšÜäňů│Š│ĘŃÇéOECDň»╣6ńެňĆĹŔżżňŤŻň«ÂŔ┐ŤŔíîňłćŠ×ÉšÜäš╗ôŠ×ťŔíĘŠśÄ´╝ÜšöčšëęňłÂÚÇáŠŐÇŠť»šÜäň║öšöĘňĆ»ń╗ąÚÖŹńŻÄňĚąńŞÜŔâŻŔÇŚ15-80%´╝îňÄ芾֊³ŔÇŚ35-75%´╝îšę║Š░öŠ▒íŠčô50-90%´╝îŠ░┤Š▒íŠčô33-80%´╝îšöčń║žŠłÉŠťČÚÖŹńŻÄ9-90%ŃÇéńŞľšĽîňč║ňŤáňžöňĹśń╝ÜÚóäŠÁő´╝îňł░2030ň╣┤´╝îňĚąńŞÜšöčšëęŠŐÇŠť»Š»Ćň╣┤ň░ćňĆ»ÚÖŹńŻÄ25ń║┐ňÉĘšÜäń║îŠ░žňîľšó│ŠÄĺŠöżŃÇé
Ŕ┐Ĺň╣┤ŠŁąňÉłŠłÉšöčšëęňşŽńŞŹŠľşŔÄĚňżŚŠö┐šşľŠö»Šîü´╝îňťĘÔÇťňŹüňŤŤń║öÔÇŁŔžäňłĺńŞş´╝îňÉłŠłÉšöčšëęňşŽň║öšöĘŔóźňłŚňůąÔÇťňĆĹň▒Ľňú«ňĄžŠłśšĽąŠÇžŠľ░ňů┤ń║žńŞÜÔÇŁ´╝îÔÇťňŐáň┐źňĆĹň▒Ľšöčšëęňî╗ŔŹ»ŃÇüšöčšëęŔé▓šžŹŃÇüšöčšëꊣɊľÖŃÇüšöčšëęŔ⯊║Éšşëń║žńŞÜ´╝îňüÜňĄžňüÜň╝║šöčšëęš╗ĆŠÁÄÔÇŁŃÇéňÉäňť░ń╣čšŤŞš╗žňç║ňĆ░ń║žńŞÜŠëŠîüŠö┐šşľ´╝îňĄęŠ┤ąň╗║Ŕ«żňŤŻň«ÂňÉłŠłÉšöčšëęŠŐÇŠť»ňłŤŠľ░ńŞşň┐â´╝îŠëôÚÇáÔÇťš╗ćŔâ×Ŕ░ĚÔÇŁŃÇüÔÇťšöčšëęňłÂÚÇáŔ░ĚÔÇŁšşëšë╣Ŕë▓ňŤşňî║´╝Ťň╣┐ńŞťň╗║šźőňÉłŠłÉšöčšëęšáöšęÂÚçŹňĄžšžĹŠŐÇňč║šíÇŔ«żŠľŻ´╝îŠĚ▒ňť│ňů늜ĚžĹňşŽňčÄÚ珚é╣ňĆĹň▒ĽňÉłŠłÉšöčšëęňşŽšşëš╗ćňłćÚóćňčč´╝îŠö»ŠîüňÉłŠłÉšöčšëęňłŤŠľ░Úôżń║žńŞÜÚôżŔ׏ňÉł´╝Ťň▒▒Ŕą┐ŠëôÚÇáňůĘňŤŻÚóćňůłšÜäšöčšëęňč║Šľ░ŠŁÉŠľÖń║žńŞÜňłÂÚÇáňč║ňť░´╝îÚś│ŠŤ▓šëçňî║Ú珚é╣ňĆĹň▒ĽňÉłŠłÉšöčšëęňůĘń║žńŞÜÚôżŃÇé
ÚÜĆšŁÇ2021ň╣┤ňĄÜň«ÂňÉłŠłÉšöčšëęňşŽňůČňĆŞňťĘšżÄŔéíńŞŐňŞé´╝îňŤŻňćůŠŐĽŔÁ䚼îń╣čŠÄÇŔÁĚń║ćńŞÇŔéíÔÇťŠŐĽŔÁäšâşÔÇŁ´╝îńŻćŠşúňŽéňĚ┤ŔĆ▓šë╣ŠëÇŔ»┤´╝îÔÇťňƬŠťëňŻôŠŻ«Š░┤ÚÇÇňÄ╗ŠŚÂ´╝îńŻáŠëŹń╝ÜščąÚüôŔ░üńŞÇšŤ┤ňťĘŔúŞŠ││ÔÇŁŃÇ銝ȊľçŠś»ŠłĹń╗ČňÉłŠłÉšöčšëęňşŽš│╗ňłŚŔíîšáöšÜäńŞŐš»ç´╝îńŞőńŞÇš»çŠľçšźáńŞş´╝Ĺń╗Čň░ćÚ珚é╣ňłćŠ×ÉňŽéńŻĽňÄ╗ń╝¬ňşśšťčÚë┤ňłźšťčŠşúšÜäňÉłŠłÉšöčšëęňşŽňůČňĆŞ´╝čń╗ąňĆŐňťĘŔ┐ÖŔéíŠÁ¬ŠŻ«ńŞş´╝îńŞŐŠŞŞń╝üńŞÜňŽéńŻĽŔÁőŔ⯊Ľ┤ńެšöčŠÇü´╝čńŞşŠŞŞň╣│ňĆ░ň×őń╝üńŞÜňł░ň║ĽňüÜň»╣ń║ćń╗Çń╣łŔâŻňĄčŔä▒ÚóľŔÇîňç║´╝čń╗ąňĆŐÚÇÜŔ┐çňô¬ń║Ťš╗┤ň║ŽŠŁąšşŤÚÇëń╝śŔ┤ĘšÜäńŞőŠŞŞÚí╣šŤ«´╝芼ČŔ»ĚŠťčňżůŃÇé
ňůŹŔ┤úňú░ŠśÄ
šŤŞňů│ňćůň«╣ňč║ń║ÄňĚ▓ňůČň╝ÇšÜäŔÁ䊾֊łľń┐íŠü»Šĺ░ňćÖ´╝îńŻćŠťČňůČňĆŞńŞŹń┐ŁŔ»üŔ»ąšşëń┐íŠü»ňĆŐŔÁ䊾֚Üäň«îŠĽ┤ŠÇžŃÇüňçćší«ŠÇž´╝îŠëÇňÉźń┐íŠü»ňĆŐŔÁ䊾Öń┐ŁŠîüňťĘŠťÇŠľ░šŐŠÇüŃÇéňÉ´╝ČňůČňĆŞŠťëŠŁâň»╣ŠťČŠŐąňĹŐŠëÇňÉźń┐íŠü»ňťĘńŞŹňĆĹňç║ÚÇÜščąšÜäŠâůňŻóńŞőňüÜňç║ń┐«Šö╣´╝îÚśůŔ»╗ŔÇůň║öňŻôŔç¬Ŕíîňů│Š│ĘšŤŞň║öšÜ䊍┤Šľ░Šłľń┐«Šö╣ŃÇé
ňťĘń╗╗ńŻĽŠâůňćÁńŞő´╝Ț»çŠľçšźáńŞşšÜäń┐íŠü»ŠłľŠëÇŔíĘŔ┐░šÜäŠäĆŔžüňŁçńŞŹŠ×䊳Éň»╣ń╗╗ńŻĽń║║šÜäŠŐĽŔÁäň╗║Ŕ««´╝áŔ«║Šś»ňÉŽňĚ▓š╗ĆŠśÄšĄ║ŠłľŠÜŚšĄ║´╝ȊչňĹŐńŞŹŔâŻńŻťńŞ║Úüôń╣ëšÜäŃÇüŔ┤úń╗╗šÜäňĺîŠ│ĽňżőšÜäńżŁŠŹ«ŠłľŔÇůňçşŔ»üŃÇéňťĘń╗╗ńŻĽŠâůňćÁńŞő´╝ČňůČňĆŞń║ŽńŞŹň»╣ń╗╗ńŻĽń║║ňŤáńŻ┐šöĘŠťČŠľçšźáńŞşšÜäń╗╗ńŻĽňćůň«╣ŠëÇň╝ĽŔç┤šÜäń╗╗ńŻĽŠŹčňĄ▒Ŕ┤čń╗╗ńŻĽŔ┤úń╗╗ŃÇ銝Ȋľçšźáń╗ůńŞ║ŠťČňůČňĆŞŠëÇŠťë´╝¬š╗Ćń║őňůłń╣ŽÚŁóŔ«ŞňĆ»´╝îń╗╗ńŻĽŠť║Š×äňĺîńެń║║ńŞŹňżŚń╗ąń╗╗ńŻĽňŻóň╝Ćš┐╗šëłŃÇüňĄŹňłÂŃÇüňĆĹŔíĘŃÇüŔŻČňĆĹŠłľň╝ĽšöĘŠťČŠŐąňĹŐšÜäń╗╗ńŻĽÚâĘňłćŃÇé