

21ńŞľš║¬ń╗ąŠŁą´╝îňĄÜšžŹń╝áŠčôšŚůÚóĹňĆĹ´╝îń╗Ä03ň╣┤šÜäÚŁ×ňůŞň×őŔé║šéÄŃÇüňÉäšžŹńŞŹňÉîń║Üň×őšÜäŠÁüŠäčŃÇüڣ׊┤▓šÜäňčâňŹÜŠő뚌ůŠ»ĺŃÇüňł░ŔéćŔÖÉňůĘšÉâšÜ䊾░ňćáŔé║šéÄ´╝áńŞÇńŞŹŠś»ňŻ▒ňôŹňĚĘňĄž´╝îŔ┐çňÄ╗ŃÇüšÄ░ňťĘŃÇüň░抣ąÚ⯊ŚÂňł╗ŠîĹŠłśšŁÇń║║š▒╗šÜäňůČňů▒ňŹźšöčńŻôš│╗ŃÇéÚÜĆšŁÇšžĹňşŽŠŐÇŠť»šÜäŔ┐ŤŠşą´╝îń╗ąqPCRŠŐÇŠť»ńŞ║ńŞ╗šÜäňłćňşÉŔ»ŐŠľşń╣čňżŚňł░ÚĽ┐ŔÂ│šÜäňĆĹň▒Ľ´╝îňłćňşÉŔ»ŐŠľşňĚ▓š╗ĆŠłÉńŞ║ń║ćńŻôňĄľŔ»ŐŠľşńŞşňó×ÚÇ芝Çň┐źšÜäŔíîńŞÜŃÇé

21ńŞľš║¬ń╗ąŠŁą´╝îń╝áŠčôšŚůÚŚ┤ŠľşŠÇžšłćňĆĹ´╝îń╝┤ÚÜĆšŁÇňůĘšÉâńŞÇńŻôňîľ´╝îň»╝Ŕç┤šľżšŚůÚś▓ŠÄžÚŁóńŞ┤Š×üňĄžňÄőňŐŤŃÇé2019ň╣┤ňůĘšÉ⊾░ňćášľźŠâůšłćňĆĹ´╝îňŞŽŠŁąń║押┤ńެňłćňşÉŠúÇŠÁőŔíîńŞÜšÜ䊾░ňĆśňîľ´╝ÜńŞÇŠś»Ŕ»ŐšľŚńŻôš│╗ń╗Äń╝áš╗čšÜäń╗ąňî╗ÚÖóńŞ║ńŞşň┐âňĆśńŞ║ňÄ╗ńŞşň┐âňîľ´╝Ťń║»ŠúÇŠÁőňť║ŠÖ»ń╗Äňî╗ÚÖóŠúÇŠÁőňĆśŠłÉšĄżňî║Šłľň«ÂšöĘŠúÇŠÁő´╝ŤńŞëŠś»ň»╣ŠúÇŠÁőŠŐÇŠť»ŠĆÉňç║ŠŤ┤ÚźśšÜäŔŽüŠ▒é´╝îŔžäŠĘíňîľŃÇüŔç¬ňŐĘňîľŃÇüň┐źÚÇčňłÉńŞ║ŔÂőňŐ┐ŃÇé

ńŞ║ń║ćň║öň»╣ňĄžÚçĆšÜäŠúÇŠÁőڝNJ▒é´╝îňÉäšžŹŠúÇŠÁőŠľ╣Š│ĽŃÇüŠúÇŠÁőŔ«żňĄçń╣芜»ň║öŠŚÂŔÇîšöčŃÇéń╗ÄŠúÇŠÁőŠľ╣Š│ĽŠŁąŔ»┤´╝îÚÖĄqPCRńŻťńŞ║COVIDšÜäŠúÇŠÁőÚçĹŠáçňçćňĄľ´╝îŠŐŚňÄčŠúÇŠÁőŃÇüšşëŠŞęŠëęňó׊úÇŠÁőŃÇüCRISPRŠúÇŠÁőšşëŠúÇŠÁőŠľ╣Š│Ľń╣čÚÇÜŔ┐çň┐źÚÇčšáöňĆĹšöĘń║ÄŠúÇŠÁő´╝Ťń╗ÄŠúÇŠÁőŔ«żňĄçŔÇîŔĘÇ´╝îň«×Ú¬îň«ĄŔç¬ňŐĘňîľŃÇüŠúÇŠÁőŔç¬ňŐĘňîľšşëŔíîńŞÜňĆĹň▒ĽňŽéšüźňŽéŔŹ╝´╝îňŽéRochešÜäŠáŞÚůŞŠúÇŠÁőńŞÇńŻôŠť║Cobas 6800ňĚ▓š╗ĆŠłÉńŞ║PCRńŞÇńŻôŠť║šÜäŠá犣ć´╝îňö«ń╗Ěš║Ž500ńŞçňůâ´╝ŤŔÖŻšäŠłÉŠťČňó×ňŐá´╝îńŻćŠ×üňĄžňť░ÚÖŹńŻÄń║ćŠ▒íŠčôšÜäÚúÄÚÖęŔĚčň»╣ń║║ňĹśšÜäŔŽüŠ▒éŃÇéňŻôšä´╝îšö▒ń║ÄňůĘŔç¬ňŐĘńŞÇńŻôŠť║Ŕ«żňĄçŠłÉŠťČŔżâÚźś´╝îńŞŹň░ĹŠť║Š×äÚ⯊ś»ÚççňĆľŔç¬ňŐĘšÜäŠáŞÚůŞŠĆÉňĆľń╗¬+ň«×ŠŚÂŔŹžňůëň«ÜÚçĆPCRňłćŠ×Éń╗¬šÜäŠúÇŠÁőŠľ╣ň╝ĆŠŁąÚÖŹńŻÄń║║ňŐŤŠłÉŠťČ´╝îŠĆÉÚźśŠúÇŠÁőŠĽłšÄçŃÇé

Cobas 6800ńŞÇńŻôŠť║
qPCRŠś»ŠáŞÚůŞŠúÇŠÁőŠťÇňŞŞŔžüšÜäńŻ┐šöĘŠľ╣Š│Ľ´╝îń╣芜»ŠúÇÚ¬îšÜäÚçĹŠáçňçćŃÇéšäÂŔÇîňŤŻňćůňĄžŔîâňŤ┤šÜäšşŤŠčą´╝îň»╝Ŕç┤ŠáĚŠťČÚçĆÚŁ×ňŞŞňĄž´╝îň»╣ń║ÄŠúÇŠÁőŠŚÂÚŚ┤ŔŽüŠ▒éń╣芻öŔżâÚźśŃÇéŠŐŚňÄčŠúÇŠÁőŃÇüšşëŠŞęŠëęňó׊úÇŠÁőšşëń║žňôüń╣čŔóźňĄžÚçĆšáöňĆĹň╣ÂŔóźň║öšöĘń║ÄňŞéňť║ŃÇéń╗ąŠŐŚňÄčŠúÇŠÁőńŞ║ńżő´╝¬Ŕç│2022ň╣┤4Šťł´╝îňŤŻňćůNMPAňů▒Šë╣ňçćń║ć23ŠČżŠŐŚňÄčŠúÇŠÁőń║žňôü´╝îńŞöň»╣Š»öŠŐŚňÄčŠúÇŠÁőšÜäš╗ôŠ×ť´╝îńŞÄňŤŻňĄľšÜäŠŐŚňÄčŠúÇŠÁőń║žňôüŔâŻňĄčŔżżňł░ńŞÇŔç┤šÜäŠúÇÚ¬îŠÇžŔâŻŃÇéňťĘ2022ň╣┤ńŞŐŠÁĚŠťČŠČíšľźŠâůńŞş´╝îňĄžÚçĆšÜäŠŐŚňÄčŠúÇŠÁőŔ»Ľňë隍ĺŔóźšöĘń║ÄŠáŞÚůŞŠúÇŠÁőň돚ÜäŔ笊łĹšşŤŠčąŃÇéŠá╣ŠŹ«ÚöÇňö«ŠâůňćÁ´╝îŠŐŚňÄčŠúÇŠÁőŔ»Ľňë隍ĺňťĘŠÁĚňĄľňŞéňť║ňŹáŠŹ«ňĄžÚçĆŔžäŠĘí´╝î2021ň╣┤ŠłĹňŤŻšÜ䊾░ňćáŠŐŚňÄčŠúÇŠÁőŔ»Ľňë隍ĺŠÁĚňĄľÚöÇňö«ŔžäŠĘíŔÂů700ń║┐ňůâŃÇé
šşëŠŞęŠëęňó׊úÇŠÁőŠŐÇŠť»ń╣芜»ňťĘŠľ░ňćášľźŠâůń╣őňÉÄňżŚňł░Š×üňĄžšÜäňĆĹň▒ĽŃÇéń╗ÄFDAŃÇüCEšşëŔÄĚŠë╣ŠâůňćÁŠŁąšťő´╝î2021ň╣┤šżÄňŤŻŠë╣ňçćń║ć3ŠČżň«ÂšöĘňłćňşÉŠúÇŠÁőšÜäń║žňôü´╝îńŞ╗ŔŽüÚ⯊ś»ÚççňĆľšşëŠŞęŠëęňó׊úÇŠÁőŠŐÇŠť»´╝îňĆ»ňťĘ30ňłćÚĺč-1ńެň░ĆŠŚÂňćůňżŚňł░ŠúÇÚ¬îš╗ôŠ×ťŃÇéňŤŻňćůń╣芝ëňŽéń╝śŠÇŁŔżżŃÇüŠÖ«ńŞľňłęňŹÄŃÇüšâşŠÖ»šöčšëęšşëňůČňĆŞšÜäňłćňşÉPOCTń║žňôüŔÄĚňżŚCEŔ«ĄŔ»ü´╝îň╣Âň╝ÇňžőÚöÇňö«ŃÇé
CRISPRŠúÇŠÁőŠŐÇŠť»Ŕ┐ĹńŞĄň╣┤ŠŁąń╣čňťĘŠľ░ňćáÚóćňččň╝éň捚¬üŔÁĚ´╝îňůĚňĄçň║Ľň▒éŠŐÇŠť»šÜäProof diagnostics 2022ň╣┤4ŠťłňĚ▓š╗Ćň«îŠłÉňč║ń║ÄCRISPRŠúÇŠÁőŠŐÇŠť»šÜ䊾░ňćáŠáŞÚůŞŠúÇŠÁőń║žňôüšáöňĆĹň╣ŠĆÉń║ĄFDAšÜäEUAšö│Ŕ»Ěň«íŠë╣´╝늝ŤňťĘń╗Őň╣┤3ňşúň║ŽŔÄĚňżŚŠë╣ňçćň╣Šşúň╝Ćň║öšöĘŃÇé
ňťĘŠľ░ňćášľźŠâůń╗ąň돴╝îň«ÂšöĘŠúÇŠÁőŠĽ┤ńŻôňĆĹň▒ĽÚâŻńŞŹňĄ¬ňůůňłćŃÇéń╝áš╗čšÜäň«ÂšöĘŠúÇŠÁőńŞ╗ŔŽüÚâŻŔüÜšäŽňťĘŔé┐šśĄšşŤŠčąŃÇüŠůóŠÇžšŚůšŤĹŠÁőŃÇüŠÇžń╝áŠĺşšľżšŚůšşŤŠčąšşëÚóćňččŃÇ銻öňŽéš╗ôšŤ┤ŔéášÖîšÜäšşŤŠčą´╝îšöĘŠłĚŔç¬ÚççŠáĚňÉÄň░ćŠáĚŠťČšŤ┤ŠÄąň»äňŤ×´╝îšČČńŞëŠľ╣ňî╗ňşŽŠúÇÚ¬îńŞşň┐âÚççňĆľŠÁőň║ĆšşëŠŐÇŠť»ň»╣ŠáĚŠťČŔ┐ŤŔíîŠúÇŠÁőňÉÄň░ćš╗ôŠ×ťšŤ┤ŠÄąňĆŹÚŽłš╗ÖšöĘŠłĚ´╝îŔ┐ÖšžŹŠľ╣ň╝ĆńŞ╗ŔŽüÚĺłň»╣Ŕé┐šśĄšşŤŠčąŃÇüHPVšŚůŠ»ĺŠúÇŠÁőšşë´╝ŤŠůóŠÇžšŚůšŤĹŠÁőÚóćňččňŽéš│ľň░┐šŚůŠéúŔÇůšşëÚççňĆľň▒ůň«ÂŔíÇš│ľŠúÇŠÁő´╝ŤŠÇžń╝áŠĺşšľżšŚůšşŤŠčąňŽéHIVŃÇüŠóůŠ»ĺšÜäšşŤŠčą´╝îšö▒ń║ÄŔ┐Öš▒╗šľżšŚůÚÜÉšžüŠÇžŠ»öŔżâň╝║´╝îňŤáŠşĄňťĘňŤŻňćůń╣čňůĚňĄçńŞÇň«ÜšÜäňĆĹň▒ĽŔžäŠĘí´╝«ŠéëHIVŠúÇŠÁőŔ»Ľňë隍ĺňťĘšŻĹńŞŐ1ň░ĆŠŚÂŔç│ň░ĹňŹľňç║500šŤĺŃÇéň«ÂšöĘňŞéňť║ń║čÚťÇňçćší«ŠÇžÚźśŃÇüŠúÇŠÁőŠĽłšÄçÚźśšÜäŠúÇŠÁőŠľ╣ň╝ĆŃÇé
ňżłňĄÜňŤŻň«ÂŔ┐čŔ┐čńŞŹŠĽóŠöżŠŁżň»╣ň▒ůň«ÂŔ笊úÇń║žňôüšÜäÚÖÉňłÂ´╝îŠúÇŠÁőŠĽ░ŠŹ«šÜäš«íšÉćńż┐Šś»ńŞÇńެÚçŹŔŽüňÄčňŤáŃÇéšë╣ňłźŠś»ňâĆŠľ░ňćáŔ┐ÖšžŹňůĚŠťëÚźśń╝áŠčôŠÇžšÜäšľżšŚů´╝îňŻôŠÂłŔ┤╣ŔÇůŔç¬ŔíîŠúÇŠÁőňç║Úś│ŠÇžŔÇîš×ĺŠŐąš╗ôŠ×ťŠŚÂ´╝îňÉÄš╗şňĆ»ŔâŻń╝ÜŔ폚öčňç║šÜäńŞÇš│╗ňłŚÚŚ«ÚóśŃÇ銾░ňćášÜäšłćňĆĹň»╝Ŕç┤ňĄžŔžäŠĘíšÜäÚççŠáĚŃÇüń║║šżĄŔüÜÚŤć´╝îňÉÂňŤŻňćůÚççŠáĚń║║ňĹśŠ×üň║ŽšĘÇš╝║´╝îÚççŠáĚňĹśń╣芳ÉńŞ║ń║ćńŞÇńެňĚąšžŹ´╝ᚾĹňŐáŠĚ▒ń║ćňĄžň«Âň»╣ň«Âň║şŔ笊úÇń║žňôüšÜäšÉćŔžú´╝îń╣čňŐáň┐źń║ćÚâĘňłćňŤŻň«ÂšÜäň▒ůň«ÂŠúÇŠÁőŔÂőňŐ┐ŃÇé2020ň╣┤ň║Ľ´╝îňŤŻň«ÂŔŹ»šŤĹň▒ÇňĆĹňŞâŃÇŐň«ÂšöĘńŻôňĄľŔ»ŐŠľşňî╗šľŚňÖĘŠó░Š│ĘňćîŠŐÇŠť»ň«íŠčąŠîçň»╝ňÄčňłÖŃÇő´╝îń╣čŠäĆňĹ│šŁÇň«ÂšöĘńŻôňĄľŔ»ŐŠľşŔ┐ŤňůąńŞÇńެŠľ░ڜŠ«ÁŃÇé
ňťĘňĆĹŔżżňŤŻň«ÂňŽéšżÄňŤŻšÜäň«ÂšöĘňłćňşÉŠúÇŠÁőń╣čňżŚňł░ň┐źÚÇčšÜäňĆĹň▒ĽŃÇéŠá╣ŠŹ«šżÄňŤŻ2021ň╣┤ŔÄĚŠë╣šÜäň«ÂšöĘOTCšÜ䊾░ňćáŠúÇŠÁőń║žňôüń╗ąňĆŐšżÄňŤŻňůĘňŤŻšÜäŠúÇŠÁőÚçĆ´╝îňĆ»ń╗ąňĆĹšÄ░2021ň╣┤ŠŐŚňÄčŠúÇŠÁőňŹáŠ»öŔżżňł░ŠëÇŠťëŠúÇŠÁőňŹáŠ»öšÜä15%´╝îň«ÂšöĘŠľ░ňćáňłćňşÉŠúÇŠÁőŔ»Ľňë隍ĺÚöÇňö«ŔÂů1000ńŞçń╗´╝îňŹáŠëÇŠťëŠľ░ňćáŠúÇŠÁőšÜä5%ŃÇé

2021ň╣┤´╝îFDAŔÄĚŠë╣ń║ćńŞëšžŹň«ÂšöĘňłćňşÉŠúÇŠÁőŔ»Ľňë隍ĺŃÇéňůÂńŞşń╗ąCue healthŃÇüLucira healthŠťÇńŞ║š¬üňç║ŃÇé2020ň╣┤11Šťł´╝îLucira healthń║žňôüŔÄĚŠë╣´╝î2021ň╣┤3Šťł´╝îCuešÜ䊾░ňćáŠúÇŠÁőń║žňôüŔÄĚŠë╣ŃÇéńŞĄŔÇůňŁçńŞ╗ŔŽüÚççňĆľšşëŠŞęŠëęňóךÜäŠúÇŠÁőŠľ╣ň╝ĆŔ┐ŤŔíîŃÇéňŻôšäÂŔ┐ÖńŞĄŠČżň▒ůň«ÂŔ笊úÇń║žňôü´╝îňťĘń║žňôüŔ«żŔ«íńŞŐňşśňťĘňĚ«ň╝éŃÇéCue HealthÚççňĆľšÜäńŞÇńެňĆ»ÚçŹňĄŹńŻ┐šöĘšÜäňŹíšŤĺÚśůŔ»╗ňÖĘ(Cue Cartridge Reader)´╝îňĆ»ńŞÄŠÖ║Ŕ⯊ëőŠť║AppÚÇÜŔ«»ň╣ÂŔ┐ÉŔíîŠúÇŠÁőňŹí´╝îňĆŽńŞÇÚâĘňłćŠś»ńŞÇŠČíŠÇžńŻ┐šöĘš╗äń╗´╝îńŞÇŠČíŠÇžš╗äń╗Âń╗ĚŠá╝š║Ž60šżÄňůâňĚŽňĆ│ŃÇéňĆ»ÚÇÜŔ┐çńŞÄŠÖ║Ŕ⯊ëőŠť║Ŕ┐׊ĹňÉÄ´╝îňůĘšĘőšö▒ŠëőŠť║AppŠĆÉšĄ║ŠôŹńŻťň╣ŠśżšĄ║š╗ôŠ×ť´╝îńż┐ń║ÄŠĽ░ŠŹ«š╗čŔ«íš«íšÉćŃÇéCue healthń╗ąńŞÇńެŠľ░ňćáŠúÇŠÁőňŹĽń║žňôüň«×šÄ░2021ň╣┤ŠöÂňůąŔżżňł░6.18ń║┐šżÄňůâ´╝î2022ň╣┤Q1ňĚ▓š╗Ćň«×šÄ░ŠöÂňůą1.8ń║┐šżÄňůâŃÇéŔÇîLucira HealthňƬŠś»ńŞÇńެńŞÇŠČíŠÇžńŻ┐šöĘŠÁőŔ»ĽňąŚń╗´╝«ňëŹňö«ń╗ĚňĄžš║Ž75šżÄňůâňĚŽňĆ│ŃÇé

ňŤŻňćůń╣芝ëńŞÇň«ÂńŞŐňŞéňůČňĆŞPreneticsňťĘšľźŠâůŠťčÚŚ┤ň╝ĽňůąšëŤŠ┤ąňĄžňşŽšÜäŠŐÇŠť»ń╗ÄŔÇîšáöňĆĹňç║Šľ░ňćášÜäň«ÂšöĘňłćňşÉŠúÇŠÁőń║žňôüŃÇéńŞ╗ŔŽüńŞ║Circle HealthPodŠúÇŠÁőš│╗š╗č´╝łňö«ń╗Ěš║Ž990ŠŞ»ňŞü´╝ë+ńŞÇŠČíŠÇžŠúÇŠÁőš╗äń╗´╝łňö«ń╗Ěš║Ž200ŠŞ»ňŞü´╝ë´╝îňĚ▓ŔÄĚňżŚCEŔ«ĄŔ»ü´╝¬Ŕç│2022ň╣┤Q1´╝îň«×šÄ░ŔÂů2200ńŞçń╗š╗äń╗ÂÚöÇňö«ŃÇéŔ»ąŠúÇŠÁőš│╗š╗čÚççňĆľÚÇćŔŻČňŻĽŃÇüšÄ»ń╗őň»╝šşëŠŞęŠëęňó×LAMPŠŐÇŠť»Ŕ┐ŤŔíîŠúÇŠÁő´╝îňĆ»ňťĘ20ňłćÚĺčňćůŠĆÉńżŤš╗ôŠ×ťŃÇéŠá╣ŠŹ«PreneticsšÜ䊼░ŠŹ«ŠśżšĄ║´╝îňĆ»ń╗ąň«×šÄ░96%šÜäšüÁŠĽĆň║Žňĺî99.9%šÜäšë╣ň╝éŠÇž´╝îŔĚčqPCRŠúÇŠÁőšÜäšČŽňÉłšÄçŔżżňł░98.4%ŃÇé
ÚÖĄPreneticsňĄľ´╝îňŤŻňćůŔ┐śŠťëňĄÜň«Âń╝üńŞÜňťĘ2021ň╣┤ňĚŽňĆ│šáöňĆĹňç║ňč║ń║ÄńŞŹňÉîšÜ䚺늪ęŠëęňó׊ŐÇŠť»šöĘń║Äň«Âň║şŠľ░ňćáŔ笊úÇšÜäń║žňôüŃÇéňîůŠőČń╝śŠÇŁŔżżŃÇüŠÖ«ńŞľňłęňŹÄŃÇüňůłŔżżňč║ňŤášşëŃÇéŔ┐ÖńŞëň«ÂňůČňĆŞšÜäŠëęňó׊ŐÇŠť»ňŁçńŞŹšŤŞňÉî´╝îňłćňłźÚççšöĘCPAŃÇüRHAMń╗ąňĆŐNew ERAšÜ䚺늪ęŠëęňó׊ŐÇŠť»ŃÇéń╝śŠÇŁŔżżšÜäń║žňôüňĚ▓š╗ĆňťĘ2022ň╣┤4ŠťłŔÄĚňżŚCEšÜäŔ笊ÁőŔ«ĄŔ»üŃÇé

ń╝śŠÇŁŔżżńŞ╗ŔŽüšáöňĆĹšÜ䊜»ňč║ń║ÄšşëŠŞęŠëęňó׊ŐÇŠť»´╝łń║ĄňĆëň╝ĽšëęŠü努ęŠëęňó׊ŐÇŠť»´╝îCPA´╝ëšÜ䊾░ňćáŔ笊Áőń║žňôüŃÇé2021ň╣┤4ŠťłŠő┐ňł░ńŞôńŞÜńŻ┐šöĘňť║ŠÖ»šÜäCEŔ«ĄŔ»ü´╝î 2022ň╣┤4ŠťłŔÄĚňżŚCEšÜäŔ笊ÁőŔ«ĄŔ»üŃÇéŠÖ«ńŞľňłęňŹÄÚÇÜŔ┐çŔç¬ńŞ╗RHAMšşëŠŞęŠëęňó׊ŐÇŠť»´╝îŔ┐ŤŔí늪ęŠöżňĄžňĺîń┐íňĆĚÚçŐŠöż´╝îŠëęňó׊ǞŔâŻńŞÄqPCRšŤŞňŻô´╝îŔ┐ťń╝śń║Äń╝áš╗čšÜäLAMPŠëęňó׊ŐÇŠť»ŃÇéňůłŔżżňč║ňŤášáöňĆĹňç║Šľ░ńŞÇń╗úšşëŠŞęŠëęňó×´╝łNew ERA´╝ëŠŐÇŠť»´╝îňťĘŠüĺň«ÜŠŞęň║ŽŠŁíń╗ÂńŞő´╝î5-8ňłćÚĺčňŹ│ňĆ»ň░ćDNA/RNAŠëęňó׊Ľ░ń║┐ňÇŹ´╝îÚůŹňÉłšőČšë╣šÜäň╝ĽšëęńŞÄŠÄóÚĺłŔ笚Ļňîľš╗ôŠ×ä´╝îńŻ┐ňůĘšĘőŠúÇŠÁőń╗ůÚťÇ10ňłćÚĺčňĚŽňĆ│ňŹ│ňĆ»ň«îŠłÉŃÇé
ÚÖĄń║ćńŞŐŔ┐░šÜ䚺늪ęňłćňşÉŠúÇŠÁőń╗¬ňÖĘńŞÄŔ»Ľňë隍ĺňĄľ´╝îŠÁĚňĄľń╣čňç║šÄ░ń║ćňżłňĄÜšÜäň░Ćň×őňĄÜÚçŹPCRń╗¬ňÖĘń╗ąŠťčšöĘń║Äň«Âň║şŔ笊úÇ´╝îňŽéVisby medical 2022ň╣┤ŔÄĚňżŚń║ćEŔŻ«ŔÂů1.35ń║┐ńŞçšżÄňůâšÜäŔ׏ŔÁä´╝«Šá犜»ŠĆÉńżŤńŞľšĽîńŞŐšČČńŞÇńެŠŚáń╗¬ňÖĘŠëőŠîüň╝ĆPCRň╣│ňĆ░´╝î2021ň╣┤2ŠťłŔÄĚňżŚń║ćFDAšÜäńŞÇŠČíŠÇžRT-PCR COVID-19ň║ŐŠŚüŠÁőŔ»ĽšÜäš┤žŠÇąńŻ┐šöĘŠÄłŠŁâŃÇéň«âŔ┐śŔÄĚňżŚń║ćFDA 510´╝łk´╝ëŔ«ŞňĆ»ňĺîCLIAŔ▒üňůŹ´╝îšöĘń║ÄńŞÇŠČíŠÇžňĄÜÚ珊úÇŠÁőŠ▓Öšť╝ŔíúňÄčńŻô´╝îŠĚőšŚůňąłšĹčŔĆîňĺîÚś┤ÚüôŠ»ŤŠ╗┤ŔÖźŃÇéFilmarryňłŤňžőń║║ń╣čň╝ÇňžőŔ┐ŤňćŤPCRň«Âň║şŔ笊úÇ´╝îIdaho MolecularňĺîAdvanced conceptsňťĘŔ┐çňÄ╗šÜä1ň╣┤ŠŚÂÚŚ┤Úçî´╝îšáöňĆĹń║ćÔÇťEikonÔÇŁšÜäPCRň╣│ňĆ░š╗ôňÉłŠľ░ň×őňćášŐšŚůŠ»ĺŠäčŠčôšŚç(COVID-19)ŠúÇŠÁőŃÇ隍«ňëŹňĚ▓š╗Ćň╝ÇňžőńŞ┤ň║ŐŔ»ĽÚ¬î´╝îň╣ÂňÉĹšżÄňŤŻFDAŠĆÉń║Ąš┤žŠÇąńŻ┐šöĘŠÄłŠŁâŃÇé

ňč║ń║ÄŔ»Ľňë隍ĺšÜäEikonń╗¬ňÖĘňĆ»ň»╣ňĄÜŔżż6ńެšŤ«ŠáçŔ┐ŤŔíîňĄÜÚçŹqPCR´╝îÚÇÜŔ┐çń║ĹŔ┐׊ĹŔŻ»ń╗ÂŔžúŔ»╗ŔŹžňůëŔ»╗ŠĽ░ŃÇéňĆ»ń╗ąňťĘ30ňłćÚĺčňćůŠĆÉńżŤŔ»ŐŠľşš╗ôŠ×ť´╝îÚóäŔ«íŠłÉŠťČňťĘ300šżÄňůâňĚŽňĆ│´╝îŠÁőŔ»ĽšŤĺšÜäń╗ĚŠá╝š║ŽńŞ║15Ŕç│20šżÄňůâŃÇé
´╝ł1´╝ëqPCRŔÖŻńŞ║ŠáŞÚůŞŠúÇŠÁőšÜäÚçĹŠáçňçć´╝îńŻćňşśňťĘŔ»ŞňĄÜÚÖÉňłÂ
qPCRšŤ«ňëŹń╗ŹšäŠś»ŠáŞÚůŞŠúÇŠÁőšÜäÚçĹŠáçňçć´╝îń╣芜»ŠťÇňŞŞÚççšöĘšÜäŠúÇŠÁőŠľ╣Š│ĽŃÇéšö▒ń║ÄňůŠŐÇŠť»ňĆĹň▒ĽŠŚÂÚŚ┤ŔżâÚĽ┐´╝ɚćčň║ŽŔżâÚźś´╝îqPCRŠúÇŠÁőŠłÉŠťČń╣čÚÇÉŠşąÚÖŹńŻÄ´╝îňĄžń╝ŚŠÄąňĆŚšĘőň║Žń╣čÚźśŃÇéńŻćŠś»qPCRŠúÇŠÁőń╣čňşśňťĘńŞÇň«ÜÚÖÉňłÂ´╝Ü
A. ňĄžŔžäŠĘíń║║šżĄÚççŠáĚň»╝Ŕç┤ŠäčŠčôÚúÄÚÖę´╝ÜŠŚóňżÇňŁçÚÇÜŔ┐çňĄžŔžäŠĘíń║║šżĄÚŤćńŞşÚççŠáĚšÜ䊾╣ň╝Ćň╝Çň▒ĽqPCRŠúÇŠÁő´╝îńŞöÚççňĆľ10ŠĚĚ1ŠłľŔÇů5ŠĚĚ1šÜ䊾╣ň╝ĆŔ┐ŤŔíîÚççÚŤć´╝îŔâŻňĄčÚÖŹńŻÄŠłÉŠťČ´╝îńŻćŠś»ň»╣ń║Äňî╗ŠŐĄń║║ňĹśŔÇîŔĘÇňĆ»ŔâŻń╝ÜŠÄąŔžŽňĄžÚçĆšÜ䊯ťňťĘŠäčŠčôŔÇů´╝îÚççŠáĚňÉÄń╣čňĄÜšö▒šČČńŞëŠľ╣ŠúÇڬ║Š×äŔ┐ŤŔíîŠúÇŠÁőŃÇéŔÇîňťĘňî╗ÚÖóÚŚĘŠÇąŔ»Őšşëň░ĆŔžäŠĘíÚççŠáĚŠúÇŠÁőňť║ŠÖ»ńŞő´╝îqPCRŠúÇŠÁőńŞŹňůĚňĄçŠłÉŠťČń╝śňŐ┐ŃÇé
B. ŠáĚŠťČŔ┐ÉŔżôŃÇüŠáŞÚůŞŠĆÉňĆľš║»ňîľšşëŔÇŚŠŚÂÚĽ┐´╝ÜqPCRŠúÇŠÁőŠŐÇŠť»ňťĘŔç¬ňŐĘňîľšÜäňĆĹň▒ĽńŞő´╝îŠúÇŠÁőŠŚÂÚŚ┤ń╣čÚÇÉŠşąš╝ęščş´╝îňĆ»ňťĘ2ň░ĆŠŚÂňćůňç║ňůĚš╗ôŠ×ť´╝îńŻćšö▒ń║ÄňĄžÚçĆŠáĚŠťČńŞ║šČČńŞëŠľ╣ň«×Ú¬îň«ĄŠúÇŠÁő´╝îŠÂëňĆŐňł░šÜäŠáĚŠťČŔ┐ÉŔżôŃÇüń┐ŁňşśŃÇüŠáŞÚůŞŠĆÉňĆľš║»ňîľšşëŠŚÂÚŚ┤ŠłÉŠťČňĆŐń║║ňŐŤŠłÉŠťČšŤŞň»╣ŔżâÚźśŃÇé
C. Š░öŠ║ÂŔâÂÚúÄÚÖęňĆŐÚźśňť║ňť░ŔŽüŠ▒é´╝ÜńŞ║Ŕżżňł░ňůšüÁŠĽĆň║ŽŔĚčšë╣ň╝éŠÇž´╝îňĆśŠŞęŠëęňó×Ŕ┐çšĘőŠŚáňĆ»Úü┐ňůŹ´╝îŠëęňó×Ŕ┐çšĘőńŞşń╝Üň»╝Ŕç┤šŚůňÄčšë犫ÁňĄžÚçĆňĄŹňłÂ´╝îń╗ÄŔÇîňĆ»ŔâŻń╝Üň»╝Ŕç┤Š░öŠ║ÂŔâÂŃÇüŠáĚŠťČń║ĄňĆëŠ▒íŠčôšÜäÚúÄÚÖęŃÇéňŤáŠşĄň»╣ń║ÄŠúÇŠÁőňť║ňť░ŔŽüŠ▒éŔżâÚźś´╝îŠëÇń╗ąqPCRŠŚáŠ│ĽÚÇéšöĘń║Äň║ŐŠŚüšÜäň┐źÚÇčŠúÇŠÁőšşëŃÇé
D. ŠúÇŠÁőŔ«żňĄçŔŽüŠ▒éÚźś´╝ÜqPCRšö▒ń║ÄňůŠëęňóךÜäŔ┐çšĘőŠÂëňĆŐňĆśŠŞęŃÇüÚÇÇšüźšşëšÄ»ŔŐé´╝îňŤáŠşĄň»╣Ŕ«żňĄçŔŽüŠ▒éŔżâÚźś´╝îŔÇáŠ│ĽňâĆšşëŠŞęŠëęňó׊łľŔÇůňůŹŠëęňóךÜäCRISPRŠŐÇŠť»ńŞÇŠáĚň»╣Ŕ«żňĄçŔŽüŠ▒éŔżâńŻÄŃÇé
´╝ł2´╝뚺늪ęŠëęňó×ŔâŻňĄčň«×šÄ░ň┐źÚÇčŃÇüšÄ░ňť║ŠúÇŠÁő´╝îńŻćŠś»ňüçÚś│ŠÇžšÄçŔżâÚźś
Ŕ┐ĹńŞĄň╣┤ŠŁąňĆĹň▒ĽŔ┐ůÚÇčšÜ䚺늪ęŠëęňó׊úÇŠÁőŠŐÇŠť»ňĆ»ń╗ąň«×šÄ░ŠáĚŠťČšÄ░ňť║ÚççÚŤćňÉÄšŤ┤ŠÄąšÄ░ňť║ŠÁőÚçĆ´╝îńŞöšö▒ń║ÄŠëęňó׊ĽłšÄçÚźś´╝îŠúÇÚ¬îš╗ôŠ×ťňĆ»ňťĘ30minňćůŔÄĚňżŚŃÇéńŻćŠś»šşëŠŞęŠëęňó׊úÇŠÁőŠŐÇŠť»ňĆŚÚÖÉń║ÄŠëęňó×Ŕ┐çšĘőńŞşń╝Üňç║šÄ░ňĄžÚçĆšÜäڣךë╣ň╝éŠÇžŠëęňó×´╝îń╗ÄŔÇîň»╝Ŕç┤ňĄžÚçĆšÜäňüçÚś│ŠÇžń║žšöč´╝îŠúÇŠÁőšë╣ň╝éŠÇžŔżâńŻÄŃÇéňÉšö▒ń║ÄŠś»šşëŠŞęŠëęňó×´╝îň»╣ń║Äň╝ĽšëęŔ«żŔ«íŔŽüŠ▒éń╣čŔżâÚźśŃÇé
ňŻôšä´╝îń╣芺úŠś»šö▒ń║ÄňůšşëŠŞęŠëęňó×´╝îÚÖŹńŻÄń║ćň»╣ŠúÇŠÁőŔ«żňĄçšÜäŔŽüŠ▒é´╝îŠëÇń╗ą2021ň╣┤ňŤŻňćůňĄľňĄžÚçĆń║žňôüšáöňĆĹňç║ŠŁąŔóźň║öšöĘń║Äň«ÂšöĘŠľ░ňćáŠúÇŠÁő´╝îńŻćńŞŹňĆ»ňÉŽŔ«ĄšÜ䊜»ňĄžŠÁüŔíîńŞőňüçÚś│ŠÇžšÜäš╗ôŠ×ťňŐ┐ň┐ůń╝Üń║žšöčńŞÇń║ŤňůÂń╗ľšÜäňŻ▒ňôŹŃÇé
2021ň╣┤ň«ÂšöĘňłćňşÉŠúÇŠÁőňĆĹň▒ĽÚŁ×ňŞŞŔ┐ůÚÇč´╝îńŻćŠś»ń╗Źń╗ąšşëŠŞęŠëęňó׊ŐÇŠť»ńŞ║ńŞ╗´╝îňşśňťĘńŞÇň«ÜšÜäň▒ÇÚÖÉŠÇžŃÇéŔÇîÚÜĆšŁÇCRISPRŔ»ŐŠľşŠŐÇŠť»šÜäÚÇÉŠşąňĆĹň▒ĽńŞÄŠłÉšćč´╝îňÉÂňůĚňĄçšŤŞň║öšÜäń╝śňŐ┐´╝îňĄžň«Âń╣čňťĘÚÇÉŠşąň░ćCRISPRŔ»ŐŠľşŠŐÇŠť»ň║öšöĘń║Äň«ÂšöĘňłćňşÉŠúÇŠÁőŃÇé
2016ň╣┤´╝îňŤŻňĄľńŞĄńެňŤóÚśčňĆĹšÄ░ń║ćCRISPRšÜ䊾░Úů´╝îňĆ»ń╗ąŔ┐ŤŔíîڣךë╣ň╝éŠÇžšÜäňłçňë▓´╝îCRISPRŠúÇŠÁőŠŐÇŠť»ńż┐šö▒ŠşĄň▒Ľň╝ÇŃÇéCRISPRŠúÇŠÁőŠŐÇŠť»ŠëÇšöĘšÜäCasŔŤőšÖŻńŞ╗ŔŽüŠťëCas12ŃÇüCas13´╝îŔ┐Öš▒╗ŔŤőšÖŻÚÖĄń║ćńŞÄCas9ńŞÇŠáĚ´╝îňůĚŠťëšë╣ň╝éŠÇžňłçňë▓ÚŁÂň║ĆňłŚšÜäňŐčŔâŻňĄľ´╝îňťĘŠ┐ÇŠ┤╗šŐŠÇüńŞő´╝îŔ┐śňůĚŠťëڣךë╣ň╝éŠÇžňłçňë▓ňůÂň«âŠáŞÚůŞň║ĆňłŚšÜäňŐčŔâŻŃÇéňťĘŠ▓튝ëŠ┐ÇŠ┤╗šÜäšŐŠÇüńŞő´╝îCasŔŤőšÖŻń┐ŁŠîüŠ▓ëÚ╗ś´╝ŤńŞÇŠŚŽŔóźŠ┐ÇŠ┤╗´╝îńż┐ń╝ÜŔ┐ŤŔíîڣךë╣ň╝éŠÇžňłçňë▓ňůÂń╗ľŠÉ║ňŞŽŔŹžňůëń┐íňĆĚšÜäŠáŞÚůŞň║ĆňłŚ´╝îń╗ÄŔÇîňĆ»ń╗ąÚçŐŠöżŔŹžňůëń┐íňĆĚ´╝îń╗ÄŔÇîšöĘŠŁąŔ┐ŤŔíîŠúÇŠÁőŃÇé
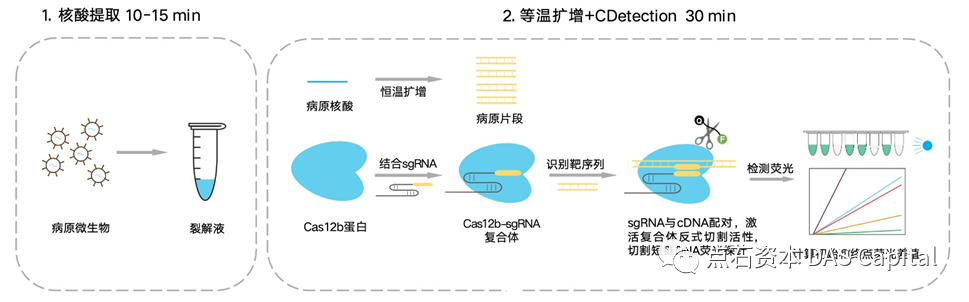
Cas12ňťĘcrRNAň╝Ľň»╝ńŞőňŹ│ňĆ»Ŕ»ćňłźÚŁÂŠáçdsDNA´╝îň╣ÂÚŁÂňÉĹň»îňÉźTšÜäPAMńŻŹšé╣´╝îň»╣ÚŁÂň║ĆňłŚŔ┐ŤŔíîšë╣ň╝éŠÇžňłçňë▓´╝îňÉÂÚÖäňŞŽÚŁ×šë╣ň╝éŠÇžňłçňë▓ssDNAšÜäŠ┤╗ŠÇžŃÇéڣŠáçŠáŞÚůŞš╗ĆšşëŠŞę´╝łRPAŠłľLAMP´╝ëŠëęňó×ň»îÚŤć´╝îšäÂňÉÄŠëęňó×ń║žšëęńŞÄCas12-crRNAš╗ôňÉł´╝îŠ┐ÇŠ┤╗Cas12šÜäÚÖäň▒×ňłçňë▓ňŐčŔ⯴╝îň»╣ssDNAŔŹžňůëŠÄóÚĺłŔ┐ŤŔíîňłçňë▓´╝îÚçŐŠöżŔŹžňůëňč║ňŤó´╝îňŻóŠłÉŠúÇŠÁőń┐íňĆĚŃÇé
Cas13Šś»ńŞÇšžŹRNAň╝Ľň»╝šÜäRNAŠáŞÚůŞňćůňłçÚů´╝îňĆ»ňťĘcrRNAšÜäň╝Ľň»╝ńŞőšë╣ň╝éŠÇžňłçňë▓ňŹĽÚôżÚŁÂŠáçRNA´╝îň╣ÂňťĘň«îŠłÉňłçňë▓ňÉÄ´╝îňĆ»š╗žš╗şń┐ŁŠîüŠ┤╗ŠÇžň╣Âňłçňë▓ňůÂń╗ľÚŁ×ڣŠáçRNAŃÇéڣŠáçŠáŞÚůŞš╗ĆšşëŠŞęŠëęňó׊ŐÇŠť»RPAŠëęňó×ň╣Âň╝ĽňůąT7ňÉ»ňŐĘňşÉň║ĆňłŚňÉÄ´╝îňćŹňłęšöĘT7 RNAŔüÜňÉłÚůÂŔŻČňŻĽňŻóŠłÉssRNA´╝îŔŻČňŻĽń║žšëęńŞÄCas13a-crRNAš╗ôňÉł´╝îŠ┐ÇŠ┤╗Cas13aŠáŞÚůŞÚůŠ┤╗ŠÇž´╝îňłçňë▓ssRNAŔŹžňůëŠÄóÚĺł´╝îÚçŐŠöżňĆ»ŔóźŠúÇŠÁőšÜäŔŹžňůëňč║ňŤóŃÇé
ňŤŻňĄľŠťÇŠŚęń║Ä2016ň╣┤ňĆĹšÄ░šÜäÚůŠś»Cas13 ŔĚč Cas12ašÜäÚů´╝îň╣ÂňťĘ2018ň╣┤ňĆĹŔíĘňč║ń║ÄCas13 ŔĚč Cas12ašÜäÚůšÜäŠúÇŠÁőŠŐÇŠť»´╝ŤňŤŻňćůňťĘ2018ň╣┤ń╣čňťĘCell DiscoveryŠťčňłŐńŞŐňĆĹŔíĘń║ćńŞĄš»çŠľçšźá´╝îňłćňłźŠś»ńŞşňŤŻšžĹňşŽÚÖóńŞŐŠÁĚšöčňĹŻšžĹňşŽšáöšęÂÚÖóšÄőÚçĹňŤóÚśčň╝ÇňĆĹšÜäňč║ń║ÄCas12ašÜäňłćňşÉŔ»ŐŠľşŠŐÇŠť»ňĆŐńŞşňŤŻšžĹňşŽÚÖóŠŁÄń╝芼֊ijňŤóÚśčňĆĹšÄ░šÜäňč║ń║ÄCas12b ÚůšÜäňĚąšĘőňîľň║öšöĘŃÇé
2022ň╣┤´╝îNatureňĆĹňŞâň╣┤ň║ŽňÇ╝ňżŚňů│Š│ĘšÜäŠŐÇŠť»ŠŽťňŹĽ´╝îňůÂńŞşCRISPR-CasŔ»ŐŠľşŠúÇŠÁőŔóźňłŚńŞ║ňůÂńŞşń╣őńŞÇ´╝îÚÇÜŔ┐çCas12ÚůŠłľŔÇůCas13ÚůšÜäšë╣ňżü´╝îňĆ»ŠúÇŠÁőň╣┐Š│ŤšÜ䚌ůňÄčńŻô´╝îń╣âŔç│ŠťëŠĽłňť░Ŕ»ŐŠľşňůÂń╗ľÚŁ×ŠäčŠčôŠÇžšľżšŚůŃÇ隍«ňëŹňŤŻňćůňĄľšÜäňůČňĆŞňÇčňŐęCRISPRŠúÇŠÁőŠŐÇŠť»ňĚ▓š╗ĆňĆ»ń╗ąňťĘ30ňłćÚĺčňćůň«×šÄ░Úĺłň»╣šŚůňÄčšÜäň┐źÚÇčŃÇüňçćší«šÜäŠúÇŠÁőŃÇé
ń╗Ä2018ň╣┤ń╗ąŠŁą´╝îCRISPRŠúÇŠÁőŠŐÇŠť»šÜ䊾çšî«šáöšęŠäłňĆĹňó×ňĄÜ´╝îňł░2021ň╣┤ňĚ▓ŔÂůńŞŐňŹâš»çŃÇéCRISPRŠúÇŠÁőŠŐÇŠť»ń╣čŠäłňĆĹŠłÉšćč´╝îň╣ÂńŞŹŠľşŠőôň▒ĽŃÇ隍«ň돊Łąšťő´╝îŠúÇŠÁőŠŐÇŠť»ńŞ╗ŔŽüňÉĹ3ńެŠľ╣ňÉĹŠőôň▒ĽšáöňĆĹŃÇé
CRISPR/Casš│╗š╗čńŻťńŞ║ńŞÇšžŹňĆ»šë╣ň╝éŠÇžŔ»ćňłźÚŁÂň║ĆňłŚ´╝îň╣ÂňůĚŠťëňéČňöżňĄžń┐íňĆĚňŐčŔ⯚ÜäŠúÇŠÁőŠŐÇŠť»´╝îňťĘCas12ń╗ąňĆŐCas13ÚůÂň»╣ňĆŹň║öńŻôš│╗ńŞşňůÂń╗ľšÜäŔŹžňůëŠÄóÚĺłňë¬ňłçňÉĚ躊ŚÂÚŚ┤ň░▒Ŕ⯊öżňĄžňł░10^5šÜäŔŹžňůëń┐íňĆĚňç║ŠŁą´╝îňĆ»šŤ┤ŠÄąň»╣ڣŠáçň║ĆňłŚŔ┐ŤŔíîŠúÇŠÁő´╝îńŻćšŤ«ň돚ÜäŠúÇŠÁőŠľ╣Š│Ľ´╝îňŁçÚťÇÚóäňůłŠëęňó×ڣŠáçŠáŞÚůŞňÉÄ´╝îňůŠúÇŠÁőšüÁŠĽĆÔÇŹň║ŽŠľ╣ňĆ»Š╗íŔÂ│Ŕ»ŐŠľşŔŽüŠ▒é´╝îŔ┐Öň░▒ňó×ňŐáń║ćŠôŹńŻťŠşąÚ¬Ą´╝îŔÇŚŠŚÂń╣芍┤ÚĽ┐ŃÇé
CRISPRŠúÇŠÁőŠŐÇŠť»ňĄęšäÂňůĚňĄçňůŹŠëęňóךÜäňč║šíÇŃÇ銝¬ŠŁąÚÇÜŔ┐çňůŹŠëęňó×ňĆ»ÚÖŹńŻÄŠúÇŠÁőŔ«żňĄçšÜäŔŽüŠ▒é´╝îňÉÂń╣čňĆ»ń╗ąšŤ┤ŠÄąń╗ÄŠ║ÉňĄ┤ńŞŐÚü┐ňůŹŠ░öŠ║ÂŔâŠ▒íŠčôšÜäÚúÄÚÖęŃÇ隍«ňëŹňůŹŠëęňóךÜäŠŐÇŠť»ńŞ╗ŔŽüÚÇÜŔ┐çÚůÂń┐âš║žŔüöŠöżňĄž´╝łńŻ┐šöĘňĄÜšžŹŠáŞÚůŞÚů´╝îňťĘCas12bŠ┐ÇŠ┤╗ňÉÄŔ┐ŤŔíîŔ┐ŤńŞÇŠşąšÜäÚůÂňşŽŠöżňĄž´╝îŠĆÉÚźśŠáŞÚůŞŠÄóÚĺłšÜäňłçňë▓ŠĽłšÄç´╝îňŽéňŤŻňĄľňĚ▓š╗ĆŠťëšáöšęÂňťĘCas13Š┐ÇŠ┤╗ňÉÄńŻ┐šöĘňĆŽńŞÇšžŹšž░ńŞ║ Csm6šÜä Cas ŔŤőšÖŻŠŁąŠöżňĄžŔŹžňůëń┐íňĆĚ´╝ëŃÇüšöÁňîľňşŽń╝áŠäčŠöżňĄž´╝łšč│ňóĘšâ»ňť║ŠĽłň║öŠÖÂńŻôš«í´╝ëŃÇüňż«ň«╣ÚçĆCRISPR-Dxš│╗š╗č´╝łňż«ŠÁüŠÄžŃÇüňż«ŠÂ▓Š╗┤ŠŐÇŠť»šşë´╝늣ąň«×šÄ░ŃÇé

ÚÇÜŔ┐çňż«ŠÁüŠÄžšşëŠľ╣ň╝Ćň«×šÄ░dd CRISPRň«ÜÚçĆŠúÇŠÁő´╝îŔ┐ŤŔÇîňťĘŠť¬ŠŁąňůĚňĄçŠŤ┤ň╣┐ÚśöšÜäňĆĹň▒Ľšę║ÚŚ┤ŃÇé
ňĆ»ń╗ąšöĘňŹĽńެCasŔŤőšÖŻŠúÇŠÁőńŞÇšžŹšŚůňÄčńŻô´╝îń╣čňĆ»ňÉÂńŻ┐šöĘňçášžŹÚůÂŔ┐ŤŔíîňĄÜÚçŹňłćŠ×É´╝îń╗ąňî║ňłćňĄÜšžŹšŚůňÄčńŻô´╝îňťĘŠť¬ŠŁąńŞ┤ň║ŐŠłľň«ÂšöĘŠŚÂň«×šÄ░ňĄÜŔüöŠúÇŠÁő´╝┤ńż┐ŠŹĚŃÇüŠŤ┤ÚÇéšöĘŃÇüŠłÉŠťČŠŤ┤ńŻÄŃÇéňŽéň╝áÚöőňŤóÚśčňťĘSHERLOCKv2š│╗š╗čńŞşňó×ňŐáń║ćCasŔŤőšÖŻšÜäšžŹš▒╗´╝łLwaCas13a ŃÇüPsmCas13bŃÇüCcaCas13b ňĺîAsCas12a´╝ë´╝îŔ┐ÖŠáĚňĆ»ń╗ąňÉŠúÇŠÁőňł░ňŤŤšžŹšŚůŠ»ĺ´╝Ťň╣ÂňłęšöĘCsm6ÚůŠöżňĄžňůŠúÇŠÁőń┐íňĆĚŃÇé
ň»╣Š»öqPCRňĆŐšşëŠŞęŠëęňó׊úÇŠÁőŠŐÇŠť»ŔÇîŔĘÇ´╝îCRISPRŠúÇŠÁőŠŐÇŠť»ÚççňĆľšşëŠŞęŠëęňó×+CasÚůšÜäňĆŹň╝Ćňłçňë▓´╝îňÇčňŐęsgRNAšÜäšë╣ň╝éŠÇžŔ»ćňłź´╝îŠĆÉňŹçń║暺늪ęŠëęňó×ňÉÄšÜäšë╣ň╝éŠÇž´╝îńŻćňĆłňżłňąŻšÜäń┐ŁšĽÖń║暺늪ęŠëęňóךÜäń╝śňŐ┐´╝öňŽéňĆ»ń╗ąň«×šÄ░šÄ░ňť║ň┐źÚÇčŠúÇŠÁőŃÇüšüÁŠĽĆň║ŽÚźśŃÇüŠúÇŠÁőŔ«żňĄçŔŽüŠ▒éńŻÄŃÇüňŹĽŠČíŠúÇŠÁőŠłÉŠťČńŻÄšşë´╝îňÉšüÁŠĽĆň║ŽňĆ»ńŞÄqPCRšŤŞň¬▓šżÄ´╝îš╗╝ňÉłŠúÇŠÁőŠłÉŠťČń╣čńŻÄń║ÄqPCRŃÇéňťĘŠť¬ŠŁą´╝îCRISPRŠúÇŠÁőŠŐÇŠť»ň«×šÄ░ňůŹŠëęňó×ňÉÄň░ćÚü┐ňůŹŠ░öŠ║ÂŔâÂń║žšöč´╝îŔ┐ŤńŞÇŠşąÚÖŹńŻÄŔ«żňĄçŔŽüŠ▒éňĺîšÄ»ňóâŔŽüŠ▒é´╝îń╗ÄŔÇ┤ÚÇéšöĘń║ÄÚŚĘŃÇüŠÇąŔ»ŐŃÇüšĄżňî║ŠúÇŠÁőŃÇüŠÁĚňů│ŠúÇšľźŃÇüň«ÂšöĘšşëňť║ŠÖ»ŃÇé
šŤ«ňëŹňŤŻňćůňĄľňĄÜň«ÂňůČňĆŞňťĘň╝Çň▒Ľňč║ń║ÄCRISPRŔ»ŐŠľşšÜ䚍Şňů│šáöňĆĹňĆŐń║žňôüŔ«żŔ«í´╝îńŞ╗ŔŽüňłćńŞ║ńŞĄňĄžš▒╗ŃÇéńŞÇňĄžš▒╗Šś»ňůĚňĄçCRISPRň║Ľň▒éńŞôňłęÚů´╝łCas12 ŃÇüCas13Úů´╝ëŠŐÇŠť»ň╣Âň╝Çň▒ĽšŤŞňů│Ŕ»ŐŠľşšÜäňůČňĆŞ´╝îňŽéProof diagnosticsŃÇüŔ┐ůŔ»ćšöčšëęšşëŃÇéňĆŽńŞÇňĄžš▒╗Šś»ňÇčňŐęCRISPRŔ»ŐŠľşŠŐÇŠť»ň╝ÇňĆĹšŤŞňů│Ŕ«żňĄçšÜäňůČňĆŞ´╝îńŻćňĆ»Ŕ⯚╝║ń╣ĆšŤŞňů│šÜäň║Ľň▒éÚůÂńŞôňłę´╝îňŽéŠŁşňĚ×ń╝ŚŠÁőŃÇüŠŁ░Š»ůšöčšëęšşëŃÇé
šČČńŞÇš▒╗ňůĚňĄçň║Ľň▒éÚůÂňĺîŠúÇŠÁőńŞôňłęŠŐÇŠť»šÜäňůČňĆŞ´╝îŠîüš╗şňťĘń╝śňŐÇŠť»ňĺîň╝ÇňĆĹňłŤŠľ░ń║žňôü´╝îŠŐąŔ»üšÜäŔ┐Ťň▒ĽšŤŞŔżâń║ÄňŹĽš║»ńŻ┐šöĘCRISPRŠŐÇŠť»šáöňĆĹŔ«żňĄçŃÇüŔ»Ľňë隍ĺšÜäňůČňĆŞňĆŹŔÇîŔżâŠůó´╝îňŽéňŤŻňĄľŔ┐Ťň▒ĽŠťÇň┐źšÜäńŞ║Proof diagnostics´╝î2022ň╣┤4Šťłň░抾░ňćášÜäŔ»Ľňë隍ĺŠĆÉń║ĄFDAšö│Ŕ»ĚEUA´╝îÚóäŔ«íńŞëňşúň║ŽňĆ»ŔâŻń╝Üň«íŠë╣ÚÇÜŔ┐çń╗ÄŔÇîŔ┐ŤŔíîŔ»ĽšöĘŃÇéňŤŻňćůňůĚňĄçň║Ľň▒éCasÚůÂńŞôňłęšÜäńŞĄň«ÂňůČňĆŞŔ┐ůŔ»ćšöčšëęń╗ąňĆŐňŹŚń║ČňÉÉÚť▓ŠŞ»šöčšëęŔ┐Ťň▒ĽŔżâň┐ź´╝îňÉÉÚť▓ŠŞ»šöčšëęňĚ▓š╗Ćń║Ä2021ň╣┤9ŠťłńŞÄń╝»ŠŁ░šöčšëęňÉłńŻťšáöňĆĹňç║Šľ░ňćáŔ»Ľňë隍ĺň╣ÂŔÄĚŠë╣ŃÇé
šČČń║îš▒╗ŔüÜšäŽňťĘńŻ┐šöĘCRISPRŠŐÇŠť»ň╝ÇňĆĹŔ»ŐŠľşŔ«żňĄçňĆŐŔÇŚŠŁÉšÜäňůČňĆŞŔ┐Ťň▒ĽšŤŞň»╣Ŕżâň┐ź´╝îňŽéŠŁşňĚ×ń╝ŚŠÁőňĚ▓š╗ĆňťĘ2020ň╣┤ŔÄĚňżŚNMPAŠë╣ňçć´╝îšáöňĆĹšÜäŠáŞÚůŞŠúÇŠÁőŔ»Ľňë隍ĺ´╝łňŤŻŠó░Š│Ęňçć20203400919´╝ëÚççšöĘ RAA ŠŐÇŠť»Šëęňó×ňÉÄ´╝îňćŹńŻ┐šöĘ CRISPR ÚůÂŔ┐ŤŔíîŠúÇŠÁő´╝îÚÇÜŔ┐çš«ÇňŹĽńŞëŠşąňŹ│ňĆ»ňťĘ1ńެň░ĆŠŚÂšÜ䊌ÂÚŚ┤Úçîň«îŠłÉŠúÇŠÁő´╝»ňŤŻňćůÚŽľŠČíŠë╣ňçćňłęšöĘ CRISPR ŠŐÇŠť»šÜ䊾░ňćᚌůŠ»ĺŠúÇŠÁőŔ»Ľňë隍ĺ´╝îńŻćňşśňťĘńŞÇň«ÜÚúÄÚÖęŃÇé
ňŤŻňćůňĄľňůĚňĄçň║Ľň▒éCasÚůÂńŞôňłęńŞöŔ┐Ťň▒ĽŔżâň┐źšÜäňůČňĆŞńŞ╗ŔŽüńŞ║ń╗ąńŞő5ň«ÂŃÇéňŤŻňĄľšÜäńŞëň«ÂňůČňĆŞŠŁąŠ║Éń║ÄńŞĄńެň«×Ú¬îň«ĄńŞôňłęŠŐÇŠť»´╝îńŞöŔ┐ĹńŞĄň╣┤ŠŁąńŞëň«ÂňůČňĆŞŔ׏ŔÁäŠÇ╗ÚóŁŔżżňł░5ń║┐šżÄňůâ´╝îŔíĘŠśÄń║ćŔÁ䊝ČňŞéňť║ň»╣ń║ÄCRISPRŔ»ŐŠľşšÜäÚçŹŔžćŃÇéńŞöńŞëň«ÂňůČňĆŞňťĘŔÄĚňżŚŔ׏ŔÁäń╣őňÉÄÚâŻňťĘňżÇň«ÂšöĘňłćňşÉŠúÇŠÁőňŞéňť║Ŕ┐ŤŔíîň╝ÇŠőôŃÇé

ňůČňĆŞŠłÉšźőń║Ä2019ň╣┤´╝îšö▒ň╝áÚöőňĆéńŞÄŠłÉšźő´╝îŠáŞň┐âŠŐÇŠť»šö▒Ú║╗šťüšÉćňĚąňşŽÚÖóňĺîňôłńŻŤňĄžňşŽŠÄłŠŁâŃÇéSHERLOCKŠŐÇŠť»Šś»ňč║ń║ÄCRISPR/Cas13ŠŁąŠúÇŠÁő´╝«ňëŹňĚ▓ňŹçš║žňł░2.0šëłŠťČÔÇöÔÇöSTOPCovid.V2ŃÇéňťĘŠáĚŠťČňłÂňĄçšÜäŔ┐çšĘőńŞşÚÇÜŔ┐çňŐáňůąšúüšĆáň»îÚŤćŠáĚŠťČńŞşšÜäRNA´╝îń╗ÄŔÇîŠĆÉÚźśŔÁĚňžőRNAŠĽ░ÚçĆ´╝îŔ┐ŤńŞÇŠşąŠĆÉÚźśń║ć STOPCovid.V2 šÜäŠúÇŠÁőšüÁŠĽĆň║Ž´╝îŔâŻňĄčŔżżňł░93.1%šÜäšüÁŠĽĆň║ŽŃÇü98.5%šÜäšë╣ň╝éŠÇž´╝îńŞöÚś│ŠÇžŠáĚŠťČňƬڝÇ15-45ňłćÚĺčň░▒ŔâŻŔÄĚňżŚš╗ôŠ×ťŃÇéÚÖĄŠşĄń╗ąňĄľ´╝îSHERLOCKňĚ▓ŔóźŔ»üŠśÄŔ⯊úÇŠÁőň»ĘňŹíšŚůŠ»ĺňĺîšÖ╗ÚŁęšâşšŚůŠ»ĺ´╝îň╣ÂŔ⯊úÇŠÁőÚŁ×ň░Ćš╗ćŔâ×Ŕé║šÖîŠéúŔÇůŠÂ▓ńŻôŠ┤╗ŠúÇńŞşšÜäńŞŹňÉüňĆśŃÇéňůČňĆŞŠł¬Ŕç│šŤ«ňëŹŔÄĚňżŚ1.4ń║┐šżÄňůâšÜäŔ׏ŔÁäŠÇ╗ÚóŁŃÇé
ňůČňĆŞŠłÉšźőń║Ä2020ň╣┤´╝îńŞ╗ŔŽüňč║ń║ÄCRISPR/Cas12b ÚůÂŔ┐ŤŔíîŔ»ŐŠľşň║öšöĘŃÇéÚÇÜŔ┐ç18ńެŠťłšÜäšáöňĆĹ´╝îŔ«żŔ«íňç║ń║ćńŞÇšžŹň░Ćň×őńż┐ŠÉ║ň╝ĆŠÖ║ŔâŻŔ«żňĄçňĆ»šöĘń║ÄŠľ░ňćáŠúÇŠÁő´╝îňÉÂňĆ»ń╗ąńŞÄŠëőŠť║Ŕ┐ŤŔíîš╗Ĺň«ÜŔÄĚňżŚŠÁőŔ»Ľš╗ôŠ×ťŃÇ隍«ňëŹProof Diagnostics ňĚ▓ňÉĹšżÄňŤŻFDAŠĆÉń║Ąń║ćńŞÇń╗Żšö│Ŕ»Ě´╝îň»╗Š▒éňůÂPOCT Covid-19 ŠÁőŔ»Ľ Proof Lab š│╗š╗čšÜäEUAŃÇéŔőąŔÄĚŠë╣´╝늝Ťň╝ÇňÉ»ň┐źÚÇčPOCTňĺîň«Âň║şňłćňşÉŔ笊úÇšÜ䊝¬ŠŁąŃÇé

2017ň╣┤šö▒Jennifer DoudnaňłŤšźő´╝îńŞ╗ŔŽüňłęšöĘCRISPRŠŐÇŠť»šáöňĆĹń╝áŠčôšŚůŃÇüŔé┐šśĄňşŽňĺîňč║ňŤáš¬üňĆśŠľ╣ÚŁóšÜäň┐źÚÇčŔ»ŐŠľşŃÇéňůČňĆŞňč║ń║ÄCRISPR-Cas12ašÜäDETECTRš│╗š╗čŔâŻňĄčňłćŠ×Éš╗ćŔâ×ŃÇüŔíÇŠÂ▓ŃÇüňöżŠÂ▓ŃÇüň░┐ŠÂ▓ňĺîš▓¬ńż┐´╝îń╗ąŠúÇŠÁőňč║ňŤáš¬üňĆśŃÇüšÖçňĺîŠŐŚšöčš┤áŔÇÉŔŹ»ŠÇž´╝îń╗ąňĆŐŔ»ŐŠľşš╗ćŔĆîňĺůŠ»ĺŠäčŠčôŃÇ銍żŠťëšáöšęÂňłęšöĘDETECTRň»╣ňîůňÉźń║║ń╣│ňĄ┤šśĄšŚůŠ»ĺ´╝łHPV´╝ëšÜäŠéúŔÇůŠáĚŠťČŔ┐ŤŔíîŠÁőŔ»Ľ´╝îňĆ»ń╗ąňĆĹšÄ░ŔâŻňĄčňťĘŠäčŠčôňĄÜšžŹńŞŹňÉîHPVš▒╗ň×őšÜäŠáĚŠťČńŞşňçćší«ŠÁőň«Üňç║ÚźśÚúÄÚÖęšÜäHPV š▒╗ň×ő´╝ÜHPV16ňĺîHPV18ŃÇéňťĘŠľ░ňćáŠúÇŠÁőŠľ╣ÚŁó´╝îňč║ń║ÄCRISPR-Cas12šÜäńżžňÉĹŠÁüňŐĘŠÁőň«ÜŠ│ĽŔíĘŠśÄCRISPR-Cas12ňůĚŠťëńŞÄqRT-PCRŠÁőŔ»ĽšŤŞňÉîšÜ䊼ƊäčŠÇžňĺîšë╣ň╝éŠÇž´╝îňůĚŠťë95´╝ůšÜäÚś│ŠÇžÚóäŠÁőńŞÇŔç┤ŠÇžňĺî100´╝ůšÜäÚś┤ŠÇžÚóäŠÁőńŞÇŔç┤ŠÇžŃÇéňůČňĆŞŠł¬Ŕç│šŤ«ňëŹňĚ▓š╗ĆŔÄĚňżŚ2.6ń║┐šżÄňůâšÜäŔ׏ŔÁäŠÇ╗ÚóŁŃÇé
ňůČňĆŞŠłÉšźőń║Ä2020ň╣┤´╝îňŤóÚśčŠĚ▒ŔÇĽňłćňşÉŔ»ŐŠľşňŹüńŻÖň╣┤´╝îń╗ąCRISPRŠŐÇŠť»ńŞ║ŠáŞň┐â´╝îš╗ôňÉłňż«ŠÁüŠÄžŠŐÇŠť»ňĺîňÉłŠłÉšöčšëęňşŽ´╝îńŞôŠ│Ęń║ÄŠľ░ňů┤ňłćňşÉšöčšëęňşŽŠŐÇŠť»šÜäňÄčňłŤň╝ÇňĆĹń╗ąňĆŐňŹ│ŠŚÂŔ»ŐŠľş´╝ł Point of Care Test, POCT ´╝ëÚóćňččń║žňôüšÜäšáöňĆĹňĺîň║öšöĘŃÇéňůČňĆŞŠőąŠťëCRISPR/CasŠúÇŠÁőŠŐÇŠť»ŠÄłŠŁâ´╝îň╣ÂňĚ▓š╗Ćň«×šÄ░šŤŞňů│ŠłÉŠ×ťŔŻČňîľňĆŐń║žńŞÜňîľŃÇé
ňÉÉÚť▓ŠŞ»šöčšëęšÜäŠŐÇŠť»ŠŁąŠ║Éń║ÄńŞşšžĹÚÖóšÄőÚçĹňŹÜňúźňŤóÚśč´╝îňůČňĆŞňťĘ2017ň╣┤ň╝ÇňĆĹń║ćňč║ń║ÄCRISPR/Cas12š│╗š╗čšÜäňłŤŠľ░ŠáŞÚůŞŠúÇŠÁőŠŐÇŠť»ŃÇé2021ň╣┤ŔĚčń╝»ŠŁ░šöčšëęňÉłńŻťšáöňĆĹňç║ń╝»ŠŁ░BG-Nova-X8š│╗š╗čŃÇéŠÉşÚůŹńŞÇňÉîŔÄĚŠë╣šÜ䊾░ň×őňćášŐšŚůŠ»ĺ2019-nCoVŠáŞÚůŞŠúÇŠÁőŔ»Ľňë隍ĺŔâŻňĄčňťĘ30minňćůň«îŠłÉňĄÜŔżż24ńެŠáĚŠťČšÜäŠúÇŠÁőŃÇé
Ŕ┐äń╗ŐńŞ║Šşó´╝îňč║ń║ÄCRISPRšÜäŔ»ŐŠľşŠľ╣Š│ĽšÜäňç║šëłšëęňĄžňĄÜň▒ÇÚÖÉń║Äń╝áŠčôšŚůšÜäŠúÇŠÁőŃÇéńŻćšö▒ń║ÄCRISPRŔ»ŐŠľşšë╣ň╝éŠÇžŠ×üňąŻ´╝îňĆ»ń╗ąŠúÇŠÁőňł░ńŞÇńެšó▒ňč║šÜ䚬üňĆś´╝ľŔ«ŞŠť¬ŠŁąňťĘÚüŚń╝áŠÇžšľżšŚůŃÇüňůÂń╗ľÚŁ×ń╝áŠčôŠÇžšľżšŚůňĺîšÖçŠúÇŠÁőńŞŐń╣čń╝ÜňĄžŠöżň╝éňŻęŃÇéňŽéń╗Ő´╝îńŞşňĄľCRISPRŔ»ŐŠľşŠŐÇŠť»ňůČňĆŞŔ┐Ťň▒ĽńŞŹšŤŞń╝»ń╗▓´╝îňĽćńŞÜňîľňĺîń║žńŞÜňîľń╣čňĄäń║ÄńŞŹŠľşŠÄóš┤óń╣őńŞş´╝¬ŠŁąšÜäň«ÂšöĘňłćňşÉŠúÇŠÁőňŞéňť║´╝îŔ░üńŞ╗Š▓ëŠÁ«´╝îňĄžňĆ»Šťčňżů´╝ü
ňůŹŔ┤úňú░ŠśÄ
šŤŞňů│ňćůň«╣ňč║ń║ÄňĚ▓ňůČň╝ÇšÜäŔÁ䊾֊łľń┐íŠü»Šĺ░ňćÖ´╝îńŻćŠťČňůČňĆŞńŞŹń┐ŁŔ»üŔ»ąšşëń┐íŠü»ňĆŐŔÁ䊾֚Üäň«îŠĽ┤ŠÇžŃÇüňçćší«ŠÇž´╝îŠëÇňÉźń┐íŠü»ňĆŐŔÁ䊾Öń┐ŁŠîüňťĘŠťÇŠľ░šŐŠÇüŃÇéňÉ´╝ČňůČňĆŞŠťëŠŁâň»╣ŠťČŠŐąňĹŐŠëÇňÉźń┐íŠü»ňťĘńŞŹňĆĹňç║ÚÇÜščąšÜäŠâůňŻóńŞőňüÜňç║ń┐«Šö╣´╝îÚśůŔ»╗ŔÇůň║öňŻôŔç¬Ŕíîňů│Š│ĘšŤŞň║öšÜ䊍┤Šľ░Šłľń┐«Šö╣ŃÇé
ňťĘń╗╗ńŻĽŠâůňćÁńŞő´╝Ț»çŠľçšźáńŞşšÜäń┐íŠü»ŠłľŠëÇŔíĘŔ┐░šÜäŠäĆŔžüňŁçńŞŹŠ×䊳Éň»╣ń╗╗ńŻĽń║║šÜäŠŐĽŔÁäň╗║Ŕ««´╝áŔ«║Šś»ňÉŽňĚ▓š╗ĆŠśÄšĄ║ŠłľŠÜŚšĄ║´╝ȊչňĹŐńŞŹŔâŻńŻťńŞ║Úüôń╣ëšÜäŃÇüŔ┤úń╗╗šÜäňĺîŠ│ĽňżőšÜäńżŁŠŹ«ŠłľŔÇůňçşŔ»üŃÇéňťĘń╗╗ńŻĽŠâůňćÁńŞő´╝ČňůČňĆŞń║ŽńŞŹň»╣ń╗╗ńŻĽń║║ňŤáńŻ┐šöĘŠťČŠľçšźáńŞşšÜäń╗╗ńŻĽňćůň«╣ŠëÇň╝ĽŔç┤šÜäń╗╗ńŻĽŠŹčňĄ▒Ŕ┤čń╗╗ńŻĽŔ┤úń╗╗ŃÇ銝Ȋľçšźáń╗ůńŞ║ŠťČňůČňĆŞŠëÇŠťë´╝¬š╗Ćń║őňůłń╣ŽÚŁóŔ«ŞňĆ»´╝îń╗╗ńŻĽŠť║Š×äňĺîńެń║║ńŞŹňżŚń╗ąń╗╗ńŻĽňŻóň╝Ćš┐╗šëłŃÇüňĄŹňłÂŃÇüňĆĹŔíĘŃÇüŔŻČňĆĹŠłľň╝ĽšöĘŠťČŠŐąňĹŐšÜäń╗╗ńŻĽÚâĘňłćŃÇé