点石观点:
(2)本次政策将对政府引导基金产生多方面的深刻影响。在定位上,促使其更精准聚焦重大战略与薄弱环节,强化产业和创业投资引导作用。管理机制上,分级分类管理更加精细,规范设立审批与预算管理,提升运作效率。统筹布局层面,加强国家级与地方基金联动,避免重复投资,优化资源配置。运作模式方面,提升专业化市场化程度,规范投资决策与监督,完善绩效和容错机制。退出机制上,政策指引和渠道拓宽保障资金循环。整体推动政府引导基金管理更科学、运作更高效,更好服务经济发展。
(一) 明确基金定位
(二) 优化产业投资类基金功能
(三) 鼓励发展创业投资类基金
(四) 发展壮大长期资本、耐心资本
二、完善分级分类管理机制
(五) 明确对基金设立的分级管理要求
(六) 完善不同类型基金差异化管理机制
(七) 规范各类政府出资预算管理
三、加强统筹,整合优化布局
(八) 国家级基金与地方基金形成合力
(九) 省级政府加强本地区基金统筹管理
(十) 加强基金布局规划和投向指导
(十一)推动基金整合优化
四、提升专业化市场化运作水平
(十二)规范基金运作管理
(十三)优化基金投资方式
(十四)充分发挥基金管理人作用
(十五)健全基金绩效管理
(十六)建立健全容错机制
(十七)优化基金发展环境
五、优化退出机制,促进投资良性循环
(十八)规范基金退出管理
(十九)拓宽基金退出渠道
(二十)完善基金退出机制
六、强化内控建设,防范化解风险
(二十一)健全风险防控体系
(二十二)严肃财经纪律
七、加强组织保障
(二十三)坚持和加强党的领导
(二十四)加强部门协同
(二十五)规范监管行为
(1)为医药产业发展注入强心剂。在知识产权保护方面,给予特殊药品数据保护期与市场独占期,激发研发积极性,让企业敢投入、愿创新,为罕见病、儿童用药等领域带来更多希望。审评审批质效提升,缩短补充申请审评时限、优化原料药管理,加速药品上市进程,患者能更快用上新药、好药。同时,支持中药研发创新,推动传统中药向新药转化,传承与创新并重,有望让中医药在现代医疗体系中发挥更大价值。
对部分药品获批上市时,对注册申请人提交的自行取得且未披露的试验数据和其他数据,分类别给予一定的数据保护期。对符合条件的罕见病用药品、儿童用药品、首个化学仿制药及独家中药品种给予一定的市场独占期。
二、积极支持创新药和医疗器械推广使用
加大创新药临床综合评价力度,加强评价结果分析应用。研究试行以药学和临床价值为基础的新上市药品企业自评,优化新上市药品挂网服务。坚持基本医疗保险“保基本”功能定位,完善医保药品目录调整机制,研究规范医保医用耗材目录和医疗服务项目目录,按程序将符合条件的创新药和医疗器械纳入医保支付范围,鼓励医疗机构采购使用。
三、加大中药研发创新支持力度
完善中医药理论、人用经验和临床试验相结合的中药特色审评证据体系,建立医疗机构规范收集整理人用经验数据的机制。健全符合中药特点的中药监管体系。积极支持名老中医方、医疗机构中药制剂向中药新药转化。鼓励运用符合产品特点的新技术、新工艺、新剂型改进已上市中药品种。
四、提高药品医疗器械审评审批质效
优化药品补充申请审评审批,省级药品监管部门提出申请,国家药监局同意后,在部分地区开展优化药品补充申请审评审批程序改革试点,需要核查检验的补充申请审评时限由200个工作日缩短为60个工作日。优化原料药管理,原料药登记主体可依法变更。
五、以高效严格监管提升医药产业合规水平
提高药品医疗器械监督检查效率,强化面向企业的质量安全警示教育,督促企业全面完善质量管理体系。根据企业和产品风险等级合理确定检查频次,减少重复检查。
六、支持医药产业扩大对外开放合作
优化药品医疗器械进口审批,简化香港、澳门已上市传统口服中成药审评审批。优化进口药材管理,扩大境外优质药材资源进口。
七、探索生物制品分段生产模式
省级药品监管部门提出申请,国家药监局同意后,在部分地区开展生产工艺、设施设备有特殊要求的生物制品分段生产试点,率先推进抗体偶联药物、多联多价疫苗等分段生产。支持符合条件的境外药品上市许可持有人在统一的药品质量管理体系下,以自建产能或者委托生产形式开展跨境分段生产。
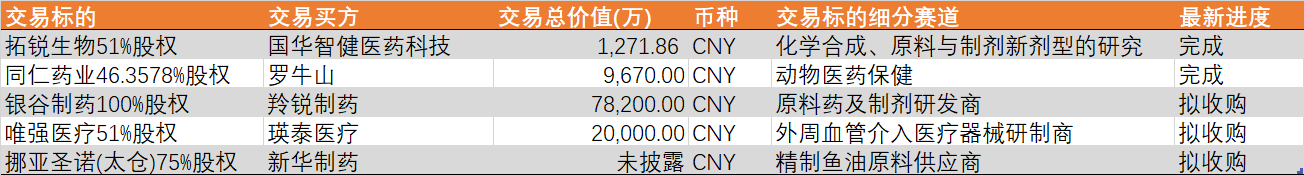
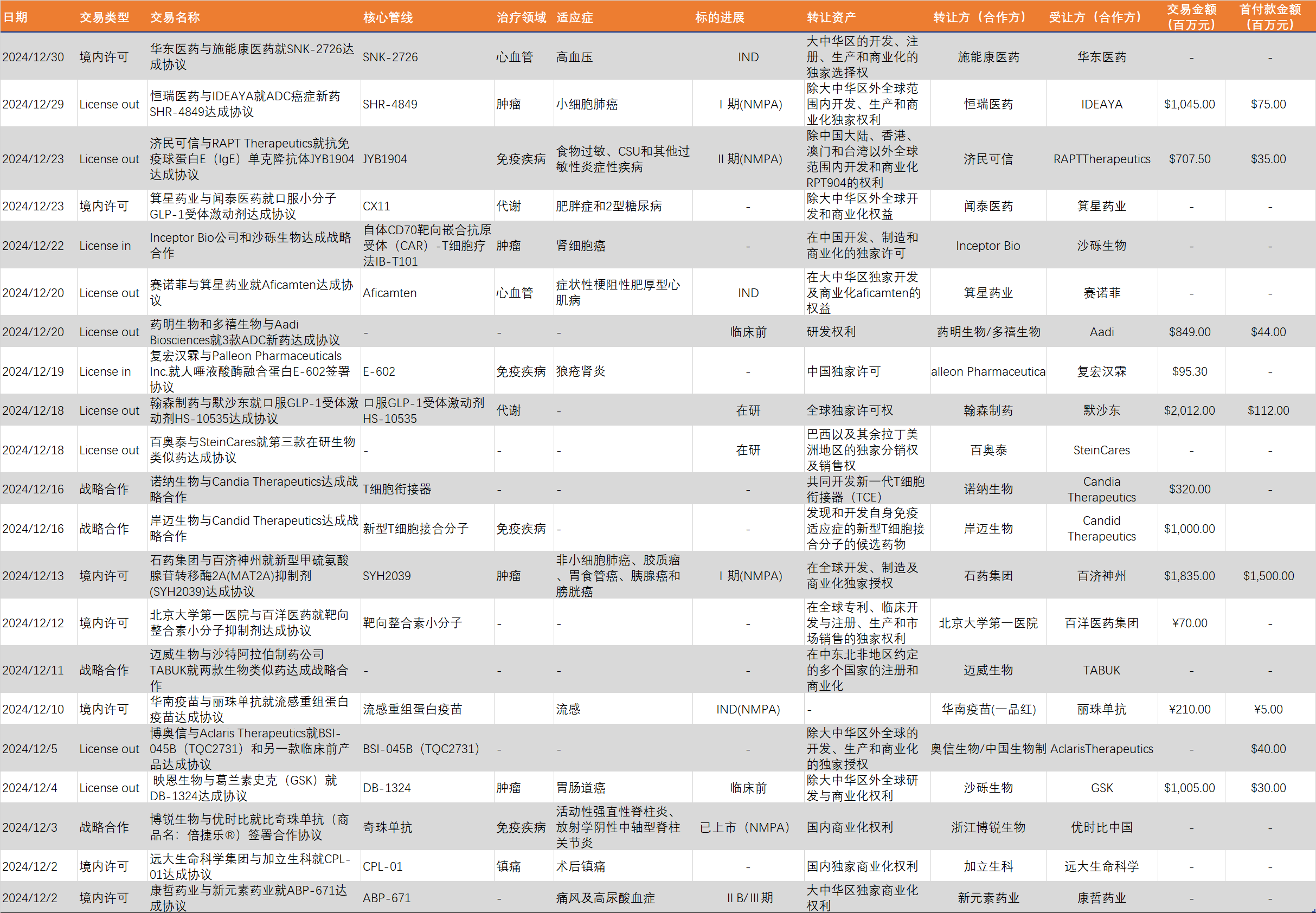
表1:12月新药交易/合作项目一览
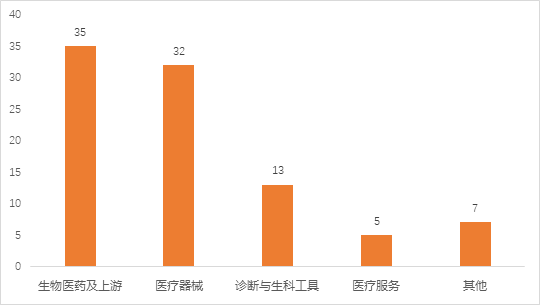
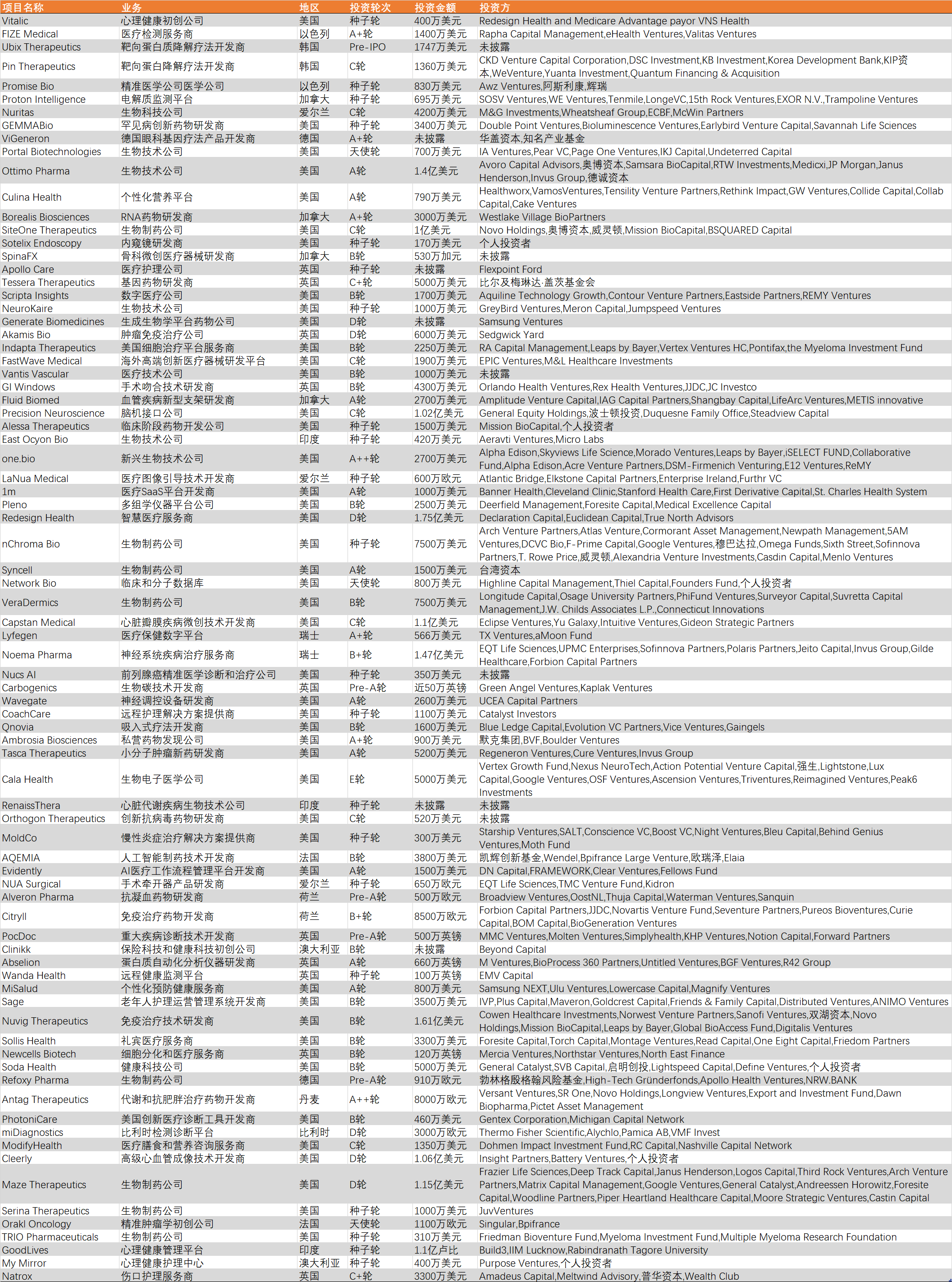
2024年12月,国内一级市场投资92家医疗企业,以生物医药及医疗器械方向为主。本月,生物医药投资项目多集中于AI+方向;医疗器械方面,多家机器人公司披露融资;诊断及生科工具方面,多家类器官厂商完成融资。
图1:2024年12月国内医疗健康领域投资主要分布在生物医药、医疗器械:
资料来源:点石资本数据库
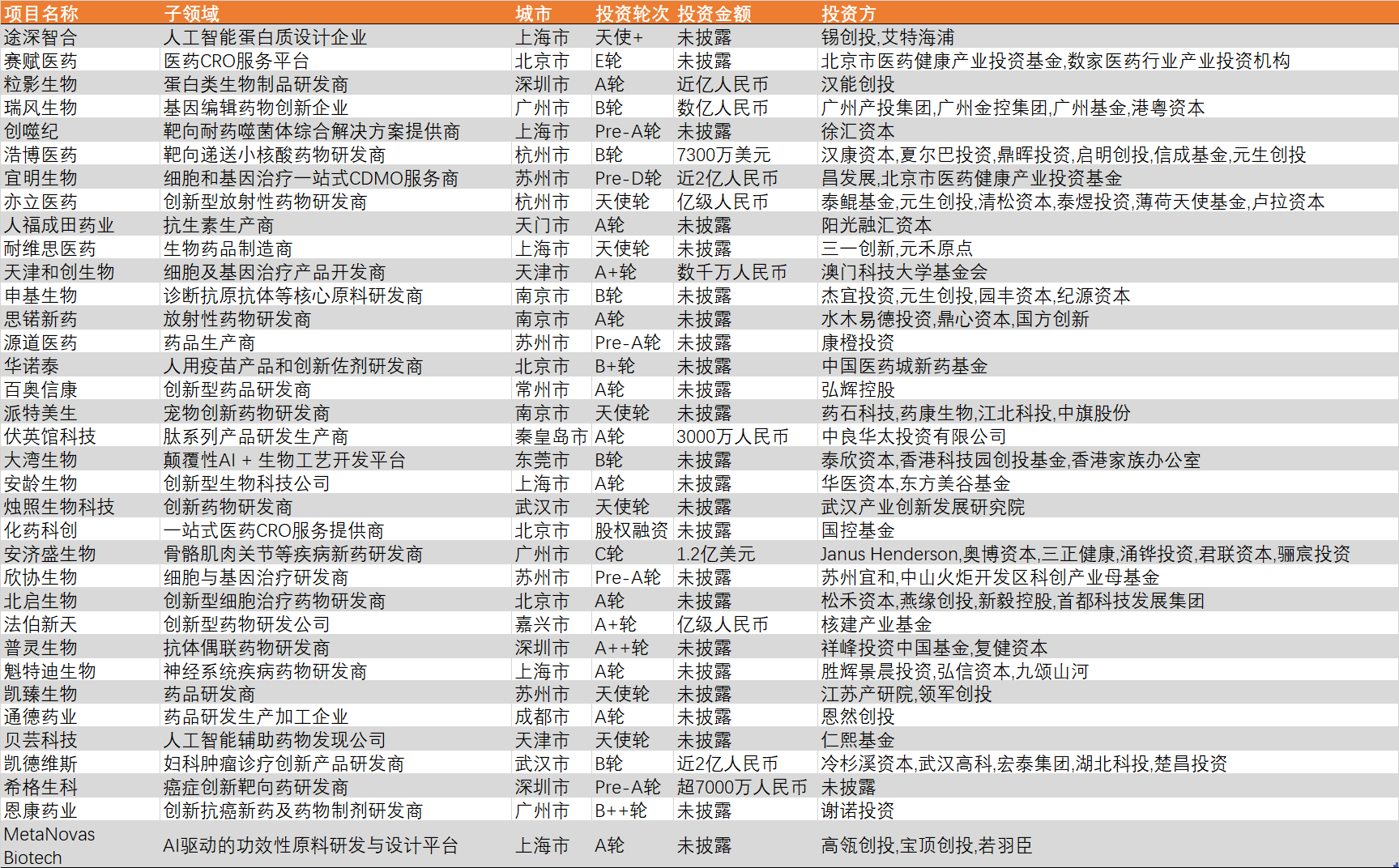
资料来源:点石资本数据库
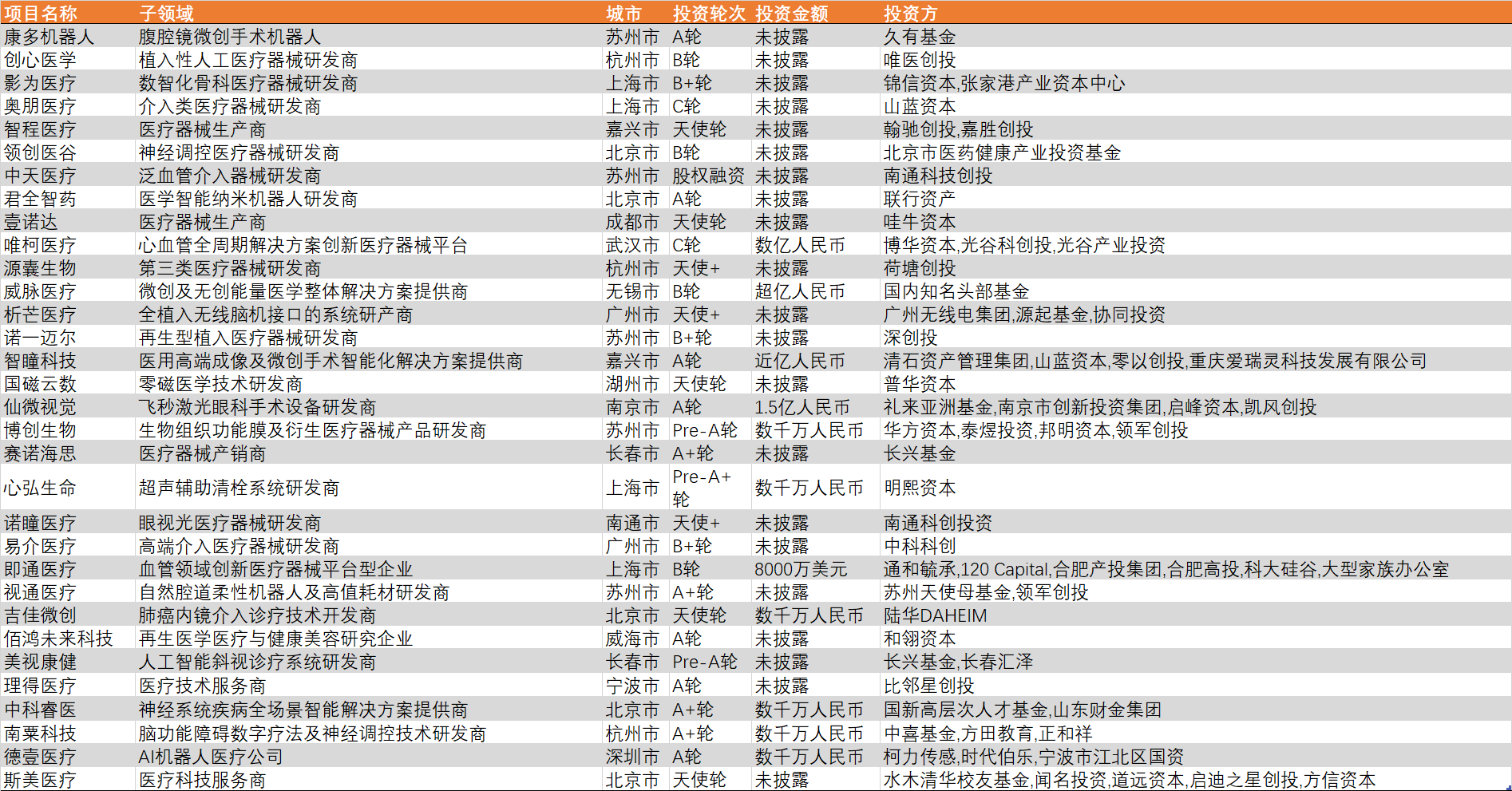
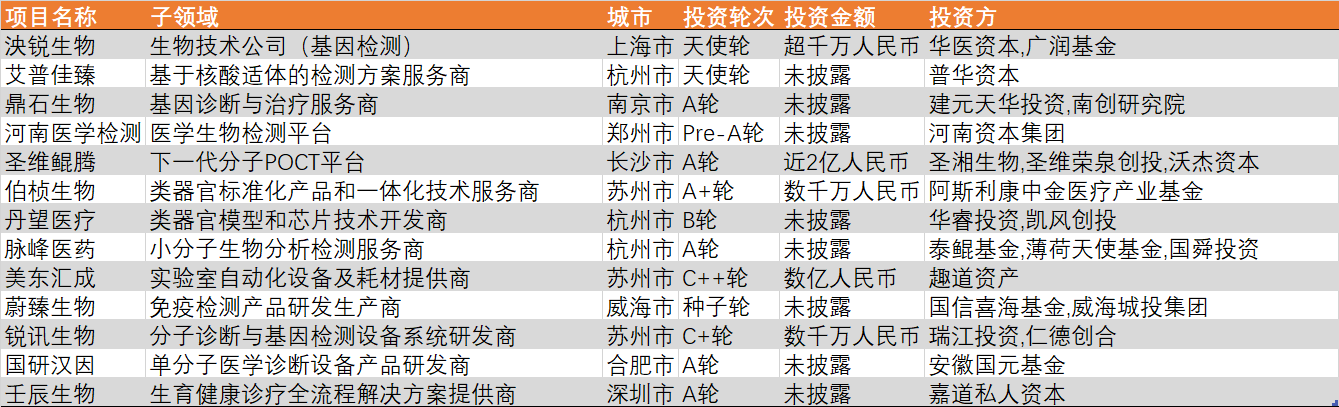
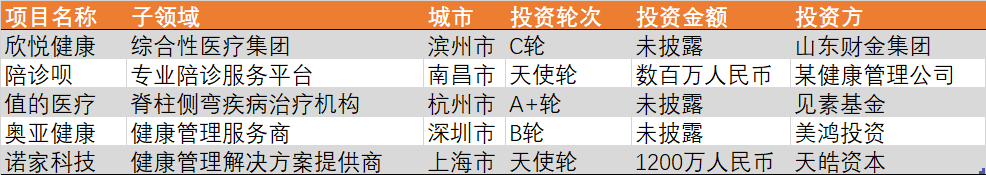
资料来源:点石资本数据库
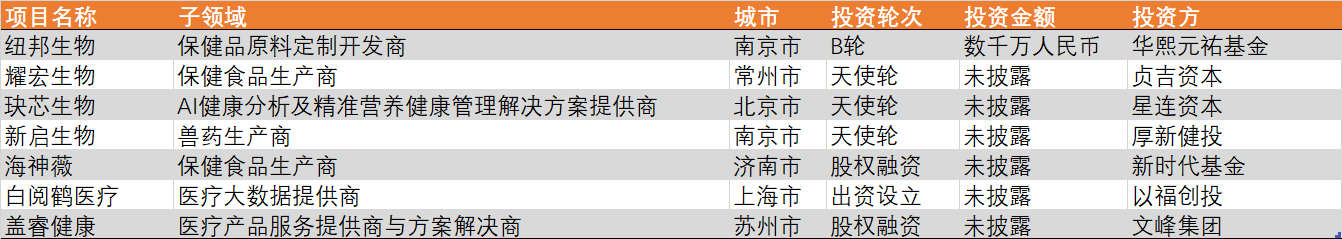
资料来源:点石资本数据库
本月海外投融资事件的重点关注方向主要在于基因治疗。12月25日,由“基因疗法先驱”James Wilson创立的公司GEMMA Biotherapeutics获得3400万美元种子轮融资,以推动其基因药物的研发。这轮投资由Double Point Ventures、Biolescence Ventures和Earlybird Venture Capital共同牵头,并得到了Savanne Life Sciences的额外支持。GEMMABio于2024年8月成立,是一家基因治疗公司,为罕见病患者开发创新药物。GEMMABio已获得三种临床阶段基因治疗候选药物的全球独家开发和商业化的权利,均针对严重儿科疾病,分别是PBGM01(用于治疗GM1神经节苷脂沉积症)、PBKR03(用于治疗克拉伯病)和PBML04(用于治疗异染性脑白质营养不良症)。12月23日,德国创新基因治疗公司ViGeneron完成A+轮融资,由华盖资本领投,知名产业基金跟投。本轮融资资金主要用于推进两款眼科基因治疗药物的临床开发。ViGeneron针对未被满足的眼科疾病需求构建了丰富的产品管线,其中两款产品已获得美国食品药品监督管理局(FDA)或欧洲药品管理局(EMA)的批准,并进入临床试验阶段。
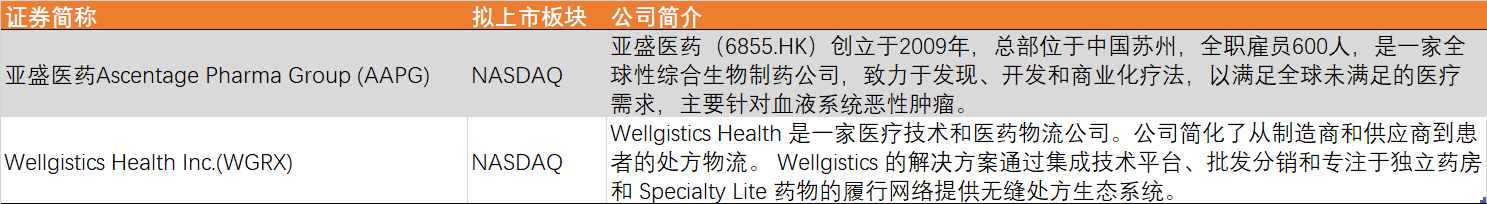

资料来源:Wind