政策速递
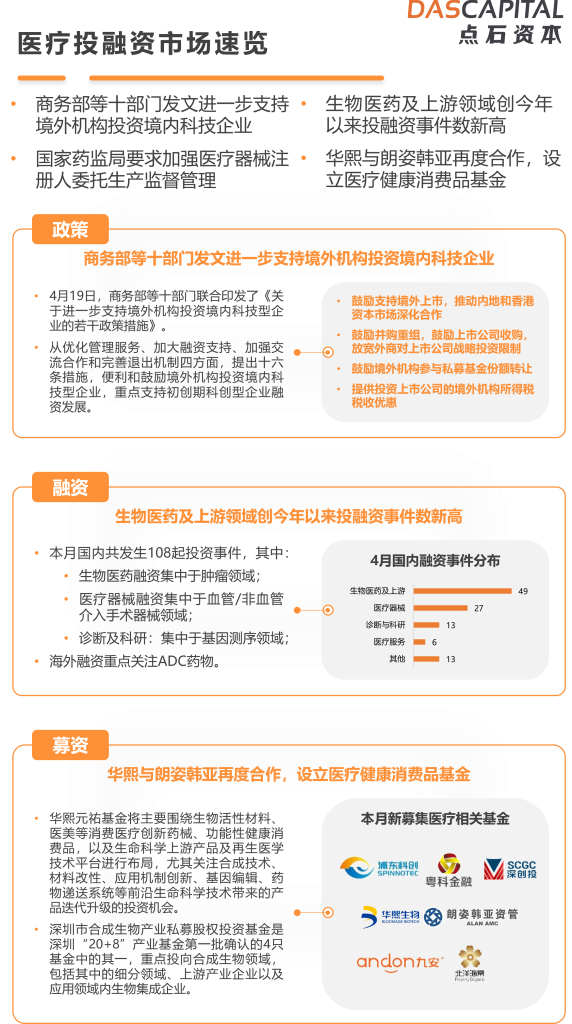
商务部再发文支持境外机构投资,药监局加强医疗器械管理措施
资本市场政策
4月22日,商务部、外交部、国家发展改革委、科技部、工业和信息化部、中国人民银行、税务总局、金融监管总局、中国证监会、国家外汇局十部门联合印发《关于进一步支持境外机构投资境内科技型企业的若干政策措施》。
点石观点:
(1)此政策措施彰显了国家积极开放市场、吸引外资投资科技型企业的决心,有助于提升国内科技创新能力,推动经济高质量发展。
(2)通过优化管理服务、加大融资支持等措施,为境外机构投资境内科技型企业提供了更加便利的环境,将有效促进国际资本与本土科技的深度融合。
(3)此举不仅有利于境外机构分享中国科技创新的机遇,也为中国科技型企业提供了更多融资渠道,有助于推动科技创新成果的转化和应用。
中国证监会等部门围绕境外上市、并购重组、份额转让等退出渠道,推出了一系列配套举措。
一是支持境外上市。将持续提高境外上市备案管理质效,加快备案办理进度,持续畅通科技型企业境外上市渠道。同时,继续推动内地和香港资本市场深化务实合作,加强香港科技型企业国际融资平台作用。自2023年3月31日《境内企业境外发行证券和上市管理试行办法》施行至2024年3月底,已办结122家企业赴境外首次公开发行上市的备案,其中71家企业拟赴香港上市。
二是鼓励并购重组。中国证监会先后出台定向可转债重组规则、修订重大资产重组规则、适当提高重组估值包容性,支持上市公司并购科技型企业,畅通投资机构退出渠道;近期进一步从分类监管、提高重组审核效率、支持“两创”公司协同效应并购、支持上市公司之间吸收合并等四方面优化并购重组有关制度,下一步将继续推进并购重组市场化改革,发挥资本市场并购重组主渠道功能,为境外机构投资境内科技型企业提供畅通的退出渠道。商务部正牵头修订《外国投资者对上市公司战略投资管理办法》,进一步放宽外国投资者对上市公司战略投资限制。
三是推进私募基金份额转让试点。将继续优化私募份额转让流程和定价机制,推动私募基金和区域性股权市场的协同发展,拓宽私募基金退出渠道,形成“投资—退出—再投资”良性循环,在此过程中鼓励和支持境外机构发挥专业优势和特长,积极参与相关投资交易。近年来,我国先后在北京、上海、广东、浙江、宁波、江苏、安徽等区域性股权市场开展私募份额转让试点,各地出台了一些支持性政策措施,推动市场生态建设,并搭建了基于区块链的交易系统。截至目前,7个省市实现私募份额转让231.72亿元、私募份额质押融资316.07亿元。同时,目前私募份额转让还存在底层资产不清晰、估值定价难、市场化机构参与度低、市场生态体系不健全等问题,相关部门将继续完善基于区块链的场外市场基础设施,建立数据可信共享和授权访问机制,不断完善市场生态,促进私募基金和区域性股权市场形成“双赢”局面。
四是便利享受税收优惠。根据我国与相关国家签订的税收协定,符合条件的境外机构投资我国境内上市公司,可享受所得税税收优惠。目前,境外机构参与所投上市公司分红派息时,需先提交《非居民纳税人享受协定待遇信息报告表》,才可享受协定优惠待遇,否则将由上市公司代扣代缴,再事后申请补充享受优惠待遇并办理退税。近期部分境外机构反映,在投资上市公司数量较多时,享受有关优惠待遇操作成本较高,总体不够便利。针对境外机构需求,税务总局、中国证监会、商务部深入调研,积极研究进一步优化上市公司派息扣缴税款和结算程序。通过畅通政府部门、结算机构、上市公司信息交互,实现上市公司可直接按优惠规定对相关境外机构进行扣缴申报和派息,无需先行代扣代缴后再由境外机构申办退税,境外机构也无需每次向各个上市公司提交相关信息报告表。具体可见与《若干措施》配套发布的《便利境外机构享受有关税收的协定优惠操作指引》。
医疗行业政策
4月3日,为贯彻实施《医疗器械监督管理条例》,全面落实医疗器械注册人(以下简称注册人)质量安全主体责任,进一步加强注册人委托生产监督管理,有效防控医疗器械质量安全风险,国家药监局发布关于进一步加强医疗器械注册人委托生产监督管理的公告,6月1日实施。
点石观点:
(1)医疗器械注册人应切实承担起质量安全主体责任,确保从设计、生产到上市后监督的每一环节都符合法规要求,保障公众健康安全。监管部门应加大监督力度,对违法行为零容忍。
(2)加强医疗器械注册人委托生产的监督管理至关重要。通过严格审核受托企业资质、完善委托生产合同管理制度以及加强监督检查,可以确保医疗器械生产的质量和安全。
(3)医疗器械监管中,应充分利用信息化手段提高监管效率和质量。建立医疗器械监管信息平台,实现信息共享和交流,有助于及时发现问题并采取有效措施,进一步保障医疗器械的质量安全。
(一)注册人应当全面落实医疗器械质量安全主体责任,建立覆盖医疗器械全生命周期的质量管理体系并保持有效运行。注册人委托生产的,应当建立健全与所委托生产的产品特点、企业规模相适应的管理机构,充分履行产品风险管理、变更控制、产品放行、售后服务、产品投诉处理、不良事件监测和产品召回等职责,定期按照医疗器械生产质量管理规范对受托生产企业质量管理体系运行情况进行审核。
注册人仅委托生产时,也应当保持产品全生命周期质量管理能力,维持质量管理体系完整性和有效性;设置与委托生产相适应的管理机构,并至少明确技术、生产、质量管理、不良事件监测、售后服务等相关部门职责,质量管理部门应当独立设置,配备足够数量和能力的专职质量管理人员,以及熟悉产品、具有相应专业知识的技术人员,能够对委托生产活动进行有效的监测和控制。
注册人应当能够依法承担医疗器械质量安全责任,鼓励通过购买商业保险等形式,建立与产品风险程度、市场规模和人身损害赔偿标准等因素相匹配的责任赔偿能力。
(二)注册人应当优先选择质量管理水平较高、生产规模较大、信用记录良好、生产自动化程度和信息化管理水平较高的企业作为受托方。进行委托生产前,注册人应当要求受托方提交信用情况说明,并查阅监管部门公开信息,全面了解受托方信用情况。
-
国家药监局器审中心计划编制医疗器械注册审查指导原则
4月11日,国家药监局器审中心网站公布《关于发布2024年度医疗器械注册审查指导原则编制计划的通告(2024年第17号)》。《计划》包括109项医疗器械注册审查指导原则,主要包括《医疗器械磁共振安全评价指导原则》《一次性使用麻醉穿刺针注册审查指导原则》《幽门螺杆菌耐药基因检测试剂注册审查指导原则》《植入式心脏起搏器注册审查指导原则(2024年修订版)》《医疗器械附条件批准上市指导原则(2024年修订版)》《医用中心吸引系统注册审查指导原则》《一次性使用鼻镜产品注册审查指导原则》《输液泵注册审查指导原则(2024年修订版)》。
点石观点:
(1)国家药监局发布的医疗器械注册审查指导原则编制计划,涵盖了从磁共振安全到医用中心吸引系统的广泛领域,显示出对医疗器械安全监管的细致与全面,有助于提升行业标准和保障患者安全。
(2)2024年度医疗器械注册审查指导原则的发布,不仅更新了多项重要产品的审查标准,还特别修订了部分原则,体现了监管部门对医疗器械行业发展的动态关注和及时调整,有助于行业健康有序发展。
(3)该计划中的指导原则不仅包含了传统医疗器械的注册审查,还涵盖了耐药基因检测试剂等新型产品,显示了国家药监局在保障医疗器械安全、促进科技创新方面的前瞻性和积极性。
| 序号 |
指导原则名称 |
| 1 |
医疗器械磁共振安全评价指导原则 |
| 2 |
造影剂高压注射设备注册审查指导原则 |
| 3 |
X射线血液辐照设备注册审查指导原则 |
| 4 |
便携式电动输液泵注册审查指导原则 |
| 5 |
体外膜肺氧合设备动物试验注册审查指导原则 |
| 6 |
放射治疗计划软件注册审查指导原则 |
| 7 |
射线束扫描测量系统注册审查指导原则 |
| 8 |
腹腔内窥镜手术系统注册审查指导原则 |
| 9 |
有源光学设备荧光诊断功能技术指导原则 |
| 10 |
二氧化碳激光治疗机注册审查指导原则 |
| 11 |
肿瘤射频消融设备注册审查指导原则 |
| 12 |
电凝切割内窥镜注册审查指导原则 |
| 13 |
胶囊式内窥镜系统注册审查指导原则 |
| 14 |
泌尿系统激光治疗机注册审查指导原则 |
| 15 |
腹腔内窥镜手术系统注册审查指导原则 |
| 16 |
主动脉覆膜支架注册审查指导原则 |
| 17 |
脱细胞基质软组织创面修复材料产品注册审查指导原则 |
| 18 |
经导管瓣膜夹系统注册审查指导原则 |
| 19 |
记忆合金肋骨板注册审查指导原则 |
| 20 |
金属骨针注册审查指导原则 |
资金募集情况
-
上海国际集团设立的基金完成首关签约,首关规模1.66亿元
4月3日,由上海国际集团发起设立、上海科创基金管理的上海国际集团创领一期创业投资合伙企业(有限合伙)正式完成首关签约,首关金额1.66亿元。该基金是上海国资体系内首支市区联动、专注于“投早投小投科技”的直投基金。基金目标规模10亿元,首期规模约2亿元,立足集成电路、生物医药、人工智能三大先导产业中具备前瞻性、颠覆性的关键核心技术领域,瞄准原始创新、科技成果转化等阶段的创新创业项目,与超前孵化基地、概念验证中心、高校成果转化中心、产业链龙头企业等密切合作,打造投资、培育、招引、落地一体化推进模式,推动科技创新与资本要素高水平融合,全力支持服务科创中心核心区建设。
4月3日,浙江省“专精特新”(温州)母基金正式落地,完成签约,标志着温州市与浙江省政府在产业基金领域的深度合作迈出了实质性步伐。“专精特新”母基金总规模30亿元,其中社会资本募资40%,基金管理人为粤科金融集团。“专精特新”母基金将助推温州产业提速转型,依托该基金在招商引资和产业培育的引导优势,锚定温州市“5+5+N”重点产业领域和重点项目,引导基金精准滴灌,不断扩大温州市在“专精特新”领域的优势,加快培育和发展新质生产力,提速构建更具竞争力的现代化产业体系。
4月6日,在江西上饶经济技术开发区产业与资本对接大会上发布了上饶经开区新质产业基金。该基金规模30亿元,主要定位为组建中小规模子基金,与同步发布的上饶市现代产业引导基金、上饶高新基金共同构建产业基金新体系,主要围绕光伏新能源、光电和新能源(锂电)汽车三大主导产业,生物医药、新材料等N个特色产业的转型升级和重大项目招商引资进行投资,培育发展新质生产力,推动上饶经开区实现高质量发展。
4月8日,乐创基金“乐土战新股权投资(海南)合伙企业(有限合伙)”已完成第一期实缴,并已于4月8日通过中国证券投资基金业协会基金产品备案。乐创基金是由乐山市政府投融资机构与富航资本等共同发起设立的投资基金。此前管理了两支基金,一支是乐西物流产业投资基金,一支是与乐山高新区成立的乐山创聚股权投资基金。乐土战新基金总规模4000万元,将主要投资于新能源及网络安全、网联汽车、新型显示和智能终端、生物医药、节能环保、新一代人工智能、尼龙新材料、智能装备、智能传感器、5G和煤化工新材料等新兴产业及优势特色产业链条上的成长期、成熟期创新型企业,不断提升金融服务实体经济的能力。
4月16日,华熙生物与朗姿韩亚资管达成战略合作,在华熙生物(海南)科技产业园成立国内首支专注于医疗健康消费品赛道的CVC—海南华熙元祐医疗健康消费品产业基金,该基金投资方向主要聚焦于创新药械、新兴健康消费品以及再生医学创新技术平台这几大核心领域。在创新药械领域,该产业基金将重点关注可再生材料、基因编辑、药物递送系统等前沿技术,特别关注医美、皮肤、眼科、骨科、口腔等消费属性强的产品。同时,也将关注先进设备和创新光电技术在这些领域的应用机会。同时,该基金还通过保持并强化在核心赛道上的技术领先地位,推动华熙生物以大分子功能化修饰为核心的材料科学技术发展,为华熙生物储备相关领域的二、三类医疗器械、药品及消费品原料的生产及商业化管线,进一步巩固华熙生物在再生医学及相关材料学科的行业领先地位。
4月16日,天开九安海河海棠科创母基金正式注册成立,该母基金由九安医疗、天开集团、海河产业基金、天津大学北洋教育发展基金会与北洋海棠基金共同设立,规模50亿元,重点投资硬科技、医疗大健康、人工智能、生物制造、新能源新材料等新技术及应用。截至目前,天开九安海河海棠基金首期基金已认缴到位。规模方面,首期基金不超过12.51亿元,九安医疗与海棠创投首次联手出资预计不超过3.5亿元,后续资金将在4年内陆续实缴。
-
浙江省科创母基金(二期)子基金落地义务,规模30.02亿元
4月18日,在浙江省科创母基金(一期)顺利运作的基础上,浙江省产业基金与金华、义乌国资平台共同出资设立浙江省科创母基金(二期),规模30.02亿元。该基金首次引入社会资本出资参与组建,主要围绕“互联网+”、生命健康、新材料三大科创高地,聚焦云计算与未来网络等15大战略领域、“9+6”未来产业,重点投早投小、投创新赛道、投创新人才。浙江省科创母基金(二期)由浙江金投盛领私募基金管理有限公司(以下简称“金投盛领”)担任基金管理人。
4月28日,工融国化(北京)股权投资基金合伙企业(有限合伙)成立,该企业由工银资本管理有限公司(认缴出资23.99亿元)和国化私募基金管理(北京)有限公司(认缴出资5.99亿元)共同担任执行事务合伙人。据官网,“中国化学工程集团”旗下的“国化投资”,是集团的投资并购和产融服务平台,积极响应国资央企大力发展战略性新兴产业的号召,践行“两台一商”战略定位(战略新兴产业管控平台、科技创新成果转化平台、现代产融结合服务提供商),加快培育先进新材料、高端化学品、绿色低碳、咨询服务四大产业集群,努力建设成“股权投资+产业运营+产融服务”一体化战略性新兴产业投资运营型企业集团。
4月30日,深圳市合成生物产业私募股权投资基金合伙企业完成工商登记,初期出资额达15亿元,由深创投红土私募股权投资基金管理(深圳)有限公司担任执行事务合伙人。该基金是深圳“20+8”产业基金第一批确认的4只基金中的其一。该基金存续期不超过10年,投向合成生物领域,包括其中的细分领域、上游产业企业以及应用领域内生物集成企业。从出资比例来看,深圳市引导基金、深创投为主要出资方,认缴比例分别为40%、39%;深圳市光明区引导基金投资管理有限公司持股10%;深圳市大鹏新区引导基金投资有限公司持股约3.33%,深圳市汇通金控基金投资有限公司持股约3.33%,深圳市盐田区国有资本投资管理有限公司持股约3.33%。
新药转让回顾
一级市场国内外医疗领域融资
3.1 国内医疗融资:重点关注抗肿瘤新药、介入器械、基因检测研发
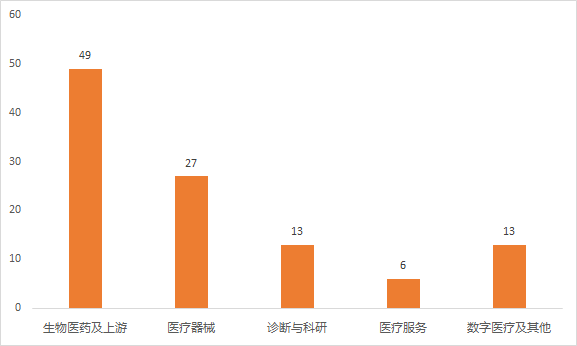
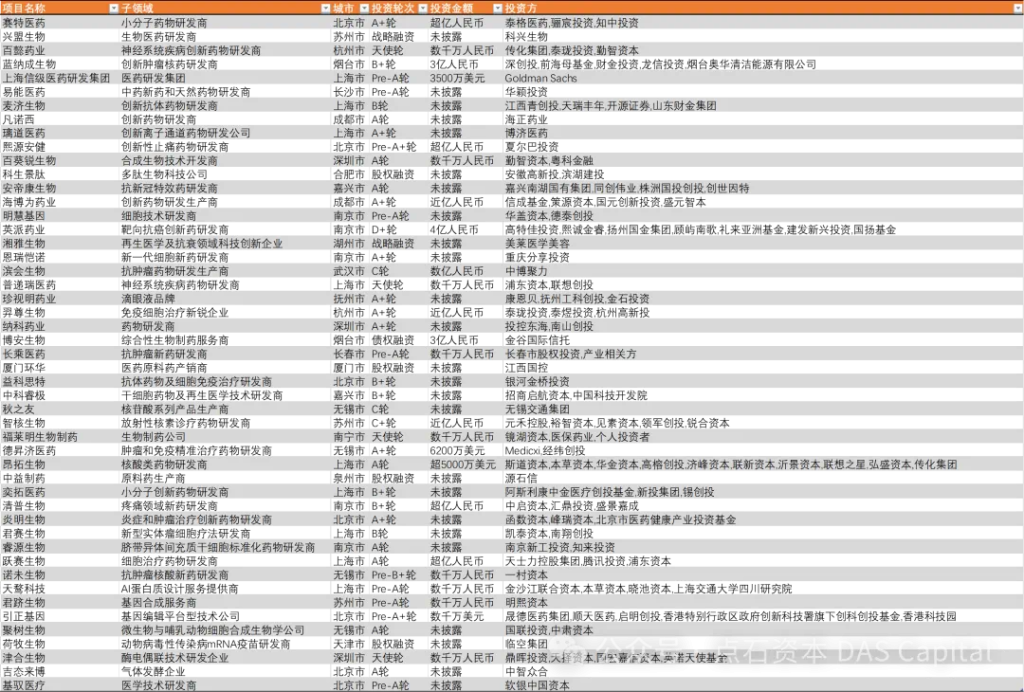
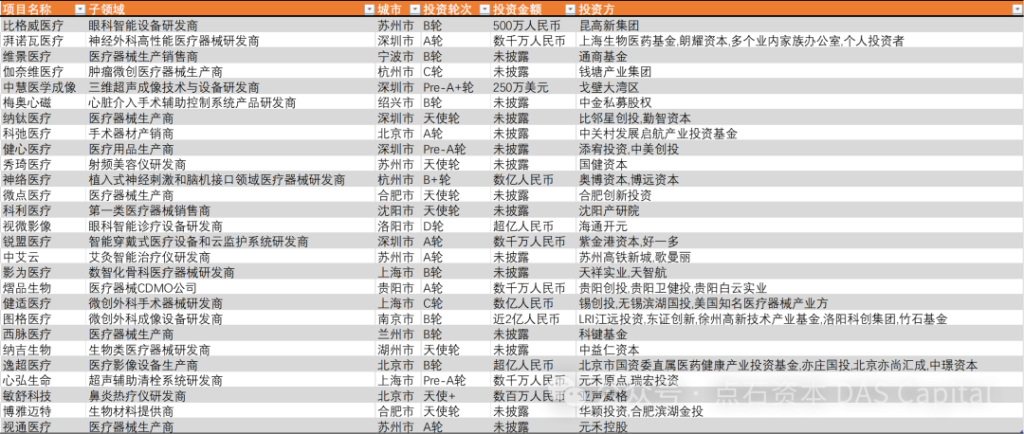
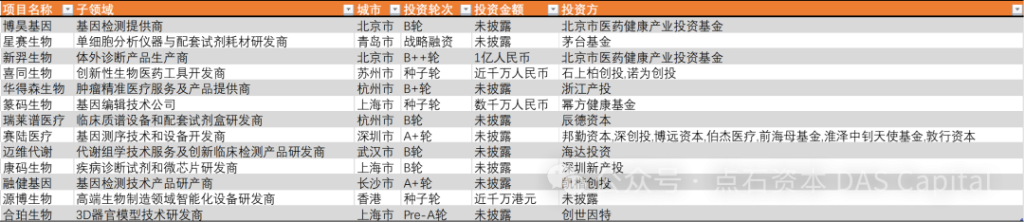
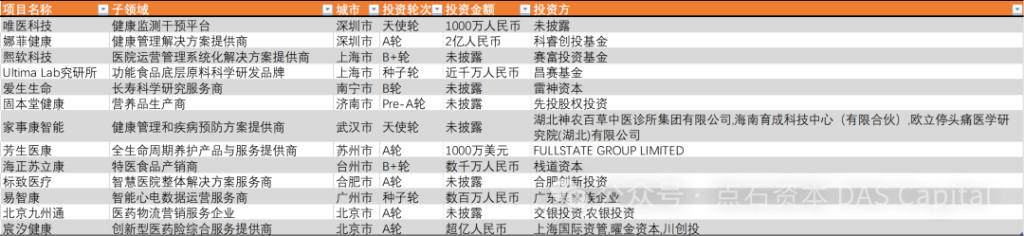
2024年4月,国内一级市场投资108家医疗企业,以生物医药及医疗器械方向为主。本月,生物医药投资项目多集中于肿瘤研发方向;医疗器械方面,多家介入类器械公司披露融资;诊断及生科工具方面,披露融资主要集中于基因检测技术产品研发。
图1:2024年4月国内医疗健康领域投资主要分布在生物医药、医疗器械及数字医疗:
资料来源:点石资本数据库
本月海外投融资事件的重点关注方向主要在ADC药物和医疗服务平台。TORL BioTherapeutics完成1.58亿美元B2轮融资,获得的资金将用于推动该公司研发管线中的多款潜在“first-in-class”和“best-in-class”ADC的临床开发。本轮融资由Deep Track Capital领投,包括Goldman Sachs Alternatives、UC Investments、百时美施贵宝、Vertex Ventures在内的现有投资者也参与了融资。该公司的主打在研疗法TORL-1-23是一款靶向CLDN 6的潜在“first-in-class”ADC,目前正在1期临床试验中接受评估,预计在今年下半年启动2期临床试验。这一临床试验旨在支持TORL-1-23的监管审评和潜在批准,用于治疗CLDN 6阳性,对含铂化疗耐药的卵巢癌。Endeavor BioMedicines完成了1.325亿美元的C轮融资。本轮融资由Matrix Capital Management旗下的AyurMaya领投,Fidelity Management & Research Company、Ally Bridge Group、Avidity Partners等跟投。获得的资金将用于推动其主打在研疗法ENV-101的临床开发,这款小分子疗法旨在治疗特发性肺纤维化(IPF)和进行性肺纤维化(PPF)。此外,这笔资金还将支持ENV-501的临床概念验证研究,ENV-501是一种针对人表皮生长因子3(HER3)阳性实体瘤的抗体偶联药物(ADC)。最近完成的随机双盲、安慰剂对照的2a期临床试验的初步结果凸显了ENV-101改变疾病进程的潜力,并为IPF患者提供了超出延缓疾病进展的治疗效果。这些研究结果将在五月份的美国胸科学会(ATS)国际会议上展示。Endeavor计划在2024年为IPF患者启动一项2b期临床试验,并同时开展PPF患者队列的研究。
IPO和并购
4.1 IPO:上海细胞治疗集团冲刺港股IPO,或将成为港交所免疫细胞储存第一股
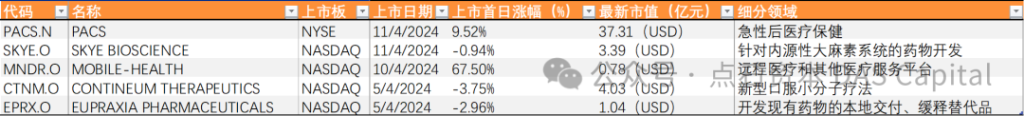
4月,纳斯达克1家公司申报IPO,港交所本月4家公司申报。创新型生物制药公司华芢生物、肿瘤医疗集佰泽医疗、内地民营医院领导者明基医院均向港交所主板递交上市申请。此外,4月30日,专注细胞医疗健康赛道的上海细胞治疗集团有限公司向港交所主板递交上市申请,或将成为港交所免疫细胞储存第一股。本月国内暂无上市。海外上市方面,纳斯达克上市4家企业,纽交所上市1家企业。

资料来源:Wind
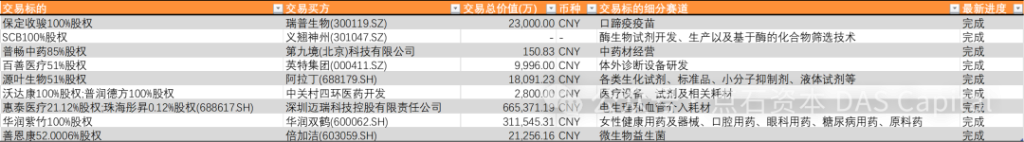
资料来源:Wind
4.2 并购:阿拉丁完成对源叶生物51%股权的收购